题目内容
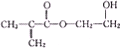 甲基丙烯酸烃乙酯是一种有机合成中重要的原料,其结构简式如图所示,下列有关说法错误的是( )
甲基丙烯酸烃乙酯是一种有机合成中重要的原料,其结构简式如图所示,下列有关说法错误的是( )| A、能发生加成反应 |
| B、能发生取代反应 |
| C、一定条件下,能与乙醇发生酯化反应 |
| D、既能是溴水褪色,又能使酸性高猛酸钾溶液褪色 |
考点:有机物的结构和性质
专题:有机物的化学性质及推断
分析:有机物含有碳碳双键,可发生加成、加聚和氧化反应,含有酯基,可发生水解反应,含有羟基,可发生取代、消去和氧化反应,以此解答该题.
解答:
解:A.含有碳碳双键,可发生加成反应,故A正确;
B.含有酯基、羟基,可发生取代反应,故B正确;
C.分子中不含有羧基,与乙醇不发生酯化反应,故C错误;
D.含有碳碳双键,可与溴水发生加成反应,可与酸性高锰酸钾发生氧化还原反应,故D正确.
故选C.
B.含有酯基、羟基,可发生取代反应,故B正确;
C.分子中不含有羧基,与乙醇不发生酯化反应,故C错误;
D.含有碳碳双键,可与溴水发生加成反应,可与酸性高锰酸钾发生氧化还原反应,故D正确.
故选C.
点评:本题考查有机物的结构与性质,为高频考点,把握官能团与性质的关系为解答的关键,侧重烯烃、酯、醇性质的考查,注意把握有机物的结构特点,题目难度不大.

练习册系列答案
相关题目
在同温同压下,下列各组热化学方程式中,△H1<△H2的是( )
| A、2H2 (g)+O2(g)=2H2O(g)△H1 2H2(g)+O2 (g)=2H2O(l)△H2 | ||||
| B、S(s)+O2(g)=SO2 (g)△H1 S(g)+O2(g)=SO2 (g)△H2 | ||||
C、CO(g)+
| ||||
D、H2 (g)+Cl2 (g)=2HCl(g)△H1
|
如图曲线a和b是盐酸与氢氧化钠溶液的相互滴定的滴定曲线,下列叙述不正确的是( )


| A、NaOH溶液的物质的量浓度为0.1mol/L |
| B、P点时反应恰好完全中和,溶液pH为7 |
| C、曲线a是NaOH人滴定盐酸的滴定曲线 |
| D、P点时溶液中的离子浓度为c(Na+)=c(Cl-)=c(H+)=c(OH-) |
已知元素A的原子最外层电子数为a.次外层电子数为b,元素B的原子M层电子数为(a-b),L层电子数为(a+b),则下列说法中不正确的是( )
| A、元素B位于元素周期表中第三周期ⅣA族 |
| B、在元素A所在的主族元素的最简单氢化物中,A的氢化物最稳定 |
| C、元素A与元素B形成的化合物在工业上可用作制玻璃的原料 |
| D、元素A与元素B形成的化合物遇任何酸都不能反应 |
镭是元素周期表中第七周期的ⅡA族元素.下面关于镭的性质的描述中不正确的是( )
| A、价层电子构型为7S2 |
| B、单质能与冷水反应,放出氢气 |
| C、氢氧化物呈两性 |
| D、碳酸盐难溶于水 |
溶液、浊液、胶体的本质区别是( )
| A、透明程度 | B、分散质颗粒大小 |
| C、稳定性 | D、丁达尔现象 |
下列叙述正确的是( )
| A、SO2能使溴水、酸性高锰酸钾溶液退色是因为SO2有漂白性 |
| B、若将SO2和Cl2以等物质的量混合后通入品红溶液中一定退色更快 |
| C、SO2通入Ba(OH)2溶液中,有白色沉淀生成,加入稀硝酸最终沉淀全部溶解 |
| D、SO2通入BaCl2溶液中无沉淀生成 |
镁燃料电池以镁合金作为电极的一极,另一极充入过氧化氢,电解质是酸化的氯化钠溶液,放电时总反应为:Mg+2H++H2O2=Mg2++2H2O,关于该电池的说法不正确的是( )
| A、镁合金为电源负极,发生氧化反应 |
| B、电解质溶液中的H+向正极移动 |
| C、正极反应为:H2O2+2e-=2OH- |
| D、放电时正极周围溶液的pH升高 |