题目内容
17.下列变化中的离子方程式书写正确的是( )| A. | 向氯化铝溶液中滴加过量的氨水:4NH3•H2O+Al3+═AlO2-+4NH4++2H2O | |
| B. | NH4Al(SO4)2溶液中滴加少量NaOH溶液:Al3++NH4++4OH-=Al(OH)3↓+NH3•H2O | |
| C. | 向明矾溶液中加入过量的Ba(OH)2溶液:Al3++2SO42-+2Ba2++4OH-=2BaSO4↓+AlO2-+2H2O | |
| D. | 向NaAlO2溶液中通入足量CO2:2AlO2-+CO2+3H2O=2Al(OH)3↓+CO32- |
分析 A.氨水为弱碱,二者反应生成氢氧化铝沉淀;
B.氢氧化钠少量,铝离子优先参与反应,铵根离子不反应;
C.氢氧化钡过量,铝离子和硫酸根离子完全反应;
D.二氧化碳足量,反应生成碳酸氢根离子.
解答 解:A.氯化铝溶液与过量氨水反应生成氢氧化铝沉淀,正确的离子方程式为:Al3++3NH3•H2O=Al(OH)3↓+3NH4+,故A错误;
B.NH4Al(SO4)2溶液中滴加少量NaOH溶液,只有铝离子反应,正确的离子方程式为:Al3++3OH-=Al(OH)3↓,故B错误;
C.明矾溶液中加入过量的Ba(OH)2溶液,反应生成硫酸钡、偏铝酸钾和水,反应的离子方程式为:Al3++2SO42-+2Ba2++4OH-=2BaSO4↓+AlO2-+2H2O,故C正确;
D.NaAlO2溶液中通入足量CO2,反应生成氢氧化铝沉淀和碳酸氢钠,正确的离子方程式为:AlO2-+CO2+2H2O=Al(OH)3↓+HCO3-,故D错误;
故选C.
点评 本题考查了离子方程式的书写判断,为高考的高频题,题目难度中等,注意掌握离子方程式的书写原则,明确离子方程式正误判断常用方法:检查反应物、生成物是否正确,检查各物质拆分是否正确,如难溶物、弱电解质等需要保留化学式,检查是否符合原化学方程式等.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
8.下列说法正确的是( )
| A. | 13C和 14N 质子数相差 1,中子数也相差1 | |
| B. | 一种元素可以有多种核素,有几种核素就有几种原子 | |
| C. | 钴5627Co、5727Co、5827Co、5927Co等几种原子,他们是同素异形体,其物理性质几乎相同,化学性质不同 | |
| D. | 核聚变如21H+31H→42He+10 n,由于有新微粒生成,该变化是化学变化 |
5.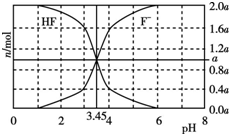 25℃时,用2a mol•L-1NaOH溶液滴定1.0L2a mol•L-1HF溶液,得到混合液中HF、F-的物质的量与溶液pH的变化关系如图所示.下列说法正确的是( )
25℃时,用2a mol•L-1NaOH溶液滴定1.0L2a mol•L-1HF溶液,得到混合液中HF、F-的物质的量与溶液pH的变化关系如图所示.下列说法正确的是( )
 25℃时,用2a mol•L-1NaOH溶液滴定1.0L2a mol•L-1HF溶液,得到混合液中HF、F-的物质的量与溶液pH的变化关系如图所示.下列说法正确的是( )
25℃时,用2a mol•L-1NaOH溶液滴定1.0L2a mol•L-1HF溶液,得到混合液中HF、F-的物质的量与溶液pH的变化关系如图所示.下列说法正确的是( )| A. | pH=3时,溶液中:c(Na+)<c(F-) | |
| B. | 当c(F-)>c(HF)时,一定有c(OH-)>c(H+) | |
| C. | pH=3.45时,NaOH溶液与HF恰好完全反应 | |
| D. | pH=4时,溶液中:c(HF)+c(Na+)+c(H+)-c(OH-)<2a mol•L-1 |
6.下列物质的除杂方式:①SO2中混有的SO3杂质可以让混合气体通过稀硫酸除去;②MnO2中混有的少量有机物,可以用加热的方法除去;③CO2中混有的SO2气体可以通过饱和NaHSO3溶液除去;④金属铜中含有的少量银和锌可以通过电解精炼的方式除去;⑤KNO3中含有的少量NaCl可以通过重结晶的方法除去,其中合理的是( )
| A. | ①②④⑤ | B. | 全部 | C. | ②④⑤ | D. | ②③④⑤ |
7.警察常从案发现场的人体气味来获取有用线索,人体气味的成分中含有以下化合物:①辛酸;②壬酸;③环十二醇;④5,9一十一烷酸内酯;⑤十八烷;⑥己醛;⑦庚醛.下列说法正确的是( )
| A. | ①、②、⑥分子中碳原子数小于10,③、④、⑤、⑦分子中碳原子数大于10 | |
| B. | ①、②是无机物,③、⑤、⑦是有机物 | |
| C. | ①、②是酸性化合物,③、⑤不是酸性化合物 | |
| D. | ②、③、④含氧元素,⑤、⑥、⑦不含氧元素 |
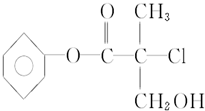 某有机物X是农药生产中的一种中间体,其结构简式如图:
某有机物X是农药生产中的一种中间体,其结构简式如图: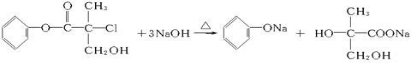 +NaCl+H2O.
+NaCl+H2O.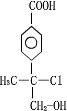 .
.
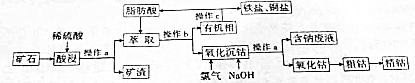
 A、B、C、D均为中学化学常见的纯净物,A是单质.它们之间有如下的反应关系:
A、B、C、D均为中学化学常见的纯净物,A是单质.它们之间有如下的反应关系: