题目内容
7.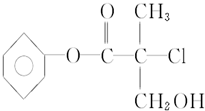 某有机物X是农药生产中的一种中间体,其结构简式如图:
某有机物X是农药生产中的一种中间体,其结构简式如图:(1)X的分子式为C10H11O3Cl.
(2)X分子中所含官能团有酯基、羟基和氯原子(填名称).
(3)X可能发生多种反应,下列有关X发生化学反应的叙述中正确的是ABD.
A.在氢氧化钠醇溶液中共热能发生消去反应
B.在铜作催化剂时加热,可被氧气氧化生成能发生银镜反应的物质
C.在浓硫酸存在时加热可发生消去反应
D.在铁作催化剂时,可跟液溴发生取代反应
(4)写出X跟氢氧化钠稀溶液共热时所发生反应的化学方程式
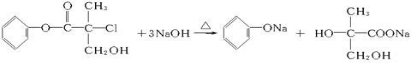 +NaCl+H2O.
+NaCl+H2O.(5)X可能有多种同分异构体,写出符合下列条件的一种同分异构体的结构简式:
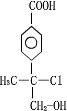 .
.①苯环只有分子处在对位的两个取代基.
②遇氯化铁溶液不变色,但能与NaHCO3溶液反应放出气体.
分析 (1)根据有机物结构简式判断含有的元素种类和原子个数,可确定有机物分子式;
(2)根据结构简式判断官能团种类;
(3)根据含有的官能团判断有机物可能具有的性质;
(4)分子中含有酯基和氯原子,都可与氢氧化钠反应;
(5)遇氯化铁溶液不变色,但遇pH试纸显红色,说明不含酚羟基,但含有羧基.
解答 解:(1)由结构简式可知有机物的分子式为C10H11O3Cl,故答案为:C10H11O3Cl;
(2)由结构简式可知含有的官能团有酯基、羟基和氯原子,故答案为:酯基、羟基和氯原子;
(3)A.分子中含有氯原子,且邻位碳原子上有氢原子,可在氢氧化钠的醇溶液中发生消去反应,故A正确;
B.分子中含有羟基,可被氧化物醛基,故B正确;
C.由于羟基邻位碳原子没有氢原子,可不能发生消去反应,故C错误;
D.该物质在铁作催化剂时,可跟液溴发生取代反应,故D正确.
故答案为:ABD;
(4)与足量NaOH溶液反应为: +NaCl+H2O,
+NaCl+H2O,
故答案为: +NaCl+H2O;
+NaCl+H2O;
(5)遇氯化铁溶液不变色,但遇pH试纸显红色,说明不含酚羟基,但含有羧基,可能的结构为 ,故答案为:
,故答案为: .
.
点评 该题是高考中的常见题型,属于中等难度的试题.试题基础性强,侧重考查学生分析问题、解决问题的能力.该题的关键是准确判断出分子中含有的官能团,然后在根据相应官能团的结构和性质,灵活分析、判断即可.该题有利于培养学生严谨的逻辑思维能力和发散思维能力.

练习册系列答案
 轻巧夺冠周测月考直通中考系列答案
轻巧夺冠周测月考直通中考系列答案
相关题目
17.用下列实验装置进行的实验中,能达到相应实验目的是( )
| A. | 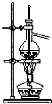 海水蒸馏 | B. | 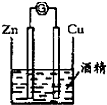 形成原电池 | C. | 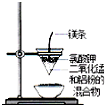 可制得金属锰 | D. | 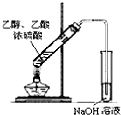 制取乙酸乙酯 |
18.已知:①1molH2分子中化学键断裂时需要吸收436kJ的能量
②1molCl2分子中化学键断裂时需要吸收243kJ的能量
③由H原子和Cl原子形成1molHCl分子时释放431kJ的能量.
下列叙述正确的是( )
②1molCl2分子中化学键断裂时需要吸收243kJ的能量
③由H原子和Cl原子形成1molHCl分子时释放431kJ的能量.
下列叙述正确的是( )
| A. | 氢气与氯气反应生成2mol氯化氢气体,需要释放183kJ的热量 | |
| B. | 氢气与氯气反应生成2mol氯化氢气体,需要吸收183kJ的热量 | |
| C. | 氢气与氯气反应生成1mol氯化氢气体,需要吸收183kJ的热量 | |
| D. | 氢气与氯气反应生成1mol氯化氢气体,需要释放183kJ的热量 |
2.用0.1000mol•L-1的盐酸溶液滴定未知浓度的NaOH溶液时,下列操作正确的是( )
| A. | 装碱液的锥形瓶用NaOH溶液润洗 | |
| B. | 滴定时,眼睛注视酸式滴定管中液面的下降情况 | |
| C. | 应用右手控制酸式滴定管的活塞 | |
| D. | 若用甲基橙作指示剂,到滴定终点时锥形瓶内液体为橙色 |
16.含有3.01×1023个氧原子的H2SO4的物质的量是( )
| A. | 0.500 mol | B. | 1.00 mol | C. | 0.125mol | D. | 0.25 mol |
17.下列变化中的离子方程式书写正确的是( )
| A. | 向氯化铝溶液中滴加过量的氨水:4NH3•H2O+Al3+═AlO2-+4NH4++2H2O | |
| B. | NH4Al(SO4)2溶液中滴加少量NaOH溶液:Al3++NH4++4OH-=Al(OH)3↓+NH3•H2O | |
| C. | 向明矾溶液中加入过量的Ba(OH)2溶液:Al3++2SO42-+2Ba2++4OH-=2BaSO4↓+AlO2-+2H2O | |
| D. | 向NaAlO2溶液中通入足量CO2:2AlO2-+CO2+3H2O=2Al(OH)3↓+CO32- |
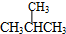 和
和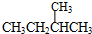 ;
;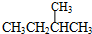 和
和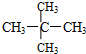 ;
;