题目内容
将Mg、Cu组成的混合物mg投入适量的HNO3溶液中,固体完全溶解时收集到的还原产物NO0.896L(标准状况),向反应后溶液加入2mol/L的NaOH溶液60mL时金属恰好沉淀完全.则形成的沉淀质量为( )
| A、(m+2.28)g |
| B、(m+2.04)g |
| C、(m+3.32)g |
| D、(m+4.34)g |
考点:有关混合物反应的计算
专题:计算题
分析:硝酸被还原为NO气体且标准状况下体积为0.896L,即物质的量为0.04mol,根据氮元素的化合价变化计算转移电子物质的量;最后沉淀为Cu(OH)2、Mg(OH)2,金属提供的电子的物质的量等于氢氧根离子的物质的量,故最后得出沉淀质量等于金属的质量加氢氧根离子的质量.
解答:
解:硝酸被还原为NO气体且标准状况下体积为0.896L,即物质的量为:
=0.04mol,转移的电子的物质的量为:0.04mol×(5-2)=0.12mol,
最后沉淀为Cu(OH)2、Mg(OH)2,金属提供的电子的物质的量等于氢氧根离子的物质的量,
故最后沉淀质量为:mg+0.12mol×17g/mol=(m+2.04)g,
故选B.
| 0.896L |
| 22.4L/mol |
最后沉淀为Cu(OH)2、Mg(OH)2,金属提供的电子的物质的量等于氢氧根离子的物质的量,
故最后沉淀质量为:mg+0.12mol×17g/mol=(m+2.04)g,
故选B.
点评:本题考查混合物的计算,题目难度中等,解题关键是判断沉淀质量为金属与金属离子结合氢氧根离子的质量之和,注意巧解巧算在化学计算中的应用方法.

练习册系列答案
 激活思维优加课堂系列答案
激活思维优加课堂系列答案 活力试卷系列答案
活力试卷系列答案 课课优能力培优100分系列答案
课课优能力培优100分系列答案
相关题目
下列说法不正确的是( )
| A、催化剂可以缩短可逆反应达到平衡的时间,但是不能改变化学平衡状态 |
| B、如果改变影响平衡的一个条件,平衡就会朝着减弱这种改变的方向移动 |
| C、对于合成氨工业,在合成氨的反应中,温度越高,越有利于氨的合成 |
| D、化学平衡常数、平衡转化率均可用于说明化学反应的限度 |
已知G、Q、X、Y、Z均为含氯元素的化合物,在一定条件下有下列转化关系(未配平):这五种化合物中Cl元素化合价由低到高的顺序是( )
①G-→Q+NaCl
②Q+H2O
X+H2
③Y+NaOH-→G+Q+H2O
④Z+NaOH-→Q+X+H2O.
①G-→Q+NaCl
②Q+H2O
| 电解 |
③Y+NaOH-→G+Q+H2O
④Z+NaOH-→Q+X+H2O.
| A、G、Y、Q、Z、X |
| B、X、Z、Q、G、Y |
| C、X、Z、Q、Y、G |
| D、G、Q、Y、Z、X |
已知:A(g)+D(g)═C(g)△H1:B(g)+D(g)═E(g)△H2:若A、B混合气体lmol完全与D反应,放出热△H3,则A、B的物质的量之比是( )
| A、(△H2-△H3):(△H1-△H3) |
| B、(△H3-△H2):(△H1-△H3) |
| C、(△H3-△H2):(△H3-△H1) |
| D、(△H1-△H2):(△H3-△H2) |
下列两种气体的分子数一定相等的是( )
| A、质量相等、密度不等的N2和C2H4 |
| B、等体积等密度的CO和C2H4 |
| C、等温等体积的O3和N2 |
| D、等压等体积的N2和CO2 |
分别用一定量等量的铁与足量的稀硫酸及足量的CuO制备单质铜,有人设计了以下两种方案:
①Fe
H2
Cu,②CuO
CuSO4
Cu.对制备得到Cu的量,下列判断正确的( )
①Fe
| H2SO4 |
| CuO |
| H2SO4 |
| Fe |
| A、一样多 | B、①多 |
| C、②多 | D、无法判断 |
下列叙述正确的是( )
| A、乙烯和苯都能够使溴水褪色,褪色的原因相同 |
| B、淀粉、油脂、蛋白质都能够发生水解,且都能生成二种产物 |
| C、煤油可由石油分馏获得,可用作燃料和保存少量金属 |
| D、乙醇、乙酸、乙酸乙酯都能发生取代反应,乙酸乙酯中的少量乙酸可用Na OH溶液除去 |
实验室制备下列物质时,所用装置或方法正确的是( )
A、用SiO2和NaOH焙烧制备硅酸钠,可采用的图装置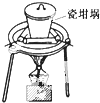 |
| B、制氧气时,用Na2O2或H2O2作反应物可选择相同的气体发生装置 |
| C、制氯气时,用饱和NaHCO3溶液和浓硫酸净化气体 |
| D、制二氧化氮时,用水或NaOH溶液吸收尾气 |