题目内容
分别用一定量等量的铁与足量的稀硫酸及足量的CuO制备单质铜,有人设计了以下两种方案:
①Fe
H2
Cu,②CuO
CuSO4
Cu.对制备得到Cu的量,下列判断正确的( )
①Fe
| H2SO4 |
| CuO |
| H2SO4 |
| Fe |
| A、一样多 | B、①多 |
| C、②多 | D、无法判断 |
考点:铜金属及其重要化合物的主要性质,铁的化学性质
专题:元素及其化合物
分析:两方案中所发生的化学方程式为:①Fe+H2SO4═FeSO4+H2↑、H2+CuO
Cu+H2O;
②CuO+H2SO4═CuSO4+H2O、Fe+CuSO4═Cu+FeSO4;
②中均可完全转化,而①中氢气还原CuO,应先通入氢气排出装置中的空气,不能全部参与还原反应.
| ||
②CuO+H2SO4═CuSO4+H2O、Fe+CuSO4═Cu+FeSO4;
②中均可完全转化,而①中氢气还原CuO,应先通入氢气排出装置中的空气,不能全部参与还原反应.
解答:
解:两方案中所发生的化学方程式为:①Fe+H2SO4═FeSO4+H2↑、H2+CuO
Cu+H2O;
②CuO+H2SO4═CuSO4+H2O、Fe+CuSO4═Cu+FeSO4;
②中均可完全转化,而方案①中氢气还原氧化铜实验,开始时需先通入一部分氢气,排除装置中的空气,实验结束时还要通一会氢气,以防止生成的铜被氧化,如果不考虑先通后停,相同质量的铁生成铜的质量是相同的,但是由于部分氢气被浪费,从而导致铁的质量被多消耗一部分,所以导致方案①对应的铜减少.故方案②生成的铜多,
故选C.
| ||
②CuO+H2SO4═CuSO4+H2O、Fe+CuSO4═Cu+FeSO4;
②中均可完全转化,而方案①中氢气还原氧化铜实验,开始时需先通入一部分氢气,排除装置中的空气,实验结束时还要通一会氢气,以防止生成的铜被氧化,如果不考虑先通后停,相同质量的铁生成铜的质量是相同的,但是由于部分氢气被浪费,从而导致铁的质量被多消耗一部分,所以导致方案①对应的铜减少.故方案②生成的铜多,
故选C.
点评:本题考查制备物质方案,为高频考点,侧重于学生的分析能力的考查,把握制备中发生的反应、分析方案的差别为解答的关键,注意氢气还原氧化铜的实际操作即可解答,侧重分析与实验能力的考查,难度不大.

练习册系列答案
相关题目
已二酸中含有两个羧基(-COOH),分子式为C6H10O4,则已二酸可能的结构有(不考虑立体异构)( )
| A、7种 | B、8种 | C、9种 | D、10种 |
下列混合物的分离方法不正确的是( )
| A、易溶与难溶固体混合物用溶解过滤方法提纯 |
| B、沸点不同的互溶液体可用蒸馏分离 |
| C、用酒精可以从碘水中萃取碘 |
| D、汽油和水的混合物可以用分液漏斗分离 |
将Mg、Cu组成的混合物mg投入适量的HNO3溶液中,固体完全溶解时收集到的还原产物NO0.896L(标准状况),向反应后溶液加入2mol/L的NaOH溶液60mL时金属恰好沉淀完全.则形成的沉淀质量为( )
| A、(m+2.28)g |
| B、(m+2.04)g |
| C、(m+3.32)g |
| D、(m+4.34)g |
已知:在100℃时,纯水的c(H+)为1×10-6mol?L-1,此时将pH=12的NaOH溶液V1 L与pH=l的H2SO4溶液V2 L混合,若所得混合溶液的pH=10,则V1:V2为( )
| A、1:9 | B、10:1 |
| C、9:1 | D、1:10 |
下列说法正确的是( )
| A、增大压强任何反应的反应速率都一定增大 |
B、已知H2CO3的电离常数分别为Ka1=4.3×10-7、Ka2=5.61×10-11,苯酚的电离常数Ka=1.1×10-10.苯酚钠溶液中通入少量CO2时的化学方程式为: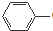 ONa+CO2+H2O→ ONa+CO2+H2O→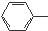 OH+NaHCO3 OH+NaHCO3 |
| C、pH=2的盐酸和pH=4的硫酸溶液等体积混合后溶液的pH=3 |
| D、在滴有酚酞的氢氧化钠溶液中逐滴滴入盐酸至红色恰好消失,此时溶液的pH=7 |
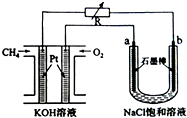 新型高效的甲烷燃料电池采用铂为电极材料,两电极上分别通入CH4和O2,电解质为KOH溶液.某研究小组用甲烷燃料电池作为电源,进行饱和氯化钠溶液电解实验,如图所示:
新型高效的甲烷燃料电池采用铂为电极材料,两电极上分别通入CH4和O2,电解质为KOH溶液.某研究小组用甲烷燃料电池作为电源,进行饱和氯化钠溶液电解实验,如图所示: