题目内容
18. 氨是重要的化工原料,用途很广.
氨是重要的化工原料,用途很广.(1)合成氨工厂常用醋酸二氨合铜(由[Cu(NH3)2]+和CH3COO-构成)溶液吸收对氨合成催化剂有毒害的CO气体.
①醋酸二氨合铜所含的元素中,第一电离能最大的是氮(填元素名称).
②醋酸二氨合铜所含元素组成的单质,所属的晶体类型有b、c、d(填标号).
a.离子晶体 b.分子晶体c.原子晶体 d.金属晶体
③第4周期元素中,基态原子与基态Cu原子具有相同未成对电子数的有4种(不含Cu).
(2)BF3气体与NH3相遇立即生成一种白色晶体:BF3+NH3=F3B-NH3.
①BF3和NH3分子的空间构型分别为正三角形、三角锥型.
②晶体F3B-NH3中,B原子的杂化轨道类型为sp3.
(3)NH3可用于合成尿素、硫酸铵等氮肥.某化肥厂从生产的硫酸铵中检出一种组成为N4H4(SO4)2的物质.该物质易溶于水,在水溶液中以SO42-和N4H44+两种正四面体构型的离子存在.N4H44+遇碱生成一种形似白磷的N4分子.
①下列相关说法中,正确的是b(填序号).
a.N4是N2的同分异构体
b.1mol N4 分解生成N2,形成了4mol π键
c.白磷的沸点比N4高,原因是P-P键键能比N-N键大
d.白磷的化学性质比N2活泼,说明P的非金属性比N强
②画出N4H44+的结构(标明其中的配位键):
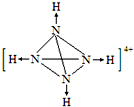 .
.
分析 (1)①非金属性越强,第一电离能越大,但是最外层电子排布处于全满或半满状态时较稳定,不易失电子,第一电离能较大;
②醋酸二氨合铜所含元素组成的单质,有铜、金刚石、氧气、氢气等;
③Cu的外围电子排布为3d104s1,只有1个未成对电子;
(2)根据分子中中心原子的价层电子对数判断杂化类型和分子的空间构型;
(3)①a.分子式相同结构不同的化合物互称同分异构体;
b.一个N2中含有2个 π键;
c.结构相似的分子晶体,相对分子量越大,熔沸点越高;
d.同主族从上到下,非金属性减弱;
②N4H44+中每个N原子与另外3个N原子形成共价键,同时与1个氢离子形成配位键.
解答 解:(1)①非金属性越强,第一电离能越大,但是最外层电子排布处于全满或半满状态时较稳定,不易失电子,第一电离能较大,醋酸二氨合铜所含的元素有Cu、O、C、H、N,由于N原子的最外层排布为半满状态,第一电离能较大,所以第一电离能最大的是N;
故答案为:氮;
②醋酸二氨合铜所含元素组成的单质,有铜属于金属晶体、金刚石属于原子晶体、氧气和氢气属于分子晶体;
故答案为:b、c、d;
③Cu的外围电子排布为3d104s1,只有1个未成对电子,第4周期元素中,基态原子含有一个未成对电子的元素有,K、Sc、GaBr,共有4种元素;
故答案为:4;
(2)①BF3中B的价层电子对数为3+$\frac{3-3×1}{2}$=3,没有孤电子对,分子的空间构型为正三角形,NH3分子中N原子的价层电子对数为3+$\frac{5-3×1}{2}$=4,含有一个孤电子对,空间构型为三角锥型;
故答案为:正三角形;三角锥型;
②晶体F3B-NH3中,B原子的价层电子对数为4,则杂化类型为sp3杂化;
故答案为:sp3;
(3)①a.分子式相同结构不同的化合物互称同分异构体,N4与N2都是N元素的单质,属于同素异形体,故a错误;
b.一个N2中含有2个 π键,1mol N4 分解生成2molN2,形成了4mol π键,故b正确;
c.结构相似的分子晶体,相对分子量越大,熔沸点越高,白磷的相对分子量比N4大,与键能无关,故c错误;
d.同主族从上到下,非金属性减弱,则P的非金属性比N弱,白磷的化学性质比N2活泼,与共价键稳定性有关,故d错误;
故答案为:b;
②N4H44+中每个N原子与另外3个N原子形成共价键,同时与1个氢离子形成配位键,则N4H44+的结构图为 ;
;
故答案为: .
.
点评 本题考查了晶体类型和第一电离能、杂化方式的判断、电子排布式的书写、电负性、微粒的空间结构、配位键等;考查的知识点较多,题目难度中等,注意对题中所给结构图的分析是解题的关键.

 阅读快车系列答案
阅读快车系列答案| A. | 加热氯化铁溶液,溶液颜色变深与盐类水解有关 | |
| B. | NaHS溶液水解方程式为:HS-+H2O?H2S+OH- | |
| C. | Na2SO3溶液中,c(OH-)=c(H+)+c(HSO3-)+c(H2SO3) | |
| D. | 0.1 mol•L-1的CH3COOH溶液和0.1 mol•L-1的CH3COONa溶液等体积混合:c(CH3COO-)+c(CH3COOH)=2c(Na+) |
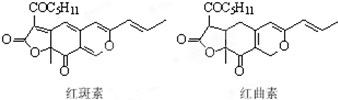 着色剂为使食品着色的物质,可增加对食品的嗜好及刺激食欲.红斑素、红曲素是常用于糖果、雪糕等食品的着色剂的主要成分,结构如图所示.下列说法正确的是( )
着色剂为使食品着色的物质,可增加对食品的嗜好及刺激食欲.红斑素、红曲素是常用于糖果、雪糕等食品的着色剂的主要成分,结构如图所示.下列说法正确的是( )| A. | 红斑素和红曲素互为同分异构体 | |
| B. | 一定条件下红斑素和红曲素都能发生加聚和缩聚反应 | |
| C. | 红斑素中含有醚键、羰基、酯键这三种含氧官能团 | |
| D. | 1 mol红曲素最多能与6 mol H2发生加成反应 |
| A. | 加热使c(H+)增大 | B. | 投入一小块金属钠 | ||
| C. | 加入少量NH4Cl固体 | D. | 以铁为电极进行电解 |
| A. | 钢制品应接电源的正极 | |
| B. | 电镀时铝作阳极,阳极反应式为Al-3e-+7AlCl4-=4Al2Cl7- | |
| C. | 电解液中H+移向阴极,OH-移向阳极 | |
| D. | 每生成1mol铝,电解液中转移3mol电子 |
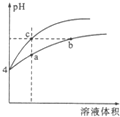 某温度下,体积和pH都相同的盐酸和氯化铵溶液加水稀释时的pH变化曲线如图所示,下列判断不正确的是( )
某温度下,体积和pH都相同的盐酸和氯化铵溶液加水稀释时的pH变化曲线如图所示,下列判断不正确的是( )| A. | a、b、c三点溶液的Kw相同 | |
| B. | b点溶液中c(H+)+c(NH3•H2O)=c(OH-) | |
| C. | 用等浓度的NaOH溶液和等体积b、c处溶液反应,消耗NaOH溶液的体积Vb>Vc | |
| D. | a、b、c三点溶液中水的电离程度a>b>c |
| A. | 生成的铜的物质的量是0.2mol | B. | 随着电解进行溶液的pH减小 | ||
| C. | 转移电子的物质的量为0.4mol | D. | 阳极反应是2H2O-4e-=4H++O2↑ |
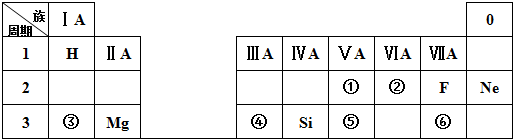
 元素周期表的形式多种多样,下图是扇形元素周期表的一部分(1~36号元素),对比中学常见元素周期表思考扇形元素周期表的填充规律,下列说法正确的是( )
元素周期表的形式多种多样,下图是扇形元素周期表的一部分(1~36号元素),对比中学常见元素周期表思考扇形元素周期表的填充规律,下列说法正确的是( )| A. | ②、⑧、⑨对应的简单离子半径依次增大 | |
| B. | ⑥的氯化物的熔点比⑦的氯化物熔点高 | |
| C. | 元素⑩处于常见周期表第四周期第VIIIB族 | |
| D. | ①分别与③、④、⑤均可形成既含极性键又含非极性键的非极性分子 |
 .
.