题目内容
14.能使湿润的淀粉KI试纸变蓝的是( )①氯水 ②溴水 ③碘水 ④氯化钠 ⑤溴化钾.
| A. | ①② | B. | ①②③ | C. | ①②④ | D. | ①③⑤ |
分析 能使湿润的淀粉-碘化钾试纸变蓝,则选项中的物质应具有氧化性,且氧化性大于碘或存在碘单质,以此来解答.
解答 解:①氯水与KI反应生成碘,能使湿润的淀粉-碘化钾试纸变蓝,故正确;
②溴水与KI反应生成碘,能使湿润的淀粉-碘化钾试纸变蓝,故正确;
③碘水含有碘,可使淀粉变蓝色,故正确;
④氯化钠与KI不反应,无碘单质生成,所以不能使湿润的淀粉碘化钾试纸变蓝,故错误;
⑤溴化钾不能氧化碘离子生成碘单质,所以不能使湿润的淀粉碘化钾试纸变蓝,故错误;
故选B.
点评 本题考查碘的特征反应及氧化还原反应,为高频考点,明确氧化性的强弱及碘遇淀粉变蓝是解答本题的关键,难度不大,注意相关基础知识的积累.

练习册系列答案
 小天才课时作业系列答案
小天才课时作业系列答案 一课四练系列答案
一课四练系列答案 黄冈小状元满分冲刺微测验系列答案
黄冈小状元满分冲刺微测验系列答案 新辅教导学系列答案
新辅教导学系列答案 阳光同学一线名师全优好卷系列答案
阳光同学一线名师全优好卷系列答案
相关题目
5.明代《天工开物》记载“火法”冶炼锌:“炉甘石十斤,装载入一泥罐内,…然后逐层用煤炭饼垫盛,其底铺薪,发火煅红,…冷淀,毁罐取出,…,即倭铅也”(注:炉甘石的主要成分为碳酸锌,泥罐中掺有煤炭).下列说法不正确的是( )
| A. | 倭铅是指金属锌和铅的混合物 | B. | 煤炭中起作用的主要成分是C | ||
| C. | 我国历史上铅的使用早于锌 | D. | 该冶炼锌的方法属于热还原法 |
2.设NA代表阿伏加德罗常数,下列说法正确的是( )
| A. | 室温下,32gO2和O3的混合气体中含有的氧原子数为2NA | |
| B. | 在常温常压下,11.2LN2含有的分子数为0.5NA | |
| C. | 0.5 mol•L-1MgCl2溶液中,含有Cl-个数为NA | |
| D. | 18 g NH4+中所含的电子数为11NA |
6.下列事实中一定能证明HClO是弱电解质的是( )
(1)pH相等的H2SO4和HClO与足量的强碱反应,HClO消耗的强碱体积大
(2)用HClO溶液做导电性实验,灯泡很暗
(3)NaClO溶液中有HClO分子存在
(4)HClO溶液有很强的氧化性
(5)等体积,等物质的量浓度的HClO与NaOH溶液恰好完全反应
(6)盐酸与KClO溶液反应生成HClO
(7)1mol/L的HClO溶液能使紫色石蕊试液先变红后褪色.
(1)pH相等的H2SO4和HClO与足量的强碱反应,HClO消耗的强碱体积大
(2)用HClO溶液做导电性实验,灯泡很暗
(3)NaClO溶液中有HClO分子存在
(4)HClO溶液有很强的氧化性
(5)等体积,等物质的量浓度的HClO与NaOH溶液恰好完全反应
(6)盐酸与KClO溶液反应生成HClO
(7)1mol/L的HClO溶液能使紫色石蕊试液先变红后褪色.
| A. | (1)(2)(3) | B. | (1)(3)(6) | C. | (1)(2)(5)(6) | D. | (1)(3)(6)(7) |
16.已知汽车尾气无害化处理反应为2NO(g)+2CO(g)?N2(g)+2CO2(g).下列说法正确的是( )
| A. | 升高温度可使该反应的逆反应速率降低 | |
| B. | 反应达到平衡后,NO的反应速率保持恒定 | |
| C. | 使用高效催化剂只能提高正反应速率 | |
| D. | 单位时间内消耗CO和CO2的物质的量相等时,反应达到平衡 |
17.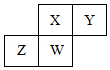 短周期元素X、Y、Z、W在元素周期表中的相对位置如图所示,其中W原子的质子数是其最外层电子数的三倍,下列说法不正确的是( )
短周期元素X、Y、Z、W在元素周期表中的相对位置如图所示,其中W原子的质子数是其最外层电子数的三倍,下列说法不正确的是( )
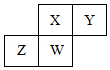 短周期元素X、Y、Z、W在元素周期表中的相对位置如图所示,其中W原子的质子数是其最外层电子数的三倍,下列说法不正确的是( )
短周期元素X、Y、Z、W在元素周期表中的相对位置如图所示,其中W原子的质子数是其最外层电子数的三倍,下列说法不正确的是( )| A. | 最简单气态氢化物的热稳定性:Y>X>W>Z | |
| B. | 最高价氧化物对应的水化物的酸性:X>W>Z | |
| C. | 原子半径:W>Z>Y>X | |
| D. | 元素X、Z、W的最高正价分别与其主族序数相等 |
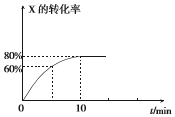 恒定温度为T1℃时,在容积为10L的密闭容器中充人1.0mol X和0.80mol Y,发生反应:
恒定温度为T1℃时,在容积为10L的密闭容器中充人1.0mol X和0.80mol Y,发生反应: