题目内容
5.明代《天工开物》记载“火法”冶炼锌:“炉甘石十斤,装载入一泥罐内,…然后逐层用煤炭饼垫盛,其底铺薪,发火煅红,…冷淀,毁罐取出,…,即倭铅也”(注:炉甘石的主要成分为碳酸锌,泥罐中掺有煤炭).下列说法不正确的是( )| A. | 倭铅是指金属锌和铅的混合物 | B. | 煤炭中起作用的主要成分是C | ||
| C. | 我国历史上铅的使用早于锌 | D. | 该冶炼锌的方法属于热还原法 |
分析 依据题意可知:碳酸锌与碳在高温下反应生成锌和一氧化碳,化学方程式:ZnCO3+2C$\frac{\underline{\;高温\;}}{\;}$Zn+3CO↑,得到的锌为倭铅,据此解答.
解答 解:A.由题意可知,倭铅是指金属锌,不是混合物,故A错误;
B.反应中C作还原剂,则煤炭中起作用的主要成分是C,故B正确;
C.我国古代术士的炼金术就用到铅,所以历史上铅的使用早于锌,故C正确;
D.依据方程式可知ZnCO3+2C$\frac{\underline{\;高温\;}}{\;}$Zn+3CO↑,该反应是利用碳还原碳酸锌生成锌单质,属于热还原法,故D正确;
故选:A.
点评 本题考查了金属冶炼的一般原理,把握题干所给信息,熟悉相关物质的性质是解题关键,题目难度不大,侧重于考查学生的分析能力.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
16.设NA为阿伏加德罗常数的数值,下列叙述正确的是( )
| A. | 1 mol/L氯化铜溶液中的Cu2+数小于NA | |
| B. | 标准状况下,22.4 L Cl2与水反应转移的电子数为NA | |
| C. | 28 g聚乙烯含有的碳原子数为2NA | |
| D. | 惰性电极电解食盐水,若线路中通过1NA电子电量,则阳极产生气体11.2L |
20.对于反应3Br2+6NaOH═5NaBr+NaBrO3+3H2O,以下叙述正确的是( )
| A. | Br2是氧化剂,NaOH是还原剂 | |
| B. | Br2既是氧化剂又是还原剂 | |
| C. | 被氧化的Br原子和被还原的Br原子的物质的量的比为5:1 | |
| D. | 每生成1mol的NaBrO3转移10mol的电子 |
10.下列物质属于非电解质的是( )
| A. | NH4Cl | B. | Al | C. | AlCl3 | D. | NH3 |
17.25℃时,在等体积的下列溶液中,发生电离的水的物质的量之比是( )
①0.5mol•L-1的H2SO4溶液,②0.05mol•L-1的Ba(OH)2溶液,③1mol•L-1的NaCl溶液,④纯水.
①0.5mol•L-1的H2SO4溶液,②0.05mol•L-1的Ba(OH)2溶液,③1mol•L-1的NaCl溶液,④纯水.
| A. | 107:107:1:1 | B. | 1:10:107:107 | C. | 107:106:2:2 | D. | 107:106:2×107:2 |
14.能使湿润的淀粉KI试纸变蓝的是( )
①氯水 ②溴水 ③碘水 ④氯化钠 ⑤溴化钾.
①氯水 ②溴水 ③碘水 ④氯化钠 ⑤溴化钾.
| A. | ①② | B. | ①②③ | C. | ①②④ | D. | ①③⑤ |
8.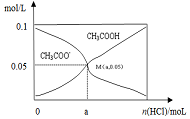 常温下向10mL 0.1mol•L-1CH3COONa溶液中,不断通入HCl后,CH3COO-与CH3COOH浓度的变化趋势如图所示(不考虑溶液体积变化),下列说法不正确的是( )
常温下向10mL 0.1mol•L-1CH3COONa溶液中,不断通入HCl后,CH3COO-与CH3COOH浓度的变化趋势如图所示(不考虑溶液体积变化),下列说法不正确的是( )
 常温下向10mL 0.1mol•L-1CH3COONa溶液中,不断通入HCl后,CH3COO-与CH3COOH浓度的变化趋势如图所示(不考虑溶液体积变化),下列说法不正确的是( )
常温下向10mL 0.1mol•L-1CH3COONa溶液中,不断通入HCl后,CH3COO-与CH3COOH浓度的变化趋势如图所示(不考虑溶液体积变化),下列说法不正确的是( )| A. | M点溶液中水的电离程度比原溶液小 | |
| B. | 在M点时,c(H+)-c(OH-)=(100a-5.0×10-2) mol/L | |
| C. | 随着HCl的通入,$\frac{c(O{H}^{-})}{c(C{H}_{2}CO{O}^{-})}$值不断减小 | |
| D. | 当n(HCl)=1.0×10-3mol时,溶液中c(Na+)>c(Cl-)>c(CHCOO-)>c(H+)>c(OH-) |