题目内容
11.(1)单质硫酸能被氧化,又能被还原,请写出一个体现单质硫的还原性的化学方程式:S+O2$\frac{\underline{\;点燃\;}}{\;}$SO2.(2)黑火药爆炸时,发生的反应之一:S+2KNO3+3C$\stackrel{引燃}{→}$K2S+3CO2↑+N2↑,该反应中1mol S能氧化0.5mol C;
(3)N2的电子式是
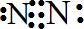 ;将空气中的氮气转化为氮的化合物的过程称为固氮,下列能实现人工固氮的是D
;将空气中的氮气转化为氮的化合物的过程称为固氮,下列能实现人工固氮的是DA.闪电B.电解饱和食盐水车间
C.根瘤菌D.合成氮车间
(4)某无色混和气体中可能含有NH3、O2、H2、NO、HCl等气体,将它通过浓H2SO4后发现气体体积减少,将剩余气体在空气接触后,气体呈红棕色,此混合气中一定不含有O2、HCl.
分析 (1)体现硫的还原性,则S元素的化合价升高;
(2)在反应2KNO3+3C+S=K2S+N2↑+3CO2↑中,N元素的化合价由+5降低为0,S元素的化合价由0降低为-2价,则KNO3和S作氧化剂,C由0价升高为+4价,做还原剂,根据反应可知,该反应中1mol S能氧化,得到2mol的电子,而1molC失去4mol的电子,根据得失电子守恒分析解答;
(3)氮气中有三个共价键,即氮原子间形成三对共用电子对;根据氮气转化为氮的化合物的过程称为固氮选出人工固氮;
(4)与浓硫酸反应的气体是氨气,空气中呈红棕色的气体是一氧化氮,能够与氨气、一氧化氮反应的不能存在;
解答 解:(1)体现硫的还原性,则S元素的化合价升高,如S+O2$\frac{\underline{\;点燃\;}}{\;}$SO2,故答案为:S+O2$\frac{\underline{\;点燃\;}}{\;}$SO2;
(2)在反应2KNO3+3C+S=K2S+N2↑+3CO2↑中,N元素的化合价由+5降低为0,S元素的化合价由0降低为-2价,则KNO3和S作氧化剂,C由0价升高为+4价,做还原剂,根据反应可知,该反应中1mol S能氧化,得到2mol的电子,而1molC失去4mol的电子,所以该反应中1mol S能氧化0.5mol C,
故答案为:0.5;
(3)氮原子间形成三对共用电子对,电子式为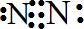 ,A.闪电,不是人工固氮;B.电解饱和食盐水车间,不是固氮;C.根瘤,属于生物固氮;D.合成氨车间,属于人工固氮,属所以D正确,
,A.闪电,不是人工固氮;B.电解饱和食盐水车间,不是固氮;C.根瘤,属于生物固氮;D.合成氨车间,属于人工固氮,属所以D正确,
故答案为: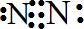 ; D;
; D;
(2)将它通过浓H2SO4后发现气体体积减少,说明一定含有氨气,所以一定没有氯化氢;将剩余气体在空气接触后,气体呈红棕色,说明一定含有一氧化氮气体,所以一定没有氧气,
故答案为:O2、HCl.
点评 本题考查了氨气的制取及性质,涉及的题量较大,充分考查了学生对氧化还原反应的知识掌握熟练程度,本题难度中等.

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案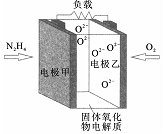 如图所示是一种以液态肼(N2H4)为燃料,氧气为氧化剂,某固体氧化物为电解质的新型燃料电池,该固体氧化物电解质在700-900℃温度时,O2-可在该固体氧化物电解质中自由移动,电池反应生成均为无毒无害的物质,下列说法正确的是( )
如图所示是一种以液态肼(N2H4)为燃料,氧气为氧化剂,某固体氧化物为电解质的新型燃料电池,该固体氧化物电解质在700-900℃温度时,O2-可在该固体氧化物电解质中自由移动,电池反应生成均为无毒无害的物质,下列说法正确的是( )| A. | 电池内的由O2-电极乙移向电极甲 | |
| B. | 电池的总反应为:N2H4+2O2═2NO+2H2O | |
| C. | 当甲电极上有1molN2H4消耗时,乙电极上有1molO2被氧化 | |
| D. | 电池外电路的电子由电极乙移向电极甲 |
| A. | 核外电子排布为1s22s22p43s2的原子处于激发态 | |
| B. | 某元素质量数51,中子数28,其基态原子中未成对电子数为1 | |
| C. | 若某基态原子的外围电子排布为4d15s2,该元素原子核外有5个电子层 | |
| D. | BF3中B原子sp2杂化,为平面三角形 |
| A. | 可能存在核外电子排布式为1s22s22p63s23p64s24p1的原子 | |
| B. | 当电子排布在同一能级的不同轨道时,总是优先单独占据一个轨道,而且自旋方向相反 | |
| C. | 次氯酸的电子式:H?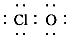 | |
| D. | 基态原子的电子获得一定能量变为激发态原子,而激发态原子变为基态原子,则要放出能量 |
| A. | 氧化铁与硝酸反应 | B. | 氢氧化铜与硝酸反应 | ||
| C. | 木炭粉与浓硝酸反应 | D. | 铜与硝酸反应 |
| A. | 11.2L氧气所含的原子数为NA | |
| B. | 2.3g金属钠变为钠离子得到0.1NA电子 | |
| C. | 0.5mol/LH2SO4中的H+数为NA | |
| D. | 常温常压下32g O2与O3的混合物含有的氧原子数为2NA |
| A. | 10mL1mol/LNa2SO4溶液 | B. | 50mL0.2mol/LNaCl溶液 | ||
| C. | 10mL0.2mol/LNa2SO4溶溶液 | D. | 200mL0.1mol/LNaNO3溶液 |
| A. | α粒子散射实验 | B. | 铀盐晶体实验 | C. | X-射线管实验 | D. | 14C放射性实验 |
| 选项 | 待提纯的物质 | 选用的试剂 | 操作方法 |
| A | NaOH(Na2CO3) | 盐酸 | - |
| B | CO2(CO) | 氧气 | 加热 |
| C | Cu(Fe) | CuSO4溶液 | 过滤 |
| D | NaCl(Na2SO4) | BaCl2溶液 | 分液 |
| A. | A | B. | B | C. | C | D. | D |