题目内容
含铬废水主要含Cr2O72-,目前处理方法有沉淀法、铁氧体法、电解法等.一种改进的铁氧体法(GT-铁氧体法)原理是:在废水中加入Fe3+,然后将含Fe3+的部分废水通过装有铁屑的反应塔充分反应后,再与其余原废水在强酸性混合反应池中混合足够长时间后,在常温下加碱,数分钟后即生成黑棕色的铁氧体.GT-铁氧体法除铬的部分化学反应方程式如下:
Fe2++2Fe3++8OH-→FeO.Fe2O3+4H2O;
FeO.Fe2O3+Cr3+→Fe3+{Fe2+.Fe3+1-x.Cr3+x}O4,0<x≤1(未配平).
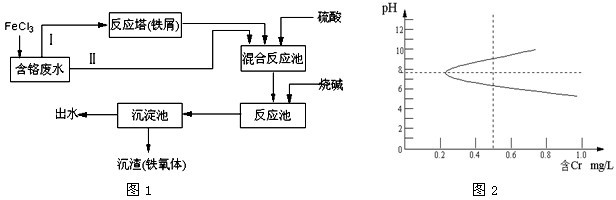
GT-铁氧体法流程如图1所示.
试回答下列问题
(1)上述流程中Cr2O72-与Fe2+只在强酸性的“混合反应池”中反应,其离子方程式为: .
(2)形成铁氧体的关键是要保证混合反应池中加碱前Fe3+与Fe2+的比值为2:1,这样出水质量和反应生成的铁氧体沉淀效果都较好.经检测某次实验选用的废水中Cr2O72-的浓度为cmol/L,加入一定量FeCl3后,使溶液中铁与铬的物质的量之比为20:1,则GT-铁氧体法中进入还原塔(铁屑)的废水约为总废水量的 (选填序号).
a.5%~10% b.10%~20% c. 25%~40%
(3)GT-铁氧体法中开始时要检测废水中Cr2O72-的浓度,其目的是: .
(4)铁氧体形成条件中溶液的pH值也很重要,废液中铬残留量与pH的关系如图2所示.如果pH值控制不当,形成的铁氧体结构就不紧密,这样处理液达不到国家排放标准(铬残留量小于0.5mg/L),你认为沉淀池中pH控制最好为: .
(5)处理含铬的酸性废水也可用电解法:先在废水中加入一定量的食盐,然后用石墨和铁电极电解,最终形成沉淀法除去.电解时阳极的电极反应式为: .
Fe2++2Fe3++8OH-→FeO.Fe2O3+4H2O;
FeO.Fe2O3+Cr3+→Fe3+{Fe2+.Fe3+1-x.Cr3+x}O4,0<x≤1(未配平).
GT-铁氧体法流程如图1所示.

试回答下列问题
(1)上述流程中Cr2O72-与Fe2+只在强酸性的“混合反应池”中反应,其离子方程式为:
(2)形成铁氧体的关键是要保证混合反应池中加碱前Fe3+与Fe2+的比值为2:1,这样出水质量和反应生成的铁氧体沉淀效果都较好.经检测某次实验选用的废水中Cr2O72-的浓度为cmol/L,加入一定量FeCl3后,使溶液中铁与铬的物质的量之比为20:1,则GT-铁氧体法中进入还原塔(铁屑)的废水约为总废水量的
a.5%~10% b.10%~20% c. 25%~40%
(3)GT-铁氧体法中开始时要检测废水中Cr2O72-的浓度,其目的是:
(4)铁氧体形成条件中溶液的pH值也很重要,废液中铬残留量与pH的关系如图2所示.如果pH值控制不当,形成的铁氧体结构就不紧密,这样处理液达不到国家排放标准(铬残留量小于0.5mg/L),你认为沉淀池中pH控制最好为:
(5)处理含铬的酸性废水也可用电解法:先在废水中加入一定量的食盐,然后用石墨和铁电极电解,最终形成沉淀法除去.电解时阳极的电极反应式为:
考点:物质分离和提纯的方法和基本操作综合应用,制备实验方案的设计
专题:实验设计题
分析:(1)Fe2+具有还原性,可与Cr2O72-+发生氧化还原反应生成Fe3+和Cr3+;
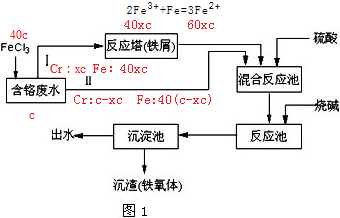
(2)设废水中含Cr2O72-为cmol,进入还原塔(铁屑)的废水约为总废水量为x,则进入反应塔的Cr2O72-为xc,未进入的Cr2O72-为c-xc,铁与铬的物质的量之比为20:1,所以氯化铁的物质的量为40c,进入反应塔的氯化铁为40xc,未进入的为40(c-xc),
在反应塔中发生反应:Fe+2Fe3+=3Fe2+
40xc 60xc
6Fe2+~Cr2O72-~6Fe3+
6c c 6c
保证反应池中加碱前Fe3+与Fe2+的比值为2:1计算x,关系较复杂,如图所示:
 ;
;
(3)从(2)可看出,要保证最佳处理效果,需确定加入FeCl3的量及进入还原塔的废水与总废水量的比值;
(4)根据废液中铬残留量与pH的关系如图2进行判断;
(5)用Fe做电极进行电解,阳极发生Fe-2e-=Fe2+,生成的亚铁离子与Cr2O72-发生氧化还原反应被还原为Cr3+然后生成Cr(OH)3沉淀除去,以此来解答.
(2)设废水中含Cr2O72-为cmol,进入还原塔(铁屑)的废水约为总废水量为x,则进入反应塔的Cr2O72-为xc,未进入的Cr2O72-为c-xc,铁与铬的物质的量之比为20:1,所以氯化铁的物质的量为40c,进入反应塔的氯化铁为40xc,未进入的为40(c-xc),
在反应塔中发生反应:Fe+2Fe3+=3Fe2+
40xc 60xc
6Fe2+~Cr2O72-~6Fe3+
6c c 6c
保证反应池中加碱前Fe3+与Fe2+的比值为2:1计算x,关系较复杂,如图所示:
 ;
;(3)从(2)可看出,要保证最佳处理效果,需确定加入FeCl3的量及进入还原塔的废水与总废水量的比值;
(4)根据废液中铬残留量与pH的关系如图2进行判断;
(5)用Fe做电极进行电解,阳极发生Fe-2e-=Fe2+,生成的亚铁离子与Cr2O72-发生氧化还原反应被还原为Cr3+然后生成Cr(OH)3沉淀除去,以此来解答.
解答:
解:(1)Fe2+具有还原性,可与Cr2O72-+发生氧化还原反应生成Fe3+和Cr3+,
反应的离子方程式为6Fe2++Cr2O72-+14H+=6Fe3++2Cr3++7H2O,
故答案为:6Fe2++Cr2O72-+14H+=6Fe3++2Cr3++7H2O;
(2)设废水中含Cr2O72-为cmol,进入还原塔(铁屑)的废水约为总废水量为x,则进入反应塔的Cr2O72-为xc,未进入的Cr2O72-为c-xc,铁与铬的物质的量之比为20:1,所以氯化铁的物质的量为40c,进入反应塔的氯化铁为40xc,未进入的为40(c-xc),
在反应塔中发生反应:Fe+2Fe3+=3Fe2+
40xc 60xc
6Fe2+~Cr2O72-~6Fe3+
6c c 6c
保证反应池中加碱前Fe3+与Fe2+的比值为2:1,得出
=
x=0.375;故选c;
(3)从(2)可看出,要保证最佳处理效果,需确定加入FeCl3的量及进入还原塔的废水与总废水量的比值;
故答案为:确定加入FeCl3的量,及进入还原塔的废水与总废水量的比值;
(4)根据废液中铬残留量与pH的关系如图2进行可知,铬残量在pH大于8,随pH增大而增大,小于7,随pH减小而增大,在7-8之间最小;
故答案为:7.7;
(5)Fe为阳极,则阳极反应为Fe-2e-=Fe2+,溶液中氢离子在阴极放电生成氢气,则阴极反应为2H++2e-=H2 ↑,生成的亚铁离子与Cr2O72-发生氧化还原反应被还原为Cr3+,故答案为:Fe-2e-=Fe2+.
反应的离子方程式为6Fe2++Cr2O72-+14H+=6Fe3++2Cr3++7H2O,
故答案为:6Fe2++Cr2O72-+14H+=6Fe3++2Cr3++7H2O;
(2)设废水中含Cr2O72-为cmol,进入还原塔(铁屑)的废水约为总废水量为x,则进入反应塔的Cr2O72-为xc,未进入的Cr2O72-为c-xc,铁与铬的物质的量之比为20:1,所以氯化铁的物质的量为40c,进入反应塔的氯化铁为40xc,未进入的为40(c-xc),
在反应塔中发生反应:Fe+2Fe3+=3Fe2+
40xc 60xc
6Fe2+~Cr2O72-~6Fe3+
6c c 6c
保证反应池中加碱前Fe3+与Fe2+的比值为2:1,得出
| 40(c-xc)+6c |
| 60xc-6c |
| 2 |
| 1 |
(3)从(2)可看出,要保证最佳处理效果,需确定加入FeCl3的量及进入还原塔的废水与总废水量的比值;
故答案为:确定加入FeCl3的量,及进入还原塔的废水与总废水量的比值;
(4)根据废液中铬残留量与pH的关系如图2进行可知,铬残量在pH大于8,随pH增大而增大,小于7,随pH减小而增大,在7-8之间最小;
故答案为:7.7;
(5)Fe为阳极,则阳极反应为Fe-2e-=Fe2+,溶液中氢离子在阴极放电生成氢气,则阴极反应为2H++2e-=H2 ↑,生成的亚铁离子与Cr2O72-发生氧化还原反应被还原为Cr3+,故答案为:Fe-2e-=Fe2+.
点评:本题考查了废水的净化,难度较大.对于(2)问,要明确反应原理及各量之间的关系,是解题的关键,要充分利用题给数据解题.本题中所给铬氧体生成的反应方程式较复杂,与解题无关,不要纠缠于是否配平及如何确定铬的大小,易进入解题误区.

练习册系列答案
相关题目
下列叙述正确的是( )
| A、氯气、SO2都具有氧化性,故而可用于漂白纸浆等 |
| B、常温下浓硫酸能与铝发生钝化,可在常温下用铝制容器贮运浓硫酸 |
| C、H2CO3是弱酸,所以NaHCO3是弱电解质 |
| D、较强的酸可以制取较弱的酸,次氯酸溶液无法制取盐酸 |
下列属于电解质并能导电的物是( )
①熔融的NaCl ②KNO3溶液 ③Cu ④酒精 ⑤NaCl晶体 ⑥盐酸.
①熔融的NaCl ②KNO3溶液 ③Cu ④酒精 ⑤NaCl晶体 ⑥盐酸.
| A、① | B、①②③⑤⑥ |
| C、①②⑥ | D、①③④⑤ |

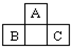 如图为短周期一部分.A、C两元素原子核外分别有两个、一个未成对电子.试回答:
如图为短周期一部分.A、C两元素原子核外分别有两个、一个未成对电子.试回答: