题目内容
7.某无色溶液中可能存在的离子有Na+、NH4+、HCO3-、Cl-、SO32-、SO42-.现取该溶液进行有关实验,实验结果如图所示: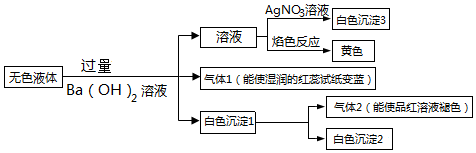
下列说法不正确的是( )
| A. | 气体2一定是SO2 | B. | 白色沉淀2一定是BaSO4 | ||
| C. | 白色沉淀1的成分只有2种可能 | D. | 溶液中只有HCO3-无法确定 |
分析 由实验流程可知,无色溶液与Ba(OH)2反应生成的白色沉淀1转化为沉淀2,且生成能使品红褪色的气体,可知沉淀1含BaSO4、BaSO3,沉淀2为BaSO4,气体2为SO2,与碱反应生成的气体1为NH3,可知原溶液中一定含NH4+、SO32-、SO42-,则不含HCO3-;
与过量Ba(OH)2反应后分离出的溶液的焰色反应为黄色,可知原溶液中含Na+,过量的碱与硝酸银可反应生成白色沉淀,则不能确定是否含Cl-,以此来解答.
解答 解:A.由上述分析可知,气体2一定是SO2,能使品红褪色,故A正确;
B.白色沉淀1与酸反应后得到沉淀2,则白色沉淀2一定是BaSO4,故B正确;
C.白色沉淀1的成分只有2种可能,为BaSO4、BaSO3或BaSO3,为BaSO3时酸为浓硫酸,故C正确;
D.气体2为二氧化硫,可知溶液中不含HCO3-,故D错误;
故选D.
点评 本题考查无机物的推断,为高频考点,把握离子之间的反应、物质的性质、相互转化为解答的关键,侧重分析与推断能力的考查,注意元素化合物知识的应用,题目难度不大.

练习册系列答案
 星级口算天天练系列答案
星级口算天天练系列答案 芒果教辅达标测试卷系列答案
芒果教辅达标测试卷系列答案
相关题目
5.已知A、B、C、D、E是短周期中原子序数依次增大的五种主族元素,其中A是组成有机物的必要元素,元素B的原子最外层电子数是其电子层数的3倍,元素D与A为同族元素,元素C与E形成的化合物CE是厨房常用调味品.下列说法正确的是( )
| A. | 原子半径:C>D>B>A | |
| B. | C与B形成的两种化合物均属于离子化合物,且化学键类型完全相同 | |
| C. | 最简单气态氢化物的稳定性:B>A | |
| D. | A、D、E的最高价氧化物对应水化物的酸性逐渐增强 |
19.某混合物的水溶液中可能含有以下离子中的若干种:Na+、Al3+、Fe3+、Mg2+、Ba2+、NH4+、Cl-、SO42-,现分别取100mL的两份溶液进行如下实验.
①第一份加过量NaOH溶液后加热,收集到0.01mol气体,无沉淀生成,同时得到溶液甲.
②向甲溶液中通入过量CO2,生成白色沉淀,沉淀经过滤、洗涤、灼烧后,得到1.02g固体.
③第二份加足量BaCl2溶液后,生成白色沉淀,过滤后的沉淀经足量盐酸洗涤、干燥后,得到11.65g固体,向滤液中加入AgNO3溶液又有白色沉淀产生.下列有关叙述正确的是( )
①第一份加过量NaOH溶液后加热,收集到0.01mol气体,无沉淀生成,同时得到溶液甲.
②向甲溶液中通入过量CO2,生成白色沉淀,沉淀经过滤、洗涤、灼烧后,得到1.02g固体.
③第二份加足量BaCl2溶液后,生成白色沉淀,过滤后的沉淀经足量盐酸洗涤、干燥后,得到11.65g固体,向滤液中加入AgNO3溶液又有白色沉淀产生.下列有关叙述正确的是( )
| A. | 由①可知原溶液存在离子为NH4+,其浓度为0.01mol/L | |
| B. | 原溶液一定存在Cl- | |
| C. | 原溶液肯定没有Fe3+、Mg2+,一定含有Na+ | |
| D. | n(NH4+):n(Al3+):n(SO42-)=1:1:5 |
17.元素周期表是学习化学的重要工具,它隐含着许多信息和规律.根据下表中短周期元素的原子半径和主要化合价,回答表后的问题.
(1)上述元素中与元素⑧处于同一周期的有Mg、P、Cl(填元素符号)
(2)元素①在元素周期表中的位置是第二周期ⅥA族
(3)①④⑦三种元素的氢化物的稳定性由强到弱的顺序为H2O>NH3>PH3(填化学式)
(4)请写出下列元素形成的常见化合物的电子式:
③⑤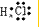 ②⑤
②⑤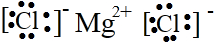 ③⑦
③⑦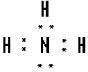
(5)请写出⑤⑧两种元素的最高价氧化物对应水化物间反应的离子方程式:3H++Al(OH)3═Al3++3H2O.
| ① | ② | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | |
| 原子半径(10-10m) | 0.74 | 1.60 | 0.53 | 1.10 | 0.99 | 1.11 | 0.75 | 1.43 |
| 最高或最低化合价 | +2 | +1 | +5 | +7 | +2 | +5 | +3 | |
| -2 | -3 | -1 | -3 |
(2)元素①在元素周期表中的位置是第二周期ⅥA族
(3)①④⑦三种元素的氢化物的稳定性由强到弱的顺序为H2O>NH3>PH3(填化学式)
(4)请写出下列元素形成的常见化合物的电子式:
③⑤
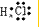 ②⑤
②⑤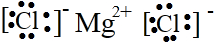 ③⑦
③⑦
(5)请写出⑤⑧两种元素的最高价氧化物对应水化物间反应的离子方程式:3H++Al(OH)3═Al3++3H2O.

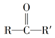 (R、R′为烃基)结构的分子
(R、R′为烃基)结构的分子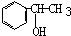 ;
;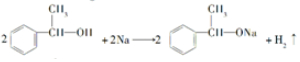 ;
;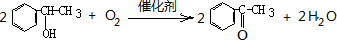 .
.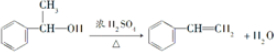 .脱水后的产物,发生聚合反应的化学方程式
.脱水后的产物,发生聚合反应的化学方程式 .
.