题目内容
15.下列反应属于吸热反应的是( )| A. | 能量变化如图所示的反应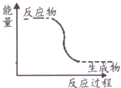 | |
| B. | 中和反应 | |
| C. | 化学键断裂吸收的热量比化学键生成放出的热量少的反应 | |
| D. | Ba(OH)2•8H2O晶体和NH4Cl晶体反应 |
分析 吸热反应是反应物的总能量小于生成物的总能量的反应,是化学键断裂时吸收的能量大于化学键形成时放出能量的反应.
根据常见的放热反应有:所有的物质燃烧、所有金属与酸反应、金属与水反应,所有中和反应;绝大多数化合反应和铝热反应;
常见的吸热反应有:绝大数分解反应,个别的化合反应(如C和CO2),一氧化碳、碳、氢气还原金属氧化物以及某些复分解(如铵盐和强碱).
解答 解:A、吸热反应是反应物的总能量小于生成物的总能量的反应,当反应物的总能量大于生成物的总能量时,反应放热,故A错误;
B、所有的中和反应均为放热反应,故B错误;
C、化学键断裂时.吸收的能量大于化学键形成时放出能量的反应为吸热反应,当化学键断裂吸收的能量小于化学键形成时放出的能量时,反应放热,故C错误;
D、Ba(OH)2•8H2O和NH4Cl的反应是典型的吸热反应,故D正确.
故选D.
点评 本题考查吸热反应,抓住中学化学中常见的吸热或放热的反应是解题的关键,对于特殊过程中的热量变化的要熟练记忆来解答此类习题

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
5.X、Y、Z、M、W为原子序数依次增大的5种短周期元素.X的质子总数与电子层数相同,Y、Z、M同周期且相邻,W原子核外电子数是M原子最外层电子数的2倍.Z与其同主族的短周期元素可形成常见气体甲.X、Y、Z 三种元素形成化合物乙.下列说法不正确的是( )
| A. | 气体甲可与Z的某种氢化物反应生成强酸 | |
| B. | W元素的晶体单质是一种良好的半导体材料 | |
| C. | 化合物乙中一定只有共价键 | |
| D. | X分别与Y、Z、M、W形成的常见化合物中,稳定性最好的是XM |
6.关于化学反应CaCO3$\frac{\underline{\;高温\;}}{\;}$CaO+CO2↑的下列说法中,正确的是( )
| A. | 属于放热反应 | B. | 属于氧化还原反应 | ||
| C. | 由热能转化为化学能 | D. | 可用于工业生产熟石灰 |
3.甲烷分子中的四个氢原子都被苯基取代,可得到的分子如图所示,对该分子的下列叙述中不正确的是( )
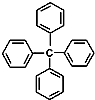

| A. | 分子式为C25H20 | |
| B. | 此物质的一氯代物有3种 | |
| C. | 此物质属芳香烃 | |
| D. | 此分子中所有原子可能处于同一平面上 |
10.下列有关化学用语表示正确的是( )
| A. | 硫原子的结构示意图: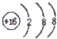 | B. | Na2S的电子式:Na+: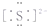 | ||
| C. | HCl的结构式:H-Cl | D. | CH4分子的球模型: |
20.以下说法正确的是( )
| A. | C70与金刚石一样属于原子晶体 | |
| B. | 共价化合物中一定不含离子键 | |
| C. | I2升华破坏了共价键 | |
| D. | HCl溶于水能电离子出H+、Cl-,所以HCl是离子化合物 |
4.化学与人类生活、生产和社会可持续发展密切相关,下列说法正确的是( )
| A. | 为测定熔融氢氧化钠的导电性,可将氫氧化钠固体放在石英坩埚中加热熔化 | |
| B. | 采取“静电除尘”、“燃煤固硫”、“汽车尾气催化净化”等方法,可提高空气质量 | |
| C. | 铝及其合金是电气、工业、家庭广泛使用的材料,是因为铝的冶炼方法比较简单 | |
| D. | 半导体行业中有一句话:“从沙滩到用户”,计箅机芯片的材料是经提纯的二氧化硅 |
5.现有8种元素的性质、数据如下表所列,它们属于第二或第三周期.
回答下列问题:
(1)③的元素符号是Li;⑧的元素名称是硼;①在元素周期表中的位置是第二周期第VIA族;
(2)比较④和⑦的氢化物的稳定性(用化学式表示)NH3>PH3
(3)用电子式表示②和⑤组成的化合物的形成过程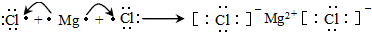 ;
;
(4)写出⑦的最高价氧化物对应的水化物与它的氢化物发生反应的化学方程式NH3+HNO3=NH4NO3
(5)写出②的最高价氧化物对应的水化物跟⑤的氢化物水溶液发生反应的离子方程式Mg(OH)2+2H+=Mg2++2H2O;
(6)“神舟”十号载人飞船内需要一种化合物来吸收航天员呼出的CO2,你认为该物质应该由上表中的①⑥元素组成(填表中编号),用化学方程式表示吸收原理2Na2O2+2CO2=2Na2CO3+O2.
| 编号 元素性质 | ① | ② | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ |
| 原子半径(10-10m) | 0.74 | 1.60 | 1.52 | 1.10 | 0.99 | 1.86 | 0.75 | 0.82 |
| 最高或最低化合价 | +2 | +1 | +5 | +7 | +1 | +5 | +3 | |
| -2 | -3 | -1 | -3 |
(1)③的元素符号是Li;⑧的元素名称是硼;①在元素周期表中的位置是第二周期第VIA族;
(2)比较④和⑦的氢化物的稳定性(用化学式表示)NH3>PH3
(3)用电子式表示②和⑤组成的化合物的形成过程
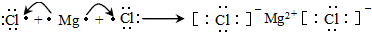 ;
;(4)写出⑦的最高价氧化物对应的水化物与它的氢化物发生反应的化学方程式NH3+HNO3=NH4NO3
(5)写出②的最高价氧化物对应的水化物跟⑤的氢化物水溶液发生反应的离子方程式Mg(OH)2+2H+=Mg2++2H2O;
(6)“神舟”十号载人飞船内需要一种化合物来吸收航天员呼出的CO2,你认为该物质应该由上表中的①⑥元素组成(填表中编号),用化学方程式表示吸收原理2Na2O2+2CO2=2Na2CO3+O2.