题目内容
氯气是一种 色的气体,该气体与铁反应的化学方程式为 .在标准状况下,将氯气与铜化合,若反应用去35.5g氯气,则消耗铜的物质的量是 ,将生成物溶于水,配成500mL溶液,则该溶液CuCl2物质的量浓度是 .将此溶液取出20mL加水配制成200mL溶液,则稀释后溶液中Cl-物质的量浓度是 .写出向该溶液中滴加AgNO3溶液时的反应方程式 .
考点:氯气的化学性质,氯气的物理性质
专题:卤族元素
分析:氯气是一种黄绿色的气体,氯气具有强氧化性能铁氧化为三价铁.根据n=
计算氯气的物质的量,再根据V=nVm计算氯气体积;根据方程式Cu+Cl2
CuCl2计算需要铜的物质的量、生成CuCl2的物质的量,根据c=
计算CuCl2的物质的量浓度,根据稀释定律c1V1=c2V2计算稀释后Cl-的物质的量浓度,盐酸与AgNO3溶液反应生成AgCl沉淀与HNO3,据此书写方程式.
| m |
| M |
| ||
| n |
| V |
解答:
解:氯气是一种黄绿色的气体,氯气能将金属氧化为最高价,铁在氯气中燃烧的产物是氯化铁,反应为:2Fe+3Cl2
2FeCl3,
35.5g氯气的物质的量=
=0.5mol,
与氢气化合生成HCl,由方程式Cu+Cl2
CuCl2,可知n(Cu)=n(Cl2)=0.5mol,生成n(CuCl2)=n(Cl2)=0.5mol,
将CuCl2溶于水,配成500mL溶液,所得溶液的物质的量浓度=
=1mol/L,此溶液取出20mL加水配制成200mL溶液,根据稀释定律可知,稀释后Cl-物质的量浓度物质的量浓度=
=0.2mol/L,
向CuCl2溶液中滴加AgNO3溶液,反应方程式为:2AgNO3+CuCl2=2AgCl↓+Cu(NO3)2,
故答案为:黄绿;2Fe+3Cl2
2FeCl3;0.5mol;1mol/L;0.2mol/L;2AgNO3+CuCl2=2AgCl↓+Cu(NO3)2.
| ||
35.5g氯气的物质的量=
| 35.5g |
| 71g/mol |
与氢气化合生成HCl,由方程式Cu+Cl2
| ||
将CuCl2溶于水,配成500mL溶液,所得溶液的物质的量浓度=
| 0.5mol |
| 0.5L |
| 0.02L×2×1mol/L |
| 0.2L |
向CuCl2溶液中滴加AgNO3溶液,反应方程式为:2AgNO3+CuCl2=2AgCl↓+Cu(NO3)2,
故答案为:黄绿;2Fe+3Cl2
| ||
点评:本题考查了化学方程式的书写,题目难度不大,注意掌握反应原理和化学方程式的书写方法,该题是高考中的高频题,侧重对学生能力的培养和训练.

练习册系列答案
 课课优能力培优100分系列答案
课课优能力培优100分系列答案 优百分课时互动系列答案
优百分课时互动系列答案
相关题目
下列各有机物的系统命名正确的是( )
| A、CH2=CH-CH=CH2 1,3-二丁烯 |
| B、CH3CH2OOCCOOCH2CH3 乙二酸二乙酯 |
| C、CH3CH2CH(OH)CH3 3-丁醇 |
| D、CH3CH(CH2CH3)CH3 2-乙基丙烷 |
将5.4g铝分别放入100ml 2mol/L硫酸(甲)和100ml 2mol/L氢氧化钠溶液(乙)中,相同条件下生成的气体的体积( )
| A、甲多 | B、乙多 |
| C、一样多 | D、无法判断 |
电解质不仅在工农业生产中占有重要地位,而且在各种生命活动中也起着重要作用,则下列有关电解质的叙述正确的是( )
| A、化合物都是电解质 |
| B、电解质一定是化合物 |
| C、SO3溶于水形成的溶液能导电,所以SO3是电解质 |
| D、NaCl固体不导电,所以NaCl不是电解质 |
关于如图所示装置的叙述,正确的是( )
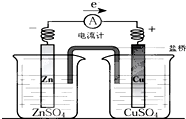

| A、铜是阳极,铜片上有气泡产生 |
| B、正极附近的SO42-离子浓度逐渐增大 |
| C、电流从锌片经导线流向铜片 |
| D、铜离子在铜片表面被还原 |
某固体化合物M不导电,但熔化或溶于水中能完全电离,下列关于M的说法中,正确的是( )
| A、M为非电解质 |
| B、M是强电解质 |
| C、M为一种盐 |
| D、M是弱电解质 |
下列说法正确的是( )
| A、只有反应体系中所有分子同时都发生有效碰撞的反应才是放热反应 |
| B、通常条件下能够自发进行的反应必须具备△H和△S均大于0 |
| C、任何化学反应只要是自发进行的放热反应都可以设计成原电池,为外界提供电能 |
| D、实验室通常将固态氯化铁溶解在盐酸中,再稀释到相应浓度来配置氯化铁溶液 |

 ,回答下列问题:
,回答下列问题: