题目内容
12.硝酸在反应中的动态变化:在浓硝酸中放入铜片,回答下列问题:(1)反应开始时的化学方程式为Cu+4HNO3(浓)=Cu(NO3)2+2NO2↑+2H2O,实验现象为溶液逐渐变蓝色,有红棕色气体逸出.
(2)若铜有剩余,则临近结束时的反应方程式为3Cu+8HNO3=3Cu(NO3)2+2NO↑+4H2O
(3)待反应停止后,再加入少量25%的稀硫酸,现象为铜片溶解,有气泡生成原因是加入稀硫酸后,氢离子与原溶液中硝酸根离子构成强氧化性酸,又能与过量的铜反应.
分析 (1)铜和浓硝酸反应生成硝酸铜、二氧化氮和水,二氧化氮是红棕色气体,铜盐溶液呈蓝色;
(2)铜有剩余,铜和稀硝酸反应生成硝酸铜和NO;
(3)酸性条件下,硝酸根离子具有强氧化性,又继续和铜反应.
解答 解:(1)铜和浓硝酸反应生成硝酸铜、二氧化氮和水,反应方程式为Cu+4HNO3(浓)=Cu(NO3)2+2NO2↑+2H2O,二氧化氮是红棕色气体,铜盐溶液呈蓝色,所以看到的现象是:溶液逐渐变蓝色,有红棕色气体逸出,故答案为:Cu+4HNO3(浓)=Cu(NO3)2+2NO2↑+2H2O;溶液逐渐变蓝色,有红棕色气体逸出;
(2)铜有剩余,随着反应的进行,硝酸浓度逐渐减小,当变为稀硝酸时,铜和稀硝酸反应生成硝酸铜和NO,反应方程式为3Cu+8HNO3=3Cu(NO3)2+2NO↑+4H2O,
故答案为:3Cu+8HNO3=3Cu(NO3)2+2NO↑+4H2O;
(3)加入稀硫酸后,氢离子原溶液中硝酸根离子构成强氧化性酸,又能与过量的铜反应,发生的反应为3Cu+8HNO3=3Cu(NO3)2+2NO↑+4H2O,可观察到铜片溶解,并有气泡生成,
故答案为:铜片溶解,有气泡生成;加入稀硫酸后,氢离子与原溶液中硝酸根离子构成强氧化性酸,又能与过量的铜反应.
点评 本题考查了硝酸的性质,为高频考点,硝酸的浓度不同导致其氧化性不同,和铜反应时其产物不同,酸性条件下硝酸根离子具有强氧化性,题目难度不大.

练习册系列答案
 金博士一点全通系列答案
金博士一点全通系列答案
相关题目
2.下列有关“化学与生活、社会”的叙述正确的是( )
| A. | 碘是人体必需微量元素,所以要多吃富含高碘酸的食物 | |
| B. | “霾尘积聚难见路人”,雾霾所形成的气溶胶有丁达尔效应 | |
| C. | 药皂中含有苯酚,能杀菌消毒,故苯酚具有强氧化性 | |
| D. | 屠呦呦获得了2015年诺贝尔奖,她用乙醚提取青蒿素的过程属于化学变化 |
3.已知X、Y、Z、W、R是原子序数依次增大的五种短周期主族元素,其中Y、R原子最外层电子数相等;X元素最低负价绝对值与W元素最高正价相等;工业上常用电解熔融氧化物的方法冶炼W单质;Z、W、R的最高价氧化物对应的水化物两两反应均生成盐和水.下列说法正确的是( )
| A. | 原子半径由大到小的顺序:Z、W、Y | |
| B. | 简单气态氢化物的稳定性由强到弱的顺序:X、Y、R | |
| C. | W的最高价氧化物对应的水化物碱性比Z的强 | |
| D. | R的最高价氧化物对应的水化物化学式一定是HRO4 |
17.某合作学习小组讨论辨析以下说法,其中正确的是( )
①碘酒和酸雨都是混合物;
②汽油和柴油都是纯净物;
③冰和干冰既是纯净物又是氧化物;
④铝合金和目前流通的硬币都是合金;
⑤盐酸和硫酸既是化合物又是酸;
⑥纯碱和烧碱都是碱;
⑦豆浆和牛奶都是胶体.
①碘酒和酸雨都是混合物;
②汽油和柴油都是纯净物;
③冰和干冰既是纯净物又是氧化物;
④铝合金和目前流通的硬币都是合金;
⑤盐酸和硫酸既是化合物又是酸;
⑥纯碱和烧碱都是碱;
⑦豆浆和牛奶都是胶体.
| A. | ①③④⑦ | B. | ①②⑤⑥ | C. | ③⑤⑥⑦ | D. | ①②③④ |
4.白磷燃烧的能价量变化(图Ⅰ)和产物的结构(图Ⅱ)如下图所示.有关说法不正确的是( )

| A. | 白磷的燃烧热为E2-E1 | |
| B. | 白磷分子中磷原子的杂化方式为sp3 | |
| C. | 1molP4O10中σ键的数目为16NA | |
| D. | 假设P-P、P-O、O=O的键能分别为a、b、c,则P=O的健能为(6a+5c-12b)/4 |
8.下列有关实验操作的说法错误的是( )
| A. | 中和滴定盛待测液的锥形瓶中有少量水对滴定结果无影响,锥形瓶不能用待测液润洗 | |
| B. | 酸式和碱式滴定管用蒸馏水洗净后还需用标准液或待测液润洗 | |
| C. | 滴定时左手控制滴定管活塞,右手握持锥形瓶,边滴边振荡,眼睛注视滴定管的液面 | |
| D. | 称量氯化钠固体,氯化钠放在称量纸上,置于托盘天平的左盘,砝码放在天平的右盘 |
9.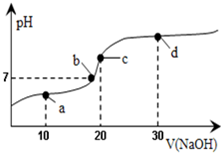 20℃时向20mL0.1mol/L醋酸溶液中不断滴入0.1mol/LNaOH(aq),溶液pH变化如图所示.此过程里溶液中离子浓度的关系错误的是( )
20℃时向20mL0.1mol/L醋酸溶液中不断滴入0.1mol/LNaOH(aq),溶液pH变化如图所示.此过程里溶液中离子浓度的关系错误的是( )
 20℃时向20mL0.1mol/L醋酸溶液中不断滴入0.1mol/LNaOH(aq),溶液pH变化如图所示.此过程里溶液中离子浓度的关系错误的是( )
20℃时向20mL0.1mol/L醋酸溶液中不断滴入0.1mol/LNaOH(aq),溶液pH变化如图所示.此过程里溶液中离子浓度的关系错误的是( )| A. | a点:c(CH3COO-)>c(Na+)>c(H+)>c(OH-) | B. | b点:c(Na+)=c(CH3COO-)>c(H+)=c(OH-) | ||
| C. | c点:c(H+)=c(CH3COOH)+c(OH-) | D. | d点:c(Na+)>c(CH3COO-)>c(OH-)>c(H+) |