题目内容
3.已知X、Y、Z、W、R是原子序数依次增大的五种短周期主族元素,其中Y、R原子最外层电子数相等;X元素最低负价绝对值与W元素最高正价相等;工业上常用电解熔融氧化物的方法冶炼W单质;Z、W、R的最高价氧化物对应的水化物两两反应均生成盐和水.下列说法正确的是( )| A. | 原子半径由大到小的顺序:Z、W、Y | |
| B. | 简单气态氢化物的稳定性由强到弱的顺序:X、Y、R | |
| C. | W的最高价氧化物对应的水化物碱性比Z的强 | |
| D. | R的最高价氧化物对应的水化物化学式一定是HRO4 |
分析 X、Y、Z、W、R是原子序数依次增大的五种短周期主族元素,Z、W、R最高价氧化物对应的水化物两两反应均生成盐和水,应氢氧化铝与强酸、强碱反应,可推知Z为Na元素、W为Al元素,工业上常用电解熔融氧化铝的方法冶炼Al单质;X元素最低负价绝对值与W元素最高正价相等,X处于VA族,原子序数小于Al,故X为N元素;Y、R原子最外层电子数相等,若Y为O,则R为S,若Y为F,则R为Cl,据此解答.
解答 解:X、Y、Z、W、R是原子序数依次增大的五种短周期主族元素,Z、W、R最高价氧化物对应的水化物两两反应均生成盐和水,应氢氧化铝与强酸、强碱反应,可推知Z为Na、W为Al,工业上常用电解熔融氧化铝的方法冶炼Al单质;X元素最低负价绝对值与W元素最高正价相等,X处于VA族,原子序数小于Al,故X为N元素;Y、R原子最外层电子数相等,若Y为O,则R为S,若Y为F,则R为Cl.
A.Y为O或F,Z为Na,W为Al,同周期随原子序数增大,原子半径减小,电子层越多半径越大,所以原子半径由大到小的顺序:Z、W、Y,故A正确;
B.X、Y为同周期元素,Y的非金属性强于X,故氢化物稳定性Y>X,故B错误;
C.金属性Al<Na,故碱性:氢氧化铝<氢氧化钠,故C错误;
D.R为S时,最高价氧化物对应水化物为H2SO4,故D错误.
故选A.
点评 本题考查原子结构和元素周期律,侧重考查学生分析推断能力,推断元素是解题的关键,注意Y、R元素的不确定性,明确元素周期律即可解答,难度不大.

练习册系列答案
 全优考典单元检测卷及归类总复习系列答案
全优考典单元检测卷及归类总复习系列答案
相关题目
11.卤族元素的单质和化合物很多,我们可以利用所学物质结构与性质的相关知识去认识和理解.
(1)卤族元素位于周期表的p区;溴的价电子排布式为4s24p5
(2)在不太稀的溶液中,氢氟酸是以二分子缔合(HF)2形式存在.使氢氟酸分子缔合的作用力是氢键
(3)请根据下表提供的第一电离能数据判断:最有可能生成较稳定的单核阳离子的卤素原子是碘
(4)已知高碘酸有两种形式,化学式分别为H5IO6(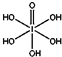 )和HIO4,前者为五元酸,后者为一元酸.请比较二者酸性强弱:H5IO6<HIO4(填“>”、“<”或“=”)
)和HIO4,前者为五元酸,后者为一元酸.请比较二者酸性强弱:H5IO6<HIO4(填“>”、“<”或“=”)
(5)已知ClO2-为角型,中心氯原子周围有四对价层电子.ClO2-中心氯原子的杂化轨道类型为sp3,写出CN-的等电子体的分子式N2或 CO(写出1个)
(6)如图1为碘晶体晶胞结构.有关说法中正确的是AD
A.碘分子的排列有2种不同的取向,2种取向不同的碘分子以4配位数交替配位形成层结构
B.用均摊法可知平均每个晶胞中有4个碘原子
C.碘晶体为无限延伸的空间结构,是原子晶体
D.碘晶体中的碘原子间存在非极性键和范德华力
(7)已知CaF2晶体(见图2)的密度为ρg/cm3,NA为阿伏加德罗常数,相邻的两个Ca2+的核间距为a cm,则CaF2的相对分子质量可以表示为$\frac{\sqrt{2}}{2}$ρNAa3

(1)卤族元素位于周期表的p区;溴的价电子排布式为4s24p5
(2)在不太稀的溶液中,氢氟酸是以二分子缔合(HF)2形式存在.使氢氟酸分子缔合的作用力是氢键
(3)请根据下表提供的第一电离能数据判断:最有可能生成较稳定的单核阳离子的卤素原子是碘
| 氟 | 氯 | 溴 | 碘 | 铍 | |
| 第一电离能 (kJ/mol) | 1681 | 1251 | 1140 | 1008 | 900 |
 )和HIO4,前者为五元酸,后者为一元酸.请比较二者酸性强弱:H5IO6<HIO4(填“>”、“<”或“=”)
)和HIO4,前者为五元酸,后者为一元酸.请比较二者酸性强弱:H5IO6<HIO4(填“>”、“<”或“=”)(5)已知ClO2-为角型,中心氯原子周围有四对价层电子.ClO2-中心氯原子的杂化轨道类型为sp3,写出CN-的等电子体的分子式N2或 CO(写出1个)
(6)如图1为碘晶体晶胞结构.有关说法中正确的是AD
A.碘分子的排列有2种不同的取向,2种取向不同的碘分子以4配位数交替配位形成层结构
B.用均摊法可知平均每个晶胞中有4个碘原子
C.碘晶体为无限延伸的空间结构,是原子晶体
D.碘晶体中的碘原子间存在非极性键和范德华力
(7)已知CaF2晶体(见图2)的密度为ρg/cm3,NA为阿伏加德罗常数,相邻的两个Ca2+的核间距为a cm,则CaF2的相对分子质量可以表示为$\frac{\sqrt{2}}{2}$ρNAa3

8.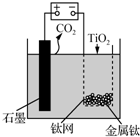 用如图所示装置(熔融CaF2-CaO作电解质)获得金属钙,并用钙还原TiO2制备金属钛.下列说法正确的是( )
用如图所示装置(熔融CaF2-CaO作电解质)获得金属钙,并用钙还原TiO2制备金属钛.下列说法正确的是( )
 用如图所示装置(熔融CaF2-CaO作电解质)获得金属钙,并用钙还原TiO2制备金属钛.下列说法正确的是( )
用如图所示装置(熔融CaF2-CaO作电解质)获得金属钙,并用钙还原TiO2制备金属钛.下列说法正确的是( )| A. | 电解过程中,Ca2+向阳极移动 | |
| B. | 阳极的电极反应式为:C+2O2--4e-═CO2↑ | |
| C. | 在制备金属钛前后,整套装置中CaO的总量减少 | |
| D. | 若用铅蓄电池作该装置的供电电源,“+”接线柱是Pb电极 |
15.下列说法正确的是( )
| A. | 大分子化合物油脂在人体内水解为氨基酸和甘油等小分子才能被吸收 | |
| B. | 现代科技已经能够拍到氢键的“照片”,直观地证实了水分子间的氢键是一个水分子中的氢原子与另一个水分子中的氧原子间形成的化学键 | |
| C. | 我国已能利用3D打印技术,以钛合金粉末为原料,通过激光熔化逐层堆积,来制造飞机钛合金结构件,高温时可用金属钠还原相应的氯化物来制取金属钛 | |
| D. | 用活性炭为糖浆脱色和用次氯酸盐漂白纸浆的原理相同 |
20.在相同温度时,100mL 0.01mol•L-1的醋酸溶液与10mL 0.1mol•L-1的醋酸溶液相比较,下列数值中,前者大于后者的是( )
| A. | 电离程度 | B. | 醋酸的电离常数 | ||
| C. | 中和时所需NaOH的物质的量 | D. | CH3COOH的物质的量 |
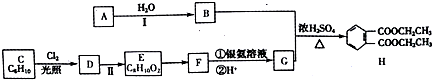
 等.
等.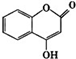 可用来制备抗凝血药,通过如图路线合成:
可用来制备抗凝血药,通过如图路线合成: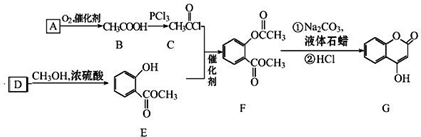
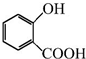 +CH3OH$→_{△}^{浓硫酸}$
+CH3OH$→_{△}^{浓硫酸}$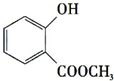 +H2O;
+H2O;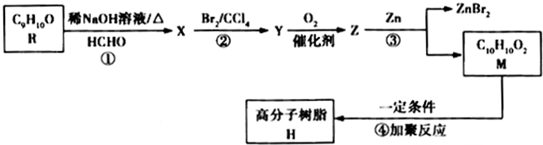
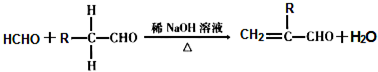
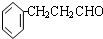 .
.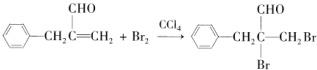 .
.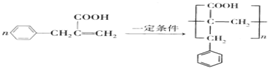 .
. .
.