题目内容
(1)将物质的量浓度相同的醋酸和氢氧化钠溶液混合后,溶液中c(CH3COO-)=c(Na+),则混合后溶液呈 (填“酸”“碱”或“中”)性,醋酸与氢氧化钠溶液体积大小关系是V(CH3COOH) (填“>”“=”或“<”)V(NaOH).
(2)常温下将0.1mol?L-1的HCN溶液与0.1mol?L-1的NaCN溶液等体积混合,溶液中c(HCN)>c(CN-).则该混合溶液的pH (填“>”“<”或“=”,下同)7;c(HCN)+c(CN-) 0.1mol?L-1;
c(OH-).
(2)常温下将0.1mol?L-1的HCN溶液与0.1mol?L-1的NaCN溶液等体积混合,溶液中c(HCN)>c(CN-).则该混合溶液的pH
| c HCN-c CN- |
| 2 |
考点:盐类水解的应用,弱电解质在水溶液中的电离平衡
专题:盐类的水解专题
分析:(1)混合溶液中c(CH3COO-)=c(Na+),根据电荷守恒得c(OH-)=c(H+),据此确定溶液酸碱性,醋酸钠溶液呈碱性,要使混合溶液呈中性,醋酸的物质的量应该稍微大于氢氧化钠;
(2)混合溶液中c(HCN)>c(CN-)说明HCN的电离程度小于CN-的水解程度,溶液呈碱性,溶液中存在物料守恒和电荷守恒,据此分析解答.
(2)混合溶液中c(HCN)>c(CN-)说明HCN的电离程度小于CN-的水解程度,溶液呈碱性,溶液中存在物料守恒和电荷守恒,据此分析解答.
解答:
解:(1)混合溶液中c(CH3COO-)=c(Na+),根据电荷守恒得c(OH-)=c(H+),溶液呈中性,醋酸钠溶液呈碱性,要使混合溶液呈中性,醋酸的物质的量应该稍微大于氢氧化钠,醋酸和氢氧化钠浓度相等,所以醋酸体积大于氢氧化钠,故答案为:中;>;
(2)混合溶液中c(HCN)>c(CN-)说明HCN的电离程度小于CN-的水解程度,溶液呈碱性,则pH>7,
溶液中存在物料守恒,根据物料守恒得c(HCN)+c(CN-)=0.1mol/L,
溶液中存在电荷守恒c(Na+)+c(H+)=c(OH-)+c(CN-)、存在物料守恒2c(Na+)=c(HCN)+c(CN-),所以得c(HCN)+2c(H+)=2c(OH-)+c(CN-),
=c(OH-)-c(H+)<c(OH-),
故答案为:>;=;<.
(2)混合溶液中c(HCN)>c(CN-)说明HCN的电离程度小于CN-的水解程度,溶液呈碱性,则pH>7,
溶液中存在物料守恒,根据物料守恒得c(HCN)+c(CN-)=0.1mol/L,
溶液中存在电荷守恒c(Na+)+c(H+)=c(OH-)+c(CN-)、存在物料守恒2c(Na+)=c(HCN)+c(CN-),所以得c(HCN)+2c(H+)=2c(OH-)+c(CN-),
| c HCN-c CN- |
| 2 |
故答案为:>;=;<.
点评:本题考查了弱电解质的电离及盐类水解,根据溶液酸碱性确定酸的电离和酸根离子水解程度大小,结合电荷守恒、物料守恒分析解答,注意(2)题,二者混合时溶液体积增大一倍导致浓度降为原来的一半,为易错点.

练习册系列答案
相关题目
下列化合物中,所有原子都处于同一平面的是( )
| A、乙烷 | B、甲苯 |
| C、氟苯 | D、二氧化硅 |
铝热法炼铁的化学方程式是:Fe2O3+2Al
2Fe+Al2O3,这种金属冶炼的方法属于( )
| ||
| A、热还原法 | B、热分解法 |
| C、电解法 | D、以上三种方法均是 |
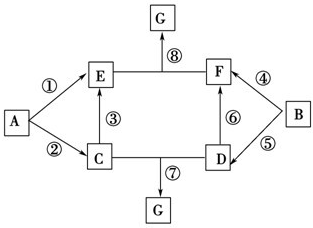 A~G的转化关系如图所示(部分反应物、产物和反应条件未标出).
A~G的转化关系如图所示(部分反应物、产物和反应条件未标出).