题目内容
室温下,某水溶液中只存在下列四种离子:Na+、A-、H+、OH-.
(1)若HA为弱酸,现有两组溶液
A组:由0.4mol/L的HA溶液与0.2mol/L的NaOH溶液等体积混合后混合液的pH<7;
B组:0.1mol/L的HA溶液
①A组溶液中除水分子外的各种微粒浓度由大到小的顺序是 ;
②两组溶液中c(A-)的大小,A组 B组(填“>”“<”或“=”);溶液中水的电离程度A组 B组(填“>”“<”或“=”).
(2)常温下,如果取0.1mol/L HA溶液与0.1mol/L NaOH溶液等体积混合(忽略混合后溶液体积的变化),测得混合溶液的pH=8,求出混合液中下列算式的精确计算结果(填具体数字):c(OH-)-c(HA)= mol/L.
(3)若由pH=3的HA溶液V1mL与pH=11的NaOH溶液V2mL混合而得,则下列说法正确的是 (填选项字母).
A.若反应后溶液呈中性,则c(OH-)+c(H+)=2×10-7mol/L
B.若V1=V2,反应后溶液一定呈中性
C.若反应后溶液呈酸性,则V1一定大于 V2
D.若反应后溶液呈碱性,则V1一定小于 V2
(4)某温度测得0.01mol?L-1的NaOH溶液的pH=11.在此温度下,将pH=2的H2SO4溶液VaL与pH=12的NaOH溶液VbL混合,若所得混合液为中性,则Va:Vb= .
(1)若HA为弱酸,现有两组溶液
A组:由0.4mol/L的HA溶液与0.2mol/L的NaOH溶液等体积混合后混合液的pH<7;
B组:0.1mol/L的HA溶液
①A组溶液中除水分子外的各种微粒浓度由大到小的顺序是
②两组溶液中c(A-)的大小,A组
(2)常温下,如果取0.1mol/L HA溶液与0.1mol/L NaOH溶液等体积混合(忽略混合后溶液体积的变化),测得混合溶液的pH=8,求出混合液中下列算式的精确计算结果(填具体数字):c(OH-)-c(HA)=
(3)若由pH=3的HA溶液V1mL与pH=11的NaOH溶液V2mL混合而得,则下列说法正确的是
A.若反应后溶液呈中性,则c(OH-)+c(H+)=2×10-7mol/L
B.若V1=V2,反应后溶液一定呈中性
C.若反应后溶液呈酸性,则V1一定大于 V2
D.若反应后溶液呈碱性,则V1一定小于 V2
(4)某温度测得0.01mol?L-1的NaOH溶液的pH=11.在此温度下,将pH=2的H2SO4溶液VaL与pH=12的NaOH溶液VbL混合,若所得混合液为中性,则Va:Vb=
考点:酸碱混合时的定性判断及有关ph的计算,弱电解质在水溶液中的电离平衡
专题:电离平衡与溶液的pH专题
分析:(1)①由0.4mol/L的HA溶液与0.2mol/L的NaOH溶液等体积混合后反应得到混合溶液HA和NaA,混合液的pH<7,说明弱酸电离大于A-离子水解分析判断了浓度;
②A组溶液中是等浓度的HA和NaA,混合溶液中HA浓度0.1mol/L,NaA浓度为0.1mol/L,B组是0.1mol/L的HA溶液,两组溶液中c(A-)A组大;NaA溶液中A-抑制酸的电离,A-离子水解浓度减小,水的电离程度增大;
(2)取0.1mol/L HA溶液与0.1mol/L NaOH溶液等体积混合,溶液的pH=8,则c(H+)=10-8mol/L,c(OH-)=10-6mol/L,根据依据溶液中质子守恒计算判断;
(3)A.若混合溶液呈中性,则氢离子浓度等于氢氧根离子浓度;
B.如果二者体积相等,根据酸的强弱判断混合溶液的酸碱性;
C.如果溶液呈酸性,则溶液可能是酸和盐溶液;
D.如果溶液呈碱性,则溶液可能是碱和盐溶液,也可能只是盐溶液.
(4)某温度(t℃)时,测得0.01mol?L-1的NaOH溶液的pH=11,据此计算离子积常数,将pH=2的H2SO4溶液VaL与pH=12的NaOH溶液VbL混合,若所得混合液为中性说明氢离子和氢氧根离子物质的量相同,列式计算.
②A组溶液中是等浓度的HA和NaA,混合溶液中HA浓度0.1mol/L,NaA浓度为0.1mol/L,B组是0.1mol/L的HA溶液,两组溶液中c(A-)A组大;NaA溶液中A-抑制酸的电离,A-离子水解浓度减小,水的电离程度增大;
(2)取0.1mol/L HA溶液与0.1mol/L NaOH溶液等体积混合,溶液的pH=8,则c(H+)=10-8mol/L,c(OH-)=10-6mol/L,根据依据溶液中质子守恒计算判断;
(3)A.若混合溶液呈中性,则氢离子浓度等于氢氧根离子浓度;
B.如果二者体积相等,根据酸的强弱判断混合溶液的酸碱性;
C.如果溶液呈酸性,则溶液可能是酸和盐溶液;
D.如果溶液呈碱性,则溶液可能是碱和盐溶液,也可能只是盐溶液.
(4)某温度(t℃)时,测得0.01mol?L-1的NaOH溶液的pH=11,据此计算离子积常数,将pH=2的H2SO4溶液VaL与pH=12的NaOH溶液VbL混合,若所得混合液为中性说明氢离子和氢氧根离子物质的量相同,列式计算.
解答:
解:(1)①由0.4mol/L的HA溶液与0.2mol/L的NaOH溶液等体积混合后反应得到混合溶液HA和NaA,混合溶液中HA浓度0.1mol/L,NaA浓度为0.1mol/L,混合液的pH<7,说明弱酸电离大于A-离子水解,溶液中离子浓度大小为:c(A-)>c(Na+)>c(HA)>c(H+)>c(OH-);
故答案为:c(A-)>c(Na+)>c(HA)>c(H+)>c(OH-);
②A组溶液中是等浓度的HA和NaA,混合溶液中HA浓度0.1mol/L,NaA浓度为0.1mol/L,B组是0.1mol/L的HA溶液,两组溶液中c(A-)A组大;NaA溶液中A-抑制酸的电离,A-离子水解浓度减小,水的电离程度增大;
故答案为:>;>;
(2)取0.1mol/L HA溶液与0.1mol/L NaOH溶液等体积混合,溶液的pH=8,c(H+)=10-8mol/L,c(OH-)=10-6mol/L,溶液显碱性,说明A-离子水解,溶液中存在质子守恒:c(OH-)=c(H+)+c(HA),则c(OH-)-c(HA)=c(H+)=10-8mol/L,故答案为:10-8;
(3)A.若混合溶液呈中性,则溶液M中c(H+)=c(OH-)=2×10-7 mol?L-1,所以溶液M中c(H+)+c(OH-)=2×10-7 mol?L-1,故正确;
B.如果二者体积相等,如果酸是强酸,则混合溶液呈中性,如果酸是弱酸,则混合溶液呈酸性,故错误;
C.如果溶液呈酸性,则溶液是酸和盐溶液,酸是弱酸,酸浓度大于氢氧化钠浓度,所以V1不一定大于V2,故错误;
D.如果溶液呈碱性,则溶液可能是碱和盐溶液,也可能只是盐溶液,则V1一定小于V2,故正确;
故选AD;
(4)某温度(t℃)时,测得0.01mol?L-1的NaOH溶液的pH=11,据此计算离子积常数Kw=0.01mol/L×10-11mol/L=10-13(mol/L),将pH=2的H2SO4溶液VaL与pH=12的NaOH溶液VbL混合,若所得混合液为中性说明氢离子和氢氧根离子物质的量相同,10-2×Va=
×Vb,得到Va:Vb=10:1,
故答案为:10:1.
故答案为:c(A-)>c(Na+)>c(HA)>c(H+)>c(OH-);
②A组溶液中是等浓度的HA和NaA,混合溶液中HA浓度0.1mol/L,NaA浓度为0.1mol/L,B组是0.1mol/L的HA溶液,两组溶液中c(A-)A组大;NaA溶液中A-抑制酸的电离,A-离子水解浓度减小,水的电离程度增大;
故答案为:>;>;
(2)取0.1mol/L HA溶液与0.1mol/L NaOH溶液等体积混合,溶液的pH=8,c(H+)=10-8mol/L,c(OH-)=10-6mol/L,溶液显碱性,说明A-离子水解,溶液中存在质子守恒:c(OH-)=c(H+)+c(HA),则c(OH-)-c(HA)=c(H+)=10-8mol/L,故答案为:10-8;
(3)A.若混合溶液呈中性,则溶液M中c(H+)=c(OH-)=2×10-7 mol?L-1,所以溶液M中c(H+)+c(OH-)=2×10-7 mol?L-1,故正确;
B.如果二者体积相等,如果酸是强酸,则混合溶液呈中性,如果酸是弱酸,则混合溶液呈酸性,故错误;
C.如果溶液呈酸性,则溶液是酸和盐溶液,酸是弱酸,酸浓度大于氢氧化钠浓度,所以V1不一定大于V2,故错误;
D.如果溶液呈碱性,则溶液可能是碱和盐溶液,也可能只是盐溶液,则V1一定小于V2,故正确;
故选AD;
(4)某温度(t℃)时,测得0.01mol?L-1的NaOH溶液的pH=11,据此计算离子积常数Kw=0.01mol/L×10-11mol/L=10-13(mol/L),将pH=2的H2SO4溶液VaL与pH=12的NaOH溶液VbL混合,若所得混合液为中性说明氢离子和氢氧根离子物质的量相同,10-2×Va=
| 10-13 |
| 10-12 |
故答案为:10:1.
点评:本题考查了酸碱混合溶液定性判断,明确酸的强弱是解本题关键,根据混合溶液中的氢离子浓度和氢氧根离子浓度相对大小判断溶液的酸碱性,难度中等.

练习册系列答案
相关题目
下列说法正确的是( )
| A、棉、麻、羊毛及合成纤维完全燃烧都只生成CO2和H2O |
| B、蛋白质是结构复杂的高分子化合物,分子中都含有C、H、O、N四种元素 |
| C、用KMnO4酸性溶液鉴别CH3CH=CHCH2OH和CH3CH2CH2CHO |
| D、向盛有少量苯酚稀溶液试管中滴加少量稀溴水,边滴边振荡,有白色沉淀出现 |
反应①Fe(s)+CO2(g)?FeO(s)+CO(g)的平衡常数为K1;反应②Fe(s)+H2O(g)?FeO(s)+H2(g)的平衡常数为K2.在不同温度时K1、K2的值如下表.
下列说法正确的是( )
| 温度(K) | K1 | K2 |
| 973 | 1.47 | 2.38 |
| 1 173 | 2.15 | 1.67 |
| A、反应①是放热反应 |
| B、反应②是放热反应 |
| C、反应②在973K时增大压强,K2增大 |
| D、在常温下反应①一定能自发进行 |
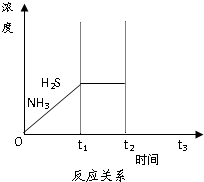 脱硫天然气中的硫化氢既能减少环境污染,又可回收硫资源.
脱硫天然气中的硫化氢既能减少环境污染,又可回收硫资源.