题目内容
13.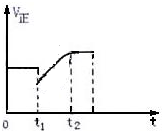 如图表示反应2SO2(g)+O2 $?_{加热}^{催化剂}$ 2SO3(g)+Q的正反应速率随时间的变化情况,试根据图曲线判断下列说法可能正确的是( )
如图表示反应2SO2(g)+O2 $?_{加热}^{催化剂}$ 2SO3(g)+Q的正反应速率随时间的变化情况,试根据图曲线判断下列说法可能正确的是( )| A. | t1时只减小了压强 | |
| B. | t1时只降低了温度 | |
| C. | t1时增加了SO2和O2的浓度,平衡向正反应方向移动 | |
| D. | t1时减小SO2浓度的同时,增加了SO3的浓度 |
分析 由图知在t1时刻V正减小,反应逆向进行,重新平衡时的速率大于原平衡速率,新平衡时反应物浓度比原来还大,结合平衡移动判断.
解答 解:A、t1时减小了压强,平衡向逆反应方向移动,重新平衡时的速率小于原平衡速率,故A错误;
B、t1降低了温度,平衡向正反应移动,重新平衡时的速率小于原平衡速率,故B错误;
C、t1时增加了SO2和O2的浓度,正反应速率应大于原平衡速率,平衡向正反应方向移动,图象中t1时刻不符合,故C错误;
D、t1时减小了SO2的浓度,增加了SO3的浓度,平衡向逆反应移动,新平衡时反应物浓度比可以原来还大,平衡时正反应速率可以比原平衡速率大,故D正确.
故选D.
点评 本题考查化学平衡图象、化学平衡移动等,题目难度中等,根据图象提取信息是解题的关键.

练习册系列答案
相关题目
3.如图所示可逆反应:mA(g)+nB(g)?xC(g),△H=Q kJ/mol,在不同温度、压强下反应物A的转化率的变化情况.下列对于反应的热效应Q和反应方程式A、B、C的化学计量数的判断中,正确的是( )
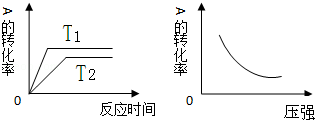

| A. | Q<0,m+n<x | B. | Q<0,m+n>x | C. | Q>0,m+n<x | D. | Q>0,m+n>x |
4.(1)捕碳技术(主要指捕获CO2)在降低温室气体排放中具有重要的作用.目前NH3和(NH4)2CO3已经被用作工业捕碳剂,它们与CO2可发生如下可逆反应.
反应Ⅰ:2NH3(l)+H2O(l)+CO2(g)?(NH4)2CO3(aq)△H1
反应Ⅱ:NH3(l)+H2O(l)+CO2(g)?NH4HCO3(aq)△H2
反应Ⅲ:(NH4)2CO3(aq)+H2O(l)+CO2(g)?2NH4HCO3(aq)△H3
则△H3与△H1、△H2之间的关系是:△H3=2△H2-△H1.
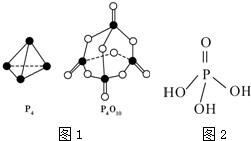
(2)白磷与氧气反应生成P4O10固体.下表所示是部分化学键的键能参数:
根据图1的分子结构和有关数据通过计算写出该反应的热化学方程式为P4(s)+5O2(g)═P4O10(s)△H=-(4c+12b-6a-5d)kJ•mol-1.
(3)三聚磷酸可视为三个磷酸分子(磷酸结构式如图2)之间脱去两个水分子产物,其结构式为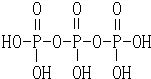 ,三聚磷酸钠(俗称“五钠”)是常用的水处理剂,其化学式为Na5P3O10.
,三聚磷酸钠(俗称“五钠”)是常用的水处理剂,其化学式为Na5P3O10.
(4)已知298K时白磷不完全燃烧的热化学方程式为:P4(s,白磷)+3O2(g)═P4O6(s)△H=-1 638kJ•mol-1.
在某密闭容器中加入62g白磷和50.4L氧气(标准状况),控制条件使之恰好完全反应.则所得到的P4O10与P4O6的物质的量之比为3:1.

反应Ⅰ:2NH3(l)+H2O(l)+CO2(g)?(NH4)2CO3(aq)△H1
反应Ⅱ:NH3(l)+H2O(l)+CO2(g)?NH4HCO3(aq)△H2
反应Ⅲ:(NH4)2CO3(aq)+H2O(l)+CO2(g)?2NH4HCO3(aq)△H3
则△H3与△H1、△H2之间的关系是:△H3=2△H2-△H1.
(2)白磷与氧气反应生成P4O10固体.下表所示是部分化学键的键能参数:
| 化学键 | P-P | P-O | P═O | O═O |
| 键能/kJ•mol-1 | a | b | c | d |
(3)三聚磷酸可视为三个磷酸分子(磷酸结构式如图2)之间脱去两个水分子产物,其结构式为
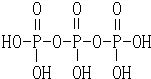 ,三聚磷酸钠(俗称“五钠”)是常用的水处理剂,其化学式为Na5P3O10.
,三聚磷酸钠(俗称“五钠”)是常用的水处理剂,其化学式为Na5P3O10.(4)已知298K时白磷不完全燃烧的热化学方程式为:P4(s,白磷)+3O2(g)═P4O6(s)△H=-1 638kJ•mol-1.
在某密闭容器中加入62g白磷和50.4L氧气(标准状况),控制条件使之恰好完全反应.则所得到的P4O10与P4O6的物质的量之比为3:1.
1.下列解释事实的离子方程式正确的是( )
| A. | 铁和稀硝酸反应制得浅绿色溶液:Fe+4H++NO3-═Fe3++NO↑+2H2O | |
| B. | 在NaClO溶液中通入过量SO2气体:ClO-+H2O+SO2═HClO+HSO3- | |
| C. | NaHCO3与少量Ca(OH)2溶液反应:Ca2++2OH-+2HCO3-═CaCO3↓+2H2O+CO32- | |
| D. | 10mL 0.5mol/L的明矾溶液与20mL 0.5mol/L的Ba(OH)2溶液混合反应:3Ba2++6OH-+2Al3++3SO42-═3BaSO4↓+2Al(OH)3↓ |
18.为提纯下列物质(括号内为杂质)选用的试剂和分离方法都正确的是( )
| 序号 | 物质 | 试剂 | 分离方法 |
| ① | 硝酸钾(氯化钠) | 蒸馏水 | 重结晶 |
| ② | 二氧化碳(氯化氢) | 饱和碳酸钠溶液 | 洗气 |
| ③ | 乙醇(水) | 金属钠 | 蒸馏 |
| ④ | NaCl溶液(Na2S) | AgCl | 过滤 |
| A. | ①③ | B. | ①④ | C. | ② | D. | ③④ |
5.氨催化氧化法制硝酸的原理为4NH3(g)+5O2(g)$?_{△}^{Pt}$4NO(g)+6H2O(g).在浓氨水中通入空气,将赤热铂
丝插入氨水中引发反应后铂丝保持红热状态至反应停止.下列说法正确的是( )
丝插入氨水中引发反应后铂丝保持红热状态至反应停止.下列说法正确的是( )
| A. | 上述反应在较高温度下才能自发进行 | |
| B. | 该反应的正反应活化能小于逆反应活化能 | |
| C. | 该反应中,断裂化学键的总键能大于形成化学键的总键能 | |
| D. | 若NH3和O2的混合气发生上述反应,气体通入足量水中,剩余气体一定是O2 |
2.下列装置中,电流表指针不能发生偏转的是( )
| A. | 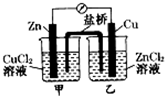 | B. | 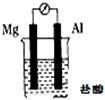 | ||
| C. | 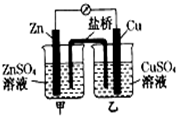 | D. |  |