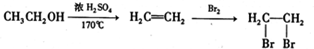题目内容
 化合物A经李比希法和质谱法分析得知其相对分子质量为136,分子式C8H8O2.其核磁共振氢谱与红外光谱如图,核磁共振氢谱面积之比为3:2:2:1.
化合物A经李比希法和质谱法分析得知其相对分子质量为136,分子式C8H8O2.其核磁共振氢谱与红外光谱如图,核磁共振氢谱面积之比为3:2:2:1.已知:A分子中只含一个苯环,且苯环上只有一个取代基,试填空.
(1)A的结构简式可能为
(2)A的芳香类同分异构体有多种,请按要求写出其中两种同分异构B和C结构简式:
①B是分子中不含甲基的芳香酸:
②C分子中含甲基,且遇FeCl3溶液显紫色,苯环上只有两上对位取代基的芳香醛:
(3)已知:

①C氧化为D时能否用酸性KMnO4溶液?说明理由:
②请用合成反应流程图表示出由C合成F的最合理的合法方案(注明反应条件).
提示:合成反应流程图表示方法示例如下:
A
| 反应条件 |
| 反应物 |
| 反应条件 |
| 反应物 |
考点:有机物的推断,有机物实验式和分子式的确定
专题:有机物的化学性质及推断
分析:(1)有机物A的分子式为分子式C8H8O2,不饱和度为
=5,A分子中只含一个苯环且苯环上只有一个取代基,其核磁共振氢谱有四个吸收峰,说明分子中含有4种H原子,峰面积之比为3:2:2:1,则四种氢原子个数之比=3:2:2:1,结合红外光谱可知,分子中存在酯基等基团,且苯环与C原子相连,故有机物A的结构简式为 ;
;
(2)A的芳香类同分异构体有多种,其中两种同分异构为B和C:
①B是分子中不含甲基的芳香酸,则侧链为-COOH;
②C分子中含甲基,且遇FeCl3溶液显紫色,含有酚羟基,苯环上只有两上对位取代基的芳香醛,故侧链为-OH、-CH2CHO;
(3)①由C、D分子式可知,C中醛基发生氧化反应转化为-COOH生成D,KmnO4氧化性强,会将羟基和支链都氧化,不能使用酸性KMnO4溶液氧化C;
②C为 ,在催化剂、加热条件下与氢气发生加成反应生成
,在催化剂、加热条件下与氢气发生加成反应生成 ,再在浓硫酸加热条件下发生水解反应生成
,再在浓硫酸加热条件下发生水解反应生成 .
.
| 2×8+2-8 |
| 2 |
 ;
;(2)A的芳香类同分异构体有多种,其中两种同分异构为B和C:
①B是分子中不含甲基的芳香酸,则侧链为-COOH;
②C分子中含甲基,且遇FeCl3溶液显紫色,含有酚羟基,苯环上只有两上对位取代基的芳香醛,故侧链为-OH、-CH2CHO;
(3)①由C、D分子式可知,C中醛基发生氧化反应转化为-COOH生成D,KmnO4氧化性强,会将羟基和支链都氧化,不能使用酸性KMnO4溶液氧化C;
②C为
 ,在催化剂、加热条件下与氢气发生加成反应生成
,在催化剂、加热条件下与氢气发生加成反应生成 ,再在浓硫酸加热条件下发生水解反应生成
,再在浓硫酸加热条件下发生水解反应生成 .
.解答:
解:(1)有机物A的分子式为分子式C8H8O2,不饱和度为
=5,A分子中只含一个苯环且苯环上只有一个取代基,其核磁共振氢谱有四个吸收峰,说明分子中含有4种H原子,峰面积之比为3:2:2:1,则四种氢原子个数之比=3:2:2:1,结合红外光谱可知,分子中存在酯基等基团,且苯环与C原子相连,故有机物A的结构简式为 ,故答案为:
,故答案为: ;
;
(2)A的芳香类同分异构体有多种,其中两种同分异构为B和C:
①B是分子中不含甲基的芳香酸,则侧链为-COOH,故B的结构简式为 ,故答案为:
,故答案为: ;
;
②C分子中含甲基,且遇FeCl3溶液显紫色,含有酚羟基,苯环上只有两上对位取代基的芳香醛,故侧链为-OH、-CH2CHO,故C的结构简式为: ,故答案为:
,故答案为: ;
;
(3)①由C、D分子式可知,C中醛基发生氧化反应转化为-COOH生成D,KmnO4氧化性强,会将羟基和支链都氧化,不能使用酸性KMnO4溶液氧化C,故答案为:不能,KmnO4氧化性强,会将羟基和支链都氧化;
②C为 ,在催化剂、加热条件下与氢气发生加成反应生成
,在催化剂、加热条件下与氢气发生加成反应生成 ,再在浓硫酸加热条件下发生水解反应生成
,再在浓硫酸加热条件下发生水解反应生成 ,合成反应流程图为:
,合成反应流程图为: ,
,
故答案为: .
.
| 2×8+2-8 |
| 2 |
 ,故答案为:
,故答案为: ;
;(2)A的芳香类同分异构体有多种,其中两种同分异构为B和C:
①B是分子中不含甲基的芳香酸,则侧链为-COOH,故B的结构简式为
 ,故答案为:
,故答案为: ;
;②C分子中含甲基,且遇FeCl3溶液显紫色,含有酚羟基,苯环上只有两上对位取代基的芳香醛,故侧链为-OH、-CH2CHO,故C的结构简式为:
 ,故答案为:
,故答案为: ;
;(3)①由C、D分子式可知,C中醛基发生氧化反应转化为-COOH生成D,KmnO4氧化性强,会将羟基和支链都氧化,不能使用酸性KMnO4溶液氧化C,故答案为:不能,KmnO4氧化性强,会将羟基和支链都氧化;
②C为
 ,在催化剂、加热条件下与氢气发生加成反应生成
,在催化剂、加热条件下与氢气发生加成反应生成 ,再在浓硫酸加热条件下发生水解反应生成
,再在浓硫酸加热条件下发生水解反应生成 ,合成反应流程图为:
,合成反应流程图为: ,
,故答案为:
 .
.
点评:本题考查有机物结构的推断、核磁共振氢谱、红外光谱图、官能团性质等,难度中等,推断A的结构是解题的关键,注意结合分子式与红外光谱含有的基团进行判断.

练习册系列答案
 启东小题作业本系列答案
启东小题作业本系列答案
相关题目
用NA表示阿伏加德罗常数的值,下列叙述不正确的是( )
| A、16g氧气和臭氧(O3)的混合气体所含原子数为NA |
| B、0.1molN5+离子中所含电子数为3.4NA |
| C、如果22.4 L的气体含有NA个分子,则必定是在标准状况下 |
| D、常温常压下,44gCO2中含有NA个CO2分子 |
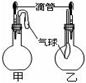 如图所示的甲、乙两个装置中,胶头滴管中吸入某种液体,平底烧瓶中充入(或放入)另一种物质,挤压胶头滴管加入液体,一段时间后两装置中的气球都有明显地胀大(忽略液体体积对气球的影响).则所用试剂分别可能依次是( )
如图所示的甲、乙两个装置中,胶头滴管中吸入某种液体,平底烧瓶中充入(或放入)另一种物质,挤压胶头滴管加入液体,一段时间后两装置中的气球都有明显地胀大(忽略液体体积对气球的影响).则所用试剂分别可能依次是( )| A、甲:铝粉和浓NaOH溶液 乙:饱和NaCl溶液和Cl2 |
| B、甲:双氧水和MnO2 乙:NaOH溶液和CO2 |
| C、甲:浓氨水和碱石灰 乙:浓氨水和SO2 |
| D、甲:水和CO2 乙:水和氯化氢 |
将2.0molSO2气体和2.0molSO3气体混合于固定体积的密闭容器中,在一定条件下发生反应:2SO2(g)+O2(g)?2SO3(g),达到平衡时SO3为nmol.在相同温度下,分别按下列配比在相同密闭容器中放入起始物质,平衡时SO3等于nmol的是( )
| A、1.6molSO2+0.3molO2+0.4molSO3 |
| B、4.0molSO2+1.0molO2 |
| C、2.0molSO2+1.0molO2+2.0molSO3 |
| D、3.0molSO2+1.0molO2+1.0molSO3 |
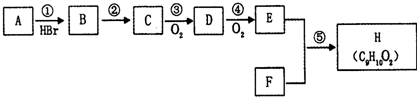


 ):又当苯环上连卤原子时,高温高压下可以水解.
):又当苯环上连卤原子时,高温高压下可以水解.


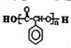 的合成路线流程图(无机试剂任选,限用4步完成).合成路线流程图如图:
的合成路线流程图(无机试剂任选,限用4步完成).合成路线流程图如图: