题目内容
常温时,下列三个反应都能向右进行:由此得出的正确结论是( )
2W-+X2═2X-+W2
2Y-+W2═2W-+Y2
2X-+Z2═2Z-+X2.
2W-+X2═2X-+W2
2Y-+W2═2W-+Y2
2X-+Z2═2Z-+X2.
| A、X-、Y-、Z-、W-中Z-的还原性最强 |
| B、X2、Y2、Z2、W2中Z2的氧化性最弱 |
| C、2Z-+Y2═2Y-+Z2不能向右进行 |
| D、还原性X->Y- |
考点:氧化还原反应
专题:氧化还原反应专题
分析:2W-+X2=W2+2X-,该反应中作X2氧化剂,还原产物是X-,W-作还原剂,氧化产物是W2,所以氧化性X2>W2,还原性W->X-;
2Y-+W2=2W-+Y2,该反应中作W2氧化剂,还原产物是W-,Y-作还原剂,氧化产物是Y2,所以氧化性W2>Y2,还原性Y->W-;
2X-+Z2=2Z-+X2,该反应中作Z2氧化剂,还原产物是Z-,X-作还原剂,氧化产物是X2,所以氧化性Z2>X2,还原性X->Z-;
氧化性强弱顺序为:Z2>X2>W2>Y2,还原性强弱顺序为:Y->W->X->Z-,以此来解答.
2Y-+W2=2W-+Y2,该反应中作W2氧化剂,还原产物是W-,Y-作还原剂,氧化产物是Y2,所以氧化性W2>Y2,还原性Y->W-;
2X-+Z2=2Z-+X2,该反应中作Z2氧化剂,还原产物是Z-,X-作还原剂,氧化产物是X2,所以氧化性Z2>X2,还原性X->Z-;
氧化性强弱顺序为:Z2>X2>W2>Y2,还原性强弱顺序为:Y->W->X->Z-,以此来解答.
解答:
解:2W-+X2=W2+2X-,该反应中作X2氧化剂,还原产物是X-,W-作还原剂,氧化产物是W2,所以氧化性X2>W2,还原性W->X-;
2Y-+W2=2W-+Y2,该反应中作W2氧化剂,还原产物是W-,Y-作还原剂,氧化产物是Y2,所以氧化性W2>Y2,还原性Y->W-;
2X-+Z2=2Z-+X2,该反应中作Z2氧化剂,还原产物是Z-,X-作还原剂,氧化产物是X2,所以氧化性Z2>X2,还原性X->Z-;
氧化性强弱顺序为:Z2>X2>W2>Y2,还原性强弱顺序为:Y->W->X->Z-;
A.由上述分析可知,Y-的还原性最强,故A错误;
B.由上述分析可知,Z2的氧化性最强,故B错误;
C.氧化性强弱顺序为:Z2>Y2,所以反应2Z-+Y2═2Y-+Z2不能向右进行,故C正确;
D.由上述分析可知,还原性为Y->X-,故D错误;
故选C.
2Y-+W2=2W-+Y2,该反应中作W2氧化剂,还原产物是W-,Y-作还原剂,氧化产物是Y2,所以氧化性W2>Y2,还原性Y->W-;
2X-+Z2=2Z-+X2,该反应中作Z2氧化剂,还原产物是Z-,X-作还原剂,氧化产物是X2,所以氧化性Z2>X2,还原性X->Z-;
氧化性强弱顺序为:Z2>X2>W2>Y2,还原性强弱顺序为:Y->W->X->Z-;
A.由上述分析可知,Y-的还原性最强,故A错误;
B.由上述分析可知,Z2的氧化性最强,故B错误;
C.氧化性强弱顺序为:Z2>Y2,所以反应2Z-+Y2═2Y-+Z2不能向右进行,故C正确;
D.由上述分析可知,还原性为Y->X-,故D错误;
故选C.
点评:本题考查氧化还原反应,为高频考点,把握反应中元素的化合价变化及氧化性、还原性比较为解答的关键,侧重分析与应用能力的考查,题目难度不大.

练习册系列答案
 春雨教育同步作文系列答案
春雨教育同步作文系列答案
相关题目
关于
C的说法正确的是( )
| 12 |
| 6 |
| A、质量数为6 |
| B、质子数为6 |
| C、电子数为13 |
| D、中子数为6 |
下列关于化学用语的表示正确的是( )
A、碘化铵的电子式: |
B、间二甲苯的结构简式: |
| C、中子数为146、质子数为92的铀(U)原子:23892U |
D、氯原子的结构示意图: |
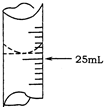 欲测定某NaOH溶液的物质的量浓度,可用0.1000mol?L-1HCl标准溶液进行中和滴定(用酚酞作指示剂).
欲测定某NaOH溶液的物质的量浓度,可用0.1000mol?L-1HCl标准溶液进行中和滴定(用酚酞作指示剂).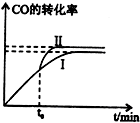 二甲醚是一种重要的清洁燃料,有多种合成方法.
二甲醚是一种重要的清洁燃料,有多种合成方法.
 的邻位异构体分子内脱水产物,香豆素的结构简式为
的邻位异构体分子内脱水产物,香豆素的结构简式为 某学习小组为证明并观察铜与稀HNO3反应的产物是NO,设计了如下图所示的实验装置.请你根据他们的思路,选择下列药品完成实验,填写实验步骤并回答问题.
某学习小组为证明并观察铜与稀HNO3反应的产物是NO,设计了如下图所示的实验装置.请你根据他们的思路,选择下列药品完成实验,填写实验步骤并回答问题.