题目内容
在下列反应中:A.2F2+2H2O=4HF+O2 B.2Na+2H2O=2NaOH+H2↑ C.CaO+H2O=Ca(OH)2
D.2H2O=2H2↑+O2↑ 水只作氧化剂的是 ,水只作还原剂的是 ,水既作氧化剂又作还原剂的是 ,水既不作氧化剂又不作还原剂的是 .
D.2H2O=2H2↑+O2↑ 水只作氧化剂的是
考点:氧化还原反应
专题:氧化还原反应专题
分析:有元素化合价变化的反应为氧化还原反应,含元素的化合价降低的物质为氧化剂,含元素化合价升高的物质为还原剂.
水作氧化剂时,H元素的化合价降低;水作还原剂时,O元素的化合价升高;水中H、O元素的化合价均变化,则既作氧化剂又作还原剂;水既不作氧化剂又不作还原剂,则反应前后水中H、O元素的化合价不变.
水作氧化剂时,H元素的化合价降低;水作还原剂时,O元素的化合价升高;水中H、O元素的化合价均变化,则既作氧化剂又作还原剂;水既不作氧化剂又不作还原剂,则反应前后水中H、O元素的化合价不变.
解答:
解:反应2F2+2H2O=4HF+O2中,水中氧元素化合价升高,水只作还原剂;
反应2Na+2H2O=2NaOH+H2↑中,水中氢元素化合价降低,只作氧化剂;
反应CaO+H2O=Ca(OH)2中,水中的氢元素和氧元素化合价均未变化,所以水既不作氧化剂也不作还原剂;
反应2H2O=2H2↑+O2↑中,水中的氢元素化合价降低,氧元素化合价升高,所以水既作氧化剂又作还原剂,
故答案为:B;A;D;C.
反应2Na+2H2O=2NaOH+H2↑中,水中氢元素化合价降低,只作氧化剂;
反应CaO+H2O=Ca(OH)2中,水中的氢元素和氧元素化合价均未变化,所以水既不作氧化剂也不作还原剂;
反应2H2O=2H2↑+O2↑中,水中的氢元素化合价降低,氧元素化合价升高,所以水既作氧化剂又作还原剂,
故答案为:B;A;D;C.
点评:本题考查氧化还原反应,为高频考点,把握反应中元素的化合价变化为解答的关键,侧重氧化还原反应基本概念的考查,注意从元素化合价角度分析,题目难度不大.

练习册系列答案
相关题目
下列说法正确的是( )
| A、SO3溶于水后能导电,故SO3为电解质 |
| B、强电解质的水溶液中不存在大量溶质分子 |
| C、向NaCN溶液中滴入酚酞试液显红色,则HCN为强酸 |
| D、25℃时,用CH3COOH溶液滴定等浓度NaOH溶液至pH=7,V(CH3COOH)<V(NaOH) |
下列各组离子在水溶液中能够大量共存的是( )
| A、OH-、SO42-、Fe3+ |
| B、NH4+、OH-、NO3- |
| C、Na+、Cl-、SO42- |
| D、H+、HCO3-、K+ |
常温时,下列三个反应都能向右进行:由此得出的正确结论是( )
2W-+X2═2X-+W2
2Y-+W2═2W-+Y2
2X-+Z2═2Z-+X2.
2W-+X2═2X-+W2
2Y-+W2═2W-+Y2
2X-+Z2═2Z-+X2.
| A、X-、Y-、Z-、W-中Z-的还原性最强 |
| B、X2、Y2、Z2、W2中Z2的氧化性最弱 |
| C、2Z-+Y2═2Y-+Z2不能向右进行 |
| D、还原性X->Y- |
胶体是一种重要的分散系.下列关于胶体的说法错误的是( )
| A、制备Fe(OH)3胶体的方法是在浓FeCl3溶液中加入大量浓NaOH溶液,并不断搅拌 |
| B、Fe(OH)3胶体中的胶体粒子大小在1~100nm之间 |
| C、可用丁达尔效应区分Fe(OH)3胶体和蔗糖溶液 |
| D、当光束通过有尘埃的空气或稀豆浆时都能观察到丁达尔效应 |
用下列实验装置能达到实验目的是( )
A、比较NaHCO3和Na2CO3热稳定性大小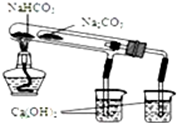 |
B、用铜和稀硝酸制取并收集少量NO |
C、验证氨气在水中溶解度的大小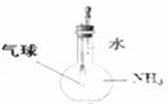 |
D、实验室用氯化铵制少量氨气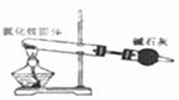 |
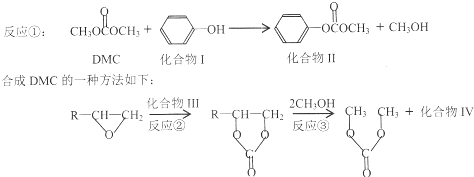
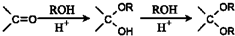
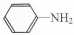 与DMC1:1发生类似反应①的反应,请写出反应方程式
与DMC1:1发生类似反应①的反应,请写出反应方程式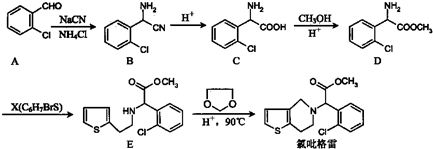
 的合成路线流程图(无机试剂任选).
的合成路线流程图(无机试剂任选).
