题目内容
18.X、Y、Z均为短周期主族元素,已知它们的原子序数的关系为 X+Z=2Y,且Z的最高价氧化物对应的水化物是强酸.则下列有关说法中正确的是( )| A. | 若X是Na,则Z 的最高价一定为偶数 | |
| B. | 若X是O,则YX一定是离子化合物 | |
| C. | 若Y是O,则非金属性:Z>Y>X | |
| D. | 若Y是Na,则X Z不可能是同一主族元素 |
分析 原子序数X+Z=2Y,则X和Z的原子序数只能同时为奇数或者同时为偶数,Z的最高价氧化物对应水化物是强酸,Z只能是N,S,Cl(短周期)等元素,以此解答该题.
解答 解:原子序数X+Z=2Y,则X和Z的原子序数只能同时为奇数或者同时为偶数,Z的最高价氧化物对应水化物是强酸,Z只能是N、S、Cl(短周期)等元素,
A.X是Na,则Z可为Cl,最高价是奇数,故A错误;
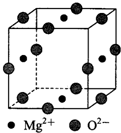
B.X是O,因为O原子序数是8,偶数,则Z只能是S,Y的原子序数为$\frac{8+16}{2}$2=12,Y是Mg,MgO是离子化合物,故B正确;
C.Y是O,则X+Z=16,只有Z为N,X为F满足,非金属性:F>O>N,即:X>Y>Z,故C错误;
D.Y是Na,则X+Z=22,Z可为N,Y为P元素,N和P是同一主族元素,7+15=22满足前述条件,故D错误.
故选B.
点评 本题考查原子结构与元素周期律的关系,为高频考点,注意根据原子序数的关系判断元素的种类是解答该题的关键,题目难度中等.

练习册系列答案
 桃李文化快乐暑假武汉出版社系列答案
桃李文化快乐暑假武汉出版社系列答案 优秀生快乐假期每一天全新寒假作业本系列答案
优秀生快乐假期每一天全新寒假作业本系列答案 暑假接力赛新疆青少年出版社系列答案
暑假接力赛新疆青少年出版社系列答案
相关题目
9.现代炼锌的方法可分为火法和湿法两大类.火法炼锌是将闪锌矿(主要含ZnS)焙烧使它转化为氧化锌,再把氧化锌和焦炭混合,在鼓风炉中加热至1100℃~1300℃,使锌蒸馏出来(设空气中N2、O2的体积分数分别为0.80、0.20),主要反应为:
焙烧炉中:2ZnS(s)+3O2(g)→2ZnO(s)+2SO2(g) ①
鼓风炉中:2C(s)+O2(g)→2CO ②
鼓风炉中:ZnO(s)+CO(g)?Zn(g)+CO2(g) ③
(1)已知闪锌矿中含硫的质量分数为16.0%,而所含杂质不含硫,则闪锌矿中硫化锌的质量分数为48.5%.现代工业生产多采用联合生产,可将闪锌矿中的硫用于生产硫酸.现有
此闪锌矿100t,在理论上可生产出98.0%的硫酸50t.
(2)焙烧炉产生的炉气中SO2的体积分数不超过14.3%(保留小数点后一位小数,下同).
(3)鼓风炉容积固定,炉内部分气态物质其物质的量浓度(mol/L)变化如下:
则鼓风炉中CO总的转化率为90.9%;若生产中CO总的利用率为95.0%,列式计算每生产1molZn,至少需要补充焦炭多少克?
(4)若ZnS全部转化为Zn,焙烧炉出来的N2、O2、SO2混合气体中N2占82.5%,鼓风炉中CO的转化率为62.5%,而O2无剩余,试列式计算每生产1mol Zn,应向焙烧炉和鼓风炉中鼓入新鲜空气共多少升(S.T.P)?
焙烧炉中:2ZnS(s)+3O2(g)→2ZnO(s)+2SO2(g) ①
鼓风炉中:2C(s)+O2(g)→2CO ②
鼓风炉中:ZnO(s)+CO(g)?Zn(g)+CO2(g) ③
(1)已知闪锌矿中含硫的质量分数为16.0%,而所含杂质不含硫,则闪锌矿中硫化锌的质量分数为48.5%.现代工业生产多采用联合生产,可将闪锌矿中的硫用于生产硫酸.现有
此闪锌矿100t,在理论上可生产出98.0%的硫酸50t.
(2)焙烧炉产生的炉气中SO2的体积分数不超过14.3%(保留小数点后一位小数,下同).
(3)鼓风炉容积固定,炉内部分气态物质其物质的量浓度(mol/L)变化如下:
| 时间/min | CO | Zn | CO2 |
| 0 | 0.11 | 0 | 0 |
| 2 | 0.10 | 0.01 | 0.01 |
| 3 | 0.01 | 0.10 | 0.10 |
| 4 | 0.01 | 0.10 | 0.10 |
(4)若ZnS全部转化为Zn,焙烧炉出来的N2、O2、SO2混合气体中N2占82.5%,鼓风炉中CO的转化率为62.5%,而O2无剩余,试列式计算每生产1mol Zn,应向焙烧炉和鼓风炉中鼓入新鲜空气共多少升(S.T.P)?
13.MnO2和锌是制造干电池的主要原料.
电解法生产MnO2传统的工艺主要流程为:软锰矿加煤还原焙烧;用硫酸浸出焙烧料;浸出液(主要含Mn2+)经净化后再进行电解.
90年代后期发明了生产MnO2和锌的新工艺,主要是采用软锰矿(主要成分为MnO2,含少量Al2O3和SiO2杂质)和闪锌矿(主要成分为ZnS,含少量FeS、CuS、CdS杂质)为主要原料,经过除杂后,得到含Zn2+、Mn2+离子的溶液,再通过电解同时获得MnO2和锌.简化流程框图如下(中间产物的固体部分已经略去):
 已知各种金属离子完全沉淀的pH如下表:
已知各种金属离子完全沉淀的pH如下表:
回答下列问题:
(1)步骤①中,软锰矿、闪锌矿粉与硫酸溶液共热时析出硫的反应为氧化还原反应,例如:MnO2+ZnS+2H2SO4=MnSO4+ZnSO4+S↓+2H2O,请写出MnO2在酸性溶液中分别和CuS和FeS发生反应的化学方程式:MnO2+CuS+2H2SO4=MnSO4+CuSO4+S↓+2H2O、MnO2+2FeS+6H2SO4=Fe2(SO4)3+3MnSO4+2S↓+6H2O.
(2)步骤②加入金属锌是为了回收金属,回收金属的主要成份为Cu、Cd(用化学符号表示)
(3)步骤③物质C由多种物质组成,其中含有两种固体,其中一种为MnO2,其作用是将Fe2+氧化为Fe3+
此空删去,另外一种固体物质可为Zn(OH)2.
(4)步骤④中电解过程中MnO2在阳极析出,该电极上发生的反应方程式为Mn2+-2e-+2H2O=MnO2+4H+.产品D的化学式为H2SO4,该物质对整个生产的意义是用于溶解软锰矿和闪锌矿,循环使用.
电解法生产MnO2传统的工艺主要流程为:软锰矿加煤还原焙烧;用硫酸浸出焙烧料;浸出液(主要含Mn2+)经净化后再进行电解.
90年代后期发明了生产MnO2和锌的新工艺,主要是采用软锰矿(主要成分为MnO2,含少量Al2O3和SiO2杂质)和闪锌矿(主要成分为ZnS,含少量FeS、CuS、CdS杂质)为主要原料,经过除杂后,得到含Zn2+、Mn2+离子的溶液,再通过电解同时获得MnO2和锌.简化流程框图如下(中间产物的固体部分已经略去):
 已知各种金属离子完全沉淀的pH如下表:
已知各种金属离子完全沉淀的pH如下表:| Zn2+ | Mn2+ | Fe2+ | Fe3+ | Al3+ | |
| pH | 8.0 | 10.1 | 9.0 | 3.2 | 4.7 |
(1)步骤①中,软锰矿、闪锌矿粉与硫酸溶液共热时析出硫的反应为氧化还原反应,例如:MnO2+ZnS+2H2SO4=MnSO4+ZnSO4+S↓+2H2O,请写出MnO2在酸性溶液中分别和CuS和FeS发生反应的化学方程式:MnO2+CuS+2H2SO4=MnSO4+CuSO4+S↓+2H2O、MnO2+2FeS+6H2SO4=Fe2(SO4)3+3MnSO4+2S↓+6H2O.
(2)步骤②加入金属锌是为了回收金属,回收金属的主要成份为Cu、Cd(用化学符号表示)
(3)步骤③物质C由多种物质组成,其中含有两种固体,其中一种为MnO2,其作用是将Fe2+氧化为Fe3+
此空删去,另外一种固体物质可为Zn(OH)2.
(4)步骤④中电解过程中MnO2在阳极析出,该电极上发生的反应方程式为Mn2+-2e-+2H2O=MnO2+4H+.产品D的化学式为H2SO4,该物质对整个生产的意义是用于溶解软锰矿和闪锌矿,循环使用.
3.下列属于同位素的一组是( )
| A. | O2、O3 | B. | 1H、2H+ | ||
| C. | ${\;}_{19}^{40}$K、${\;}_{20}^{40}$Ca | D. | H、D、T |
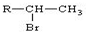 (R为烃基)
(R为烃基)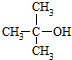 .
.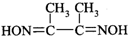 是检验Ni2+的灵敏试剂.
是检验Ni2+的灵敏试剂.