题目内容
14.下列物质中既含有共价键又含有离子键的是( )| A. | KOH | B. | MgO | C. | H2SO4 | D. | CO2 |
分析 一般金属元素与非金属元素形成离子键,非金属元素之间形成共价键,以此来解答.
解答 解:A.KOH中钾离子和氢氧根之间存在离子键,氢氧根离子中氧原子和氢原子之间存在共价键,故A正确;
B.MgO只有镁离子与氧离子形成的离子键,故B错误;
C.硫酸中只存在共价键,故C错误;
D.二氧化碳中只存在C=O共价键,故D错误;
故选:A.
点评 本题主要考查化学键,熟悉判断化学键的一般规律即可解答,题目难度不大.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
4.常温下,AgCl、AgI的溶度积常数(Ksp)依次为1.8×10-10mol2•L-2、8.3×10-17mol2•L-2.下列有关沉淀溶解平衡的说法正确的是( )
| A. | KSP(AB2)小于KSP(CD),则AB2的溶解度一定小于CD的溶解度 | |
| B. | 在氯化银的沉淀溶解平衡体系中,加入蒸馏水,氯化银的KSP增大 | |
| C. | 在氯化银的沉淀溶解平衡体系中,加入碘化钾固体,氯化银沉淀可转化为碘化银沉淀 | |
| D. | 在碳酸钙的沉淀溶解平衡体系中,加入稀盐酸,溶解平衡不移动 |
5.下列表示对应化学反应的离子方程式正确的是( )
| A. | 铜与硝酸银溶液反应:Cu+Ag+═Cu2++Ag | |
| B. | 等体积等物质的量浓度的氢氧化钡溶液与碳酸氢铵溶液混合Ba2++2OH-+NH4++HCO3-═BaCO3↓+NH3•H2O+H2O | |
| C. | 向Ca(ClO)2溶液中通入二氧化硫:Ca2++2ClO-+SO2+H2O═CaSO3↓+2HClO | |
| D. | 氯化钙溶液中通入二氧化碳气体:Ca2++CO2+H2O═CaCO3↓+2H+ |
9.下列实验操作与实验目的相对应的是( )
| 实验操作 | 实验目的 | |
| A | 苯、溴水和铁屑混合于带长导管的烧瓶中 | 制备溴苯 |
| B | 淀粉溶液水解后冷却至室温,加碘水观察现象 | 检验淀粉是否完全水解 |
| C | 向蔗糖溶液中加入适量稀硫酸,水浴加热,再加入新制的Cu(OH)2,加热至沸腾 | 检验蔗糖水解产物 |
| D | 将溴乙烷与氢氧化钠水溶液共热一段时间,再向冷却后的混合液中滴加硝酸银溶液 | 检验溴乙烷中的溴原子 |
| A. | A | B. | B | C. | C | D. | D |
19.下列能形成原电池的装置(溶液均为稀硫酸)是( )
| A. |  | B. | 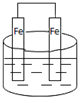 | C. |  | D. |  |
3.与H2O具有相同电子数的是( )
| A. | F | B. | O2 | C. | CH4 | D. | C2H6 |
4.检验淀粉已完全水解的试剂是( )
| A. | 新制的Cu(OH)2悬浊液 | B. | 碘水 | ||
| C. | 酸性高锰酸钾溶液 | D. | 稀硫酸 |
