题目内容
10.烃类分子中的碳原子的共用电子对数是( )| A. | 2 | B. | 3 | C. | 4 | D. | 5 |
分析 根据烃类分子中碳原子的最层电子数为4以及稳定结构来解答;
解答 解:烃类分子中每个碳原子结合4个电子形成8电子稳定结构,也就是四对共用电子,故选C.
点评 本题考查学生碳原子的成键方式,可以根据所学知识进行回答,较简单.

练习册系列答案
相关题目
20.表为元素周期表中的一部分,列出10种元素在元素周期表中的位置.试用元素符号、离子符号或化学式回答下列问题.
(1)①③⑤三种元素最高价氧化物对应水化物中,碱性最强的是NaOH;(填化学式)
(2)元素⑦的氢化物常温下和元素②的单质反应的化学方程式2K+2H2O=2KOH+H2↑;
(3)①和⑦两元素形成四核化合物的电子式 ,该物质中含有的化学键类型为离子键与共价键(或非极性键);
,该物质中含有的化学键类型为离子键与共价键(或非极性键);
(4)①的最高价氧化物对应水化物和⑤的最高价氧化物相互反应的离子方程式为Al2O3+2OH-=2AlO2-+H2O.
| ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 | |
| 2 | ⑥ | ⑦ | ||||||
| 3 | ① | ③ | ⑤ | ⑧ | ⑨ | ⑩ | ||
| 4 | ② | ④ |
(2)元素⑦的氢化物常温下和元素②的单质反应的化学方程式2K+2H2O=2KOH+H2↑;
(3)①和⑦两元素形成四核化合物的电子式
 ,该物质中含有的化学键类型为离子键与共价键(或非极性键);
,该物质中含有的化学键类型为离子键与共价键(或非极性键);(4)①的最高价氧化物对应水化物和⑤的最高价氧化物相互反应的离子方程式为Al2O3+2OH-=2AlO2-+H2O.
1.下列物质含有共价键的离子化合物是( )
| A. | NaOH | B. | NaCl | C. | N2 | D. | HCl |
18.以下化学用语正确的是( )
| A. | 苯的最简式 C6H6 | B. | 羟基的电子式 | ||
| C. | 乙烯的结构简式CH2CH2 | D. | 甲醛的结构式: |
5.某主族元素的原子,M层上有一个半充满的能级(即该能级的每个轨道只有1个电子),这种原子的质子数( )
| A. | 是11或15 | B. | 只能是15 | C. | 只能是7 | D. | 只能是11 |
2.下列物质的电子式书写正确的是( )
| A. | NaOH  | B. | H2S 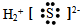 | C. | N2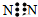 | D. | CO2 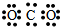 |
19.电解水时,可以加入少量电解质以增强导电性,下列物质中不宜加入的是( )
| A. | Na2SO4 | B. | NaOH | C. | HCl | D. | H2SO4 |