题目内容
17.向CuSO4和Fe2(SO4)3的混合溶液中加入一定质量的铁粉,充分反应后过滤,向滤渣中加入稀盐酸,无明显现象,下列叙述中正确的是( )| A. | 滤液中一定有Cu2+ | B. | 滤液中一定无Cu2+ | ||
| C. | 滤液中一定有Fe3+ | D. | 滤液中一定无Fe3+ |
分析 CuSO4和Fe2(SO4)3的混合溶液中加入一定质量的铁粉,由于氧化性Fe3+>Cu2+,故铁先和Fe3+反应,只有当Fe3+反应完全后,铁再和Cu2+反应,充分反应后过滤,向滤渣中加入稀盐酸,无明显现象,说明滤渣的成分是铜而不含铁,据此分析.
解答 解:CuSO4和Fe2(SO4)3的混合溶液中加入一定质量的铁粉,由于氧化性Fe3+>Cu2+,故铁先和Fe3+反应:2Fe3++Fe=3Fe2+,只有当Fe3+反应完全后,铁再和Cu2+反应:Cu2++Fe=Fe2++Cu.充分反应后过滤,向滤渣中加入稀盐酸,无明显现象,说明滤渣的成分是铜而不含铁,而既然有铜被置换出,则说明Cu2+已经和铁反应,则Fe3+已经反应完全,故溶液中一定无Fe3+,故C错误、D正确;有铜被置换出,只能说明Cu2+已经和铁反应,至于是否反应完全则无法确定,故溶液中无法确定是否还含Cu2+,故A和B均错误.
故选D.
点评 本题考查了反应的先后顺序问题,应注意的是同一种还原剂(氧化剂)在遇到不同的氧化剂(还原剂)时,会先和氧化性(还原性)强的反应.

练习册系列答案
相关题目
8.下列离子方程式书写正确的是( )
| A. | 稀盐酸滴在铜片上:Cu+2H+═Cu2++H2↑ | |
| B. | 氧化镁与稀盐酸混合:MgO+2H+═Mg2++H2O | |
| C. | 石灰石上滴加稀盐酸:CaCO3+2H+═Ca2++H2CO3 | |
| D. | 铜片插入硝酸银溶液中:Cu+Ag+═Cu2++Ag |
5.下列化学用语正确的是( )
| A. | Cl-的结构示意图: | |
| B. | 乙酸的结构示意图:C2H4O2 | |
| C. | 硫酸的电离方程式:H2SO4═H2++SO42- | |
| D. | 氯化钠的电子式: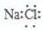 |
12.下列关于SO2性质的说法正确的是( )
| A. | 无色无味 | B. | 密度比空气小 | C. | 可与Ca(OH)2反应 | D. | 可用于漂白食品 |
2.下列关于铜电极的叙述正确的是( )
| A. | 用电解法精炼铜时,粗铜作阴极、精铜作阳极 | |
| B. | 在镀件上电镀铜时,用金属铜作阳极 | |
| C. | 在电解池中,铜作电极时,溶液中的阴离子在铜极上失电子 | |
| D. | 电解饱和食盐水制稀硫酸制Cl2、H2时,可用金属铜作阳极 |
9.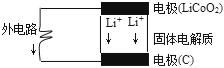 锂电池的构造如图所示,电池内部“→”表示放电时Li*的迁移方向,电池总反应可表示为:Li1-xCoO2+LixC$?_{放电}^{充电}$LiCoO2+6C,下列说法错误的是( )
锂电池的构造如图所示,电池内部“→”表示放电时Li*的迁移方向,电池总反应可表示为:Li1-xCoO2+LixC$?_{放电}^{充电}$LiCoO2+6C,下列说法错误的是( )
 锂电池的构造如图所示,电池内部“→”表示放电时Li*的迁移方向,电池总反应可表示为:Li1-xCoO2+LixC$?_{放电}^{充电}$LiCoO2+6C,下列说法错误的是( )
锂电池的构造如图所示,电池内部“→”表示放电时Li*的迁移方向,电池总反应可表示为:Li1-xCoO2+LixC$?_{放电}^{充电}$LiCoO2+6C,下列说法错误的是( )| A. | 该电池的负极为LiCoO2 | |
| B. | 电池中的固体电解质可以是熔融的氯化钠、干冰等 | |
| C. | 充电时的阴极反应:Li1-xCoO2+xLi++xe-═LiCoO2 | |
| D. | 外电路上的“→”表示放电时的电子流向 |
6.FeS2与HNO3反应后的氧化产物为Fe(NO3)3 和H2SO4,若反应中FeS2与HNO3的物质的量之比为1:8,HNO3的还原产物为( )
| A. | NO2 | B. | NO | C. | N2 O | D. | N2O3 |
7.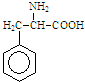 某有机物结构简式如图.一定条件下,该物质与甘氨酸(NH2-CH2-COOH)混合发生反应生成的链状二肽有( )
某有机物结构简式如图.一定条件下,该物质与甘氨酸(NH2-CH2-COOH)混合发生反应生成的链状二肽有( )
 某有机物结构简式如图.一定条件下,该物质与甘氨酸(NH2-CH2-COOH)混合发生反应生成的链状二肽有( )
某有机物结构简式如图.一定条件下,该物质与甘氨酸(NH2-CH2-COOH)混合发生反应生成的链状二肽有( )| A. | 1种 | B. | 2种 | C. | 3种 | D. | 4种 |