题目内容
下列物质属于离子晶体的是( )
| A、熔点是1070℃,固态不导电,熔融状态能导电,易溶于水 |
| B、熔点是10.31℃,液态不导电,水溶液能导电 |
| C、熔点3550℃,不溶于水,不导电 |
| D、熔点是97.80℃,质软,固态可导电,密度是0.97g?cm-3 |
考点:离子晶体
专题:化学键与晶体结构
分析:离子晶体:阴阳离子通过离子键结合形成的晶体;一般熔点较高,硬度较大、难挥发,固体不导电,但质脆,一般易溶于水,其水溶液或熔融态能导电.
解答:
解:A.离子晶体的性质:一般熔点较高,固体不导电,一般易溶于水,其水溶液或熔融态能导电,故A正确;
B.离子晶体的性质:一般熔点较高,其水溶液或熔融态能导电,故B错误;
C.离子晶体的性质:一般熔点较高,易溶于水,其水溶液或熔融态能导电,故C错误;
D.离子晶体的性质:一般熔点较高,质脆,固体不导电,其水溶液或熔融态能导电,故D错误,
故选A.
B.离子晶体的性质:一般熔点较高,其水溶液或熔融态能导电,故B错误;
C.离子晶体的性质:一般熔点较高,易溶于水,其水溶液或熔融态能导电,故C错误;
D.离子晶体的性质:一般熔点较高,质脆,固体不导电,其水溶液或熔融态能导电,故D错误,
故选A.
点评:本题考查离子晶体的性质,难度不大.要注意离子晶体一般熔点较高,硬度较大、难挥发,固体不导电,但质脆,一般易溶于水,其水溶液或熔融态能导电.

练习册系列答案
相关题目
将10.6gNa2CO3和8.4gNaHCO3的混合物溶于水配成1L溶液,关于该溶液的说法错误的是( )
| A、溶液中:C(HCO3-)>C(CO32-) |
| B、溶液中:C(Na+)+C(H+)=2C(CO32-)+C(HCO3-)+C(OH-) |
| C、溶液中:2C(H+)+C(HCO3-)+3C(H2CO3)=C(CO32-)+2C(OH-) |
| D、该溶液的碱性强于0.1mol/L的Na2CO3溶液的碱性 |
有下列原子:
Li、
Li、
Na、
Mg、
C、
N,关于这些原子的说法中正确的是( )
6 3 |
7 3 |
23 11 |
24 12 |
14 6 |
14 7 |
A、
| ||||
B、
| ||||
C、
| ||||
D、
|
下列物质的分类全部正确的是( )
| A、NO2-酸性氧化物 Mn2O7-碱性氧化物 Al2O3-两性氧化物 |
| B、油脂-纯净物 胆矾-混合物 HD-单质 |
| C、纯碱-碱 硫化氢-酸 小苏打-酸式盐 |
| D、氨气-非电解质 硫酸钡-强电解质 醋酸-弱电解质 |
下列所得溶液的物质的量浓度等于0.1mo/L的是( )
| A、将0.1mol氨气充分溶解在1L水中 |
| B、将10g质量分数为98%的硫酸与990g水混合 |
| C、将8g三氧化硫溶于水并配成1L溶液 |
| D、将0.1mol氧化钾溶于水并配成1L溶液 |
下列物质表示式正确的是( )
| A、N2的结构式:N-N |
B、Na+的电子式: |
| C、HCl的电子式:H:Cl |
D、F原子的电子式: |
已知R2+离子核外有a个电子,b个中子,表示R原子符号正确的是( )
A、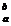 R R |
B、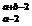 R R |
C、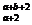 R R |
D、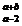 R R |