题目内容
下列物质表示式正确的是( )
| A、N2的结构式:N-N |
B、Na+的电子式: |
| C、HCl的电子式:H:Cl |
D、F原子的电子式: |
考点:电子式、化学式或化学符号及名称的综合
专题:化学用语专题
分析:A.氮气分子中存在氮氮三键,不是单键;
B.钠离子为简单阳离子,其电子式直接用离子符号表示;
C.氯化氢的电子式中应该写出氯原子最外层的3对孤电子对;
D.氟原子不带电荷,其最外层为7个电子.
B.钠离子为简单阳离子,其电子式直接用离子符号表示;
C.氯化氢的电子式中应该写出氯原子最外层的3对孤电子对;
D.氟原子不带电荷,其最外层为7个电子.
解答:
解:A.氮气分子中存在3对共用电子对,氮气的电子式为: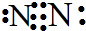 ,所以氮气的结构式为:N≡N,故A错误;
,所以氮气的结构式为:N≡N,故A错误;
B.钠离子的电子式用其离子符号表示,所以钠离子的电子式为:Na+,故B错误;
C.氯化氢分子为共价化合物,氯原子最外层达到8电子稳定结构,氯化氢的电子式为: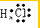 ,故C错误;
,故C错误;
D.F原子为中性,最外层7个电子,反应中的电子式为: ,故D正确;
,故D正确;
故选D.
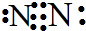 ,所以氮气的结构式为:N≡N,故A错误;
,所以氮气的结构式为:N≡N,故A错误;B.钠离子的电子式用其离子符号表示,所以钠离子的电子式为:Na+,故B错误;
C.氯化氢分子为共价化合物,氯原子最外层达到8电子稳定结构,氯化氢的电子式为:
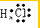 ,故C错误;
,故C错误;D.F原子为中性,最外层7个电子,反应中的电子式为:
 ,故D正确;
,故D正确;故选D.
点评:本题考查了结构式、电子式的表示方法,题目难度中等,注意掌握常见化学用语的概念及正确的表示方法,明确原子、阴阳离子的电子式的区别.

练习册系列答案
 口算题卡北京妇女儿童出版社系列答案
口算题卡北京妇女儿童出版社系列答案
相关题目
已知短周期元素的离子aA2+、bB+、cC3-、dD-都具有相同的电子层结构.则下列叙述正确的是( )
| A、原子半径 A>B>D>C |
| B、原子序数 d>c>b>a |
| C、离子半径 B>A>C>D |
| D、原子结构的最外层电子数目 D>C>A>B |
设NA为阿佛加德罗常数的数值,下列说法正确的是( )
| A、在室温下,8g甲烷含有的共价键数为NA个 |
| B、3.2g Cu与足量的浓硝酸反应生成的气体分子数为0.1NA |
| C、含有NA个中子的D2O的质量为2.0g |
| D、1mol Fe与足量的稀HNO3反应,转移2NA个电子 |
下列物质属于离子晶体的是( )
| A、熔点是1070℃,固态不导电,熔融状态能导电,易溶于水 |
| B、熔点是10.31℃,液态不导电,水溶液能导电 |
| C、熔点3550℃,不溶于水,不导电 |
| D、熔点是97.80℃,质软,固态可导电,密度是0.97g?cm-3 |
下列关于
K的说法错误的是( )
40 19 |
| A、原子核内有21个中子 |
| B、质量数为40 |
| C、核外电子数为19 |
| D、中子数为19 |
下列化学用语或模型正确的是( )
A、氯化氢的电子式: |
| B、8个中子的碳原子:12C |
C、硫离子结构示意图: |
D、CH4分子的比例模型: |
若阿伏加德罗常数的数值用NA表示,下列说法正确的是( )
| A、标准状况下,1.12L 氦气所含原子数为0.05NA |
| B、22.4 LHCl溶于水,溶液中H+数为NA |
| C、1.6gNH2-离子所含电子数为NA |
| D、10g D2O所含的中子数为4.5NA |
用NA表示阿伏加德罗常数,下列叙述中,正确的是( )
| A、常温常压下,11.2 L氯气所含的原子数为NA |
| B、常温常压下,1 molCl2与石灰乳完全反应转移电子数为NA |
| C、NA个氧分子和NA个氦分子的质量比等于4:1 |
| D、1.9 g的H3O+离子中含有的质子数为1.0 NA |
 密闭容器中mA(g)+nB(g)?pC(g),反应达到平衡,经测定增大压强P时,A的转化率随P而变化的曲线如图.则:
密闭容器中mA(g)+nB(g)?pC(g),反应达到平衡,经测定增大压强P时,A的转化率随P而变化的曲线如图.则: