题目内容
20.(1)在标准状况下,CO与CO2的混合气体共39.2L,质量为61g.则两种气体的物质的量之和为1.75mol,其中CO的体积分数是57.1%,CO2的质量分数是54.1%.(2)同温同压下的氧气和氢气,两种气体的密度之比为16:1;若质量相等,两种气体的体积之比为1:16.
分析 (1)根据体积结合n=$\frac{V}{{V}_{m}}$=$\frac{m}{M}$可列方程式组解答;
(2)同温同压下,气体摩尔体积相等,根据ρ=$\frac{M}{{V}_{m}}$知,二者的密度之比等于其摩尔质量之比;如果二者质量相等,根据V=$\frac{m}{M}$知,相同气体摩尔体积时,其体积之比等于摩尔质量的反比.
解答 解:(1)两种气体的物质的量之和为$\frac{39.2L}{22.4L/mol}$=1.75mol,
设混合气体中CO的物质的量为x,CO2的物质的量为y,
则有$\left\{\begin{array}{l}{x+y=1.75}\\{28x+44y=61}\end{array}\right.$,
解得x=1mol,y=0.75mol,
CO占总体积的体积分数即为物质的量分数,为$\frac{1mol}{1.75mol}×100%$≈57.1%,
CO2的质量分数是$\frac{0.75mol×44g/mol}{61g}×100%$=54.1%,
故答案为:1.75;57.1%;54.1%;
(2)温同压下,气体摩尔体积相等,氮气的摩尔质量是32g/mol、氢气的摩尔质量是2g/mol,根据ρ=$\frac{M}{{V}_{m}}$知,气体摩尔体积相等时,二者的密度之比等于其摩尔质量之比=32g/mol:2g/mol=16:1;
如果二者质量相等,根据V=$\frac{m}{M}$知,相同气体摩尔体积时,其体积之比等于摩尔质量的反比=2g/mol:32g/mol=1:16,
故答案为:16:1;1:16.
点评 本题考查物质的量的相关计算,为高频考点,侧重于学生的分析、计算能力的考查,注意把握相关概念的理解以及公式的运用,难度不大.

练习册系列答案
相关题目
10.下列离子方程式书写正确的是( )
| A. | 碳酸氢钙溶液中加入过量的氢氧化钠溶液:Ca2++2HCO3-+2OH-=CaCO3↓+2H2O+CO32- | |
| B. | 氯气与水的反应:Cl2+H2O=2H++Cl-+ClO- | |
| C. | 铜片跟稀硝酸反应:Cu+2NO3-+4H+═Cu2++2NO2↑+2H2O | |
| D. | 铝片和氢氧化钠溶液反应:Al+OH-+6H2O=[Al(OH)4]-+3H2↑ |
8.同周期的四种短周期元素X、Y、Z和W的原子序数依次递增,其原子的最外层电子数之和为18,X和Y的原子序数比为6:7,X的最高正价是W的最低负价绝对值的2倍.下列说法正确的是( )
| A. | Y的氧化物不能与任何酸发生反应 | |
| B. | X和W可形成离子化合物 | |
| C. | X、Y、Z和W都没有同素异形体 | |
| D. | Z和W的最高价氧化物对应的水化物都是强酸 |
15.下列有关实验操作和结论均正确的是( )
| 选项 | 操作 | 结论 |
| A | 配制FeCl2溶液时加入适量的盐酸 | 抑制Fe2+水解 |
| B | 浓硫酸和蔗糖反应产生的气体通过足量的KMnO4溶液,气体全部被吸收且溶液紫红色褪去 | “黑面包实验”产生的气体具有还原性 |
| C | 制备乙酸乙酯的实验,将蒸出的乙酸乙酯蒸汽导在饱和的NaOH溶液液面以上 | 防止倒吸,便于分层. |
| D | 幼儿使用含NaF的牙膏,可以使牙齿上的Ca5(PO4)3OH转化为Ca5(PO4)3F,防止蛀牙 | Ksp[Ca5(PO4)3F]<Ksp[Ca5(PO4)3OH] |
| A. | A | B. | B | C. | C | D. | D |
5.下列关于物质的量及粒子数的叙述,正确的是( )
| A. | 1 mol任何物质都含有6.02×1023个分子 | |
| B. | 0.012kg 12C中含有约6.02×1023个12C | |
| C. | 1mol CO2中含有1mol碳和2 mol氧 | |
| D. | 1mol H含有6.02×1024个质子 |
7.在一定温度下,将气体X和气体Y 各0.16mol充入10L 恒容密闭容器中,发生反应X(g)+Y(g)?2Z(g)△H<0,反应过程中测定的数据如表( )
下列判断正确的是( )
| t/min | 2 | 4 | 7 | 9 |
| n(Y)/mol | 0.12 | 0.11 | 0.10 | 0.10 |
| A. | 反应前2min的平均速率v(Z)=2.0×10-3 mol/(L•min) | |
| B. | 其他条件不变,降低温度,平衡向正反应方向移动 | |
| C. | 当进行4分钟时,反应已达平衡状态 | |
| D. | 其他条件不变,通过缩小容器体积增大压强,平衡常数减小 |
4.观察下列模型并结合相关信息,判断下列说法中不正确的是( )
| B12结构单元 | SF6 | S8 | HCN |
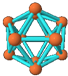 | 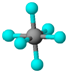 | 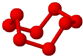 | 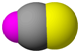 |
| 熔点1873K | 气体 | 易溶于CS2 | 溶液显弱酸性 |
| A. | 单质B12形成的晶体可能为原子晶体 | |
| B. | SF6是由极性键构成的非极性分子 | |
| C. | S8和HCN形成晶体后,晶体类型相同 | |
| D. | HCN形成晶体后,晶体中的作用力只有共价键 |
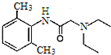 )是一种局部麻醉药物,可由下列路线合成:
)是一种局部麻醉药物,可由下列路线合成: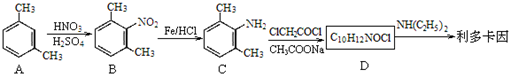
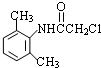 .
.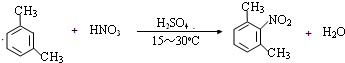 .
.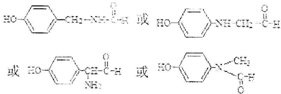 .
.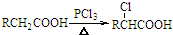 ,写出以苯和乙醇为原料制备
,写出以苯和乙醇为原料制备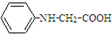 的合成路线流程图(无机试剂任选).合成路线流程图示例如下:H2C=CH2$\stackrel{HBr}{→}$CH3CH2Br$→_{△}^{NaOH溶液}$CH3CH2OH.
的合成路线流程图(无机试剂任选).合成路线流程图示例如下:H2C=CH2$\stackrel{HBr}{→}$CH3CH2Br$→_{△}^{NaOH溶液}$CH3CH2OH.