题目内容
14.下列溶液一定呈中性的是( )| A. | c(H+)=1×10-7mol•L-1的溶液 | |
| B. | pH=pOH 的溶液 | |
| C. | pH=14-pOH 的溶液 | |
| D. | 浓度均为0.1 mol•L-1的一元酸与氢氧化钠溶液等体积混合 |
分析 溶液的酸碱性是根据溶液中氢离子浓度和氢氧根离子浓度的相对大小判断的,
当溶液中氢离子浓度大于氢氧根离子浓度时,溶液呈酸性;
当氢离子浓度和氢氧根离子浓度相等时,溶液呈中性;
当溶液中氢氧根离子浓度大于氢离子浓度时,溶液呈碱性,
注意不能根据溶液的PH值大小判断.
解答 解:A、(H+)=10-7mol•L-1的溶液,溶液的PH=7,PH=7的溶液不一定呈中性,如100℃时,水的离子积常数是10-12,当PH=6时溶液呈中性,当PH=7时溶液呈碱性,故A错误;
B、pH=pOH 的溶液中C(H+)=C(OH-),溶液一定呈中性,故B正确;
C、pH=14-pOH 的溶液,pH+pOH=14,只能说明水的离子积常数是10-14,此时溶液可能是酸性,碱性或者中性,故C错误;
D、浓度均为0.1 mol•L-1的一元酸与氢氧化钠溶液等体积混合,二者恰好完全反应,酸若为强酸显中性,酸若为弱酸显碱性,故D错误,
故选:B.
点评 本题考查了溶液酸碱性的分析判断,盐类水解的应用,溶液中水的离子积常数随温度变化,题目较简单.

练习册系列答案
相关题目
5.下列叙述中正确的是( )
| A. | 由非金属元素组成的化合物中一定不含离子键 | |
| B. | 离子化合物一定含有金属元素 | |
| C. | 分子中一定含有共价键 | |
| D. | 某种离子化合物可以同时含有离子键、极性共价键 |
2.以下实验能获得成功的是( )
| A. | 用酸性KMnO4溶液鉴别乙烯和乙炔 | |
| B. | 将铁屑、液溴、苯混合制溴苯 | |
| C. | 苯和溴苯采用分液的方法分离 | |
| D. | 溴乙烷中滴入AgNO3溶液检验其中的溴元素:Br-+Ag+═AgBr↓ |
6.将淀粉和淀粉酶的混合物放入玻璃纸袋中,扎好袋口,浸入流动的温水中.相当一段时间后,取袋内液体分别与碘水、新制Cu(OH)2(加热)作用,其现象分别是( )
| A. | 显蓝色、无现象 | B. | 显蓝色、红色沉淀 | ||
| C. | 无现象、变黑色 | D. | 无现象、红色沉淀 |
3.石油分馏是石油综合利用的重要环节,下列有关石油分馏的说法正的是( )
| A. | 石油分馏是利用加热的方法将石油分成不同沸点产物的方法 | |
| B. | 石油分馏得到的分馏产物仍是一些混合物 | |
| C. | 石油分馏可以得到石油气、汽油、煤气、乙烯和丙烯等产品 | |
| D. | 石油分馏过程是加热条件下发生的化学变化 |
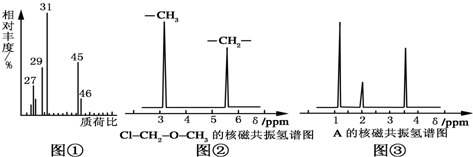
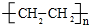 .
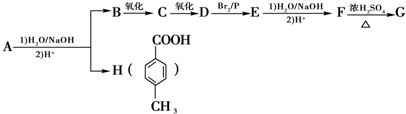
.
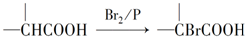
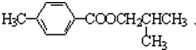 .
.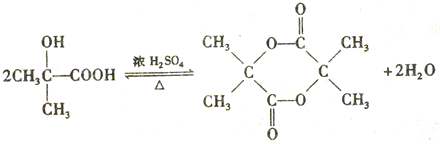 .
.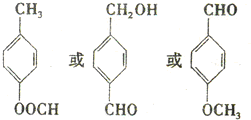 .
. )结构.
)结构.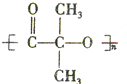 ,形成该聚合物的反应类型为:缩聚反应.
,形成该聚合物的反应类型为:缩聚反应.