题目内容
9.表中列出了有关晶体的说明,有错误的是( )| 选项 | A | B | C | D |
| 晶体名称 | 碘化钾 | 干冰 | 硫 | 碘 |
| 晶体中的微粒名称 | 阴、阳离子 | 分子 | 原子 | 分子 |
| 晶体内存在的结合力 | 离子键 | 范德华力 | 共价键 | 范德华力 |
| A. | A | B. | B | C. | C | D. | D |
分析 离子晶体是阴、阳离子通过离子键形成的晶体;
原子晶体是原子之间通过共价键形成的晶体;
分子晶体是分子间通过分子间作用力(包括范德华力和氢键)构成的晶体;
据此分析.
解答 解:A、碘化钾属于离子晶体,有阴阳离子通过离子键结合,故A正确;
B、干冰属于分子晶体,分子间通过范德华力结合,故B正确;
C、硫属于分子晶体,构成微粒为分子,晶体中存在共价键和范德华力,故C错误;
D、碘属于分子晶体,分子间通过范德华力结合,故D正确;
故选C.
点评 本题考查晶体类型判断,难度不大,掌握各种类型晶体的构成键微粒、作用力即可解答.

练习册系列答案
 中考利剑中考试卷汇编系列答案
中考利剑中考试卷汇编系列答案 教育世家状元卷系列答案
教育世家状元卷系列答案 黄冈课堂作业本系列答案
黄冈课堂作业本系列答案 单元加期末复习先锋大考卷系列答案
单元加期末复习先锋大考卷系列答案
相关题目
19.下列五种烃①2-甲基丁烷②2,2-二甲基丙烷③戊烷④丙烷⑤丁烷,按沸点由高到低的顺序排列的是( )
| A. | ①>②>③>⑤>④ | B. | ②>③>⑤>④>① | C. | ③>①>②>⑤>④ | D. | ④>⑤>②>①>③ |
20. 一定温度下,在2L的密闭容器中,A、B、D三种气体的物质的量随时间变化的曲线如图所示.下列表述正确的是( )
一定温度下,在2L的密闭容器中,A、B、D三种气体的物质的量随时间变化的曲线如图所示.下列表述正确的是( )
 一定温度下,在2L的密闭容器中,A、B、D三种气体的物质的量随时间变化的曲线如图所示.下列表述正确的是( )
一定温度下,在2L的密闭容器中,A、B、D三种气体的物质的量随时间变化的曲线如图所示.下列表述正确的是( )| A. | 反应的化学方程式为A(g)+B(g)?D(g) | |
| B. | 反应开始到10s,用B表示的反应速率为0.079mol/(L•s) | |
| C. | 在10s时,D的体积分数为71.8% | |
| D. | 反应开始到10s时,A的转化率为79% |
17.下列说法正确的是( )
| A. | 含C=C的物质一定是烯烃 | B. | 最简式为C3H6的物质一定是丙烯 | ||
| C. | CH≡CCH2Cl属于不饱和烃 | D. | 烯烃中一定含C=C |
4.下表为烯类化合物与溴发生加成反应的相对速率(以乙烯为标准).
(1)下列化合物与氯化氢加成时,取代基对速率的影响与表中规律类似,其中反应速率最快的是A(填序号).
A.(CH3)2C=C(CH3)2 B.CH3CH=CHCH2CH3
C.CH2=CH CH3 D.CH2=CHCl
(2)烯烃与溴化氢、水加成时,产物有主次之分,例如:
CH2=CHCH3+HBr→CH3CHBrCH3+CH3CH2Br
(主要产物)(次要产物)
请写出 与HBr反应的主要产物的结构简式
与HBr反应的主要产物的结构简式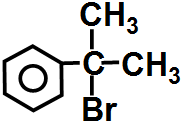 .
.
| 烯类化合物 | 相对速率 |
| (CH3)2C=CHCH3 | 10.4 |
| CH3CH=CH2 | 2.03 |
| CH2=CH2 | 1.00 |
| CH2=CHBr | 0.04 |
A.(CH3)2C=C(CH3)2 B.CH3CH=CHCH2CH3
C.CH2=CH CH3 D.CH2=CHCl
(2)烯烃与溴化氢、水加成时,产物有主次之分,例如:
CH2=CHCH3+HBr→CH3CHBrCH3+CH3CH2Br
(主要产物)(次要产物)
请写出
 与HBr反应的主要产物的结构简式
与HBr反应的主要产物的结构简式 .
.
14.下列溶液一定呈中性的是( )
| A. | c(H+)=1×10-7mol•L-1的溶液 | |
| B. | pH=pOH 的溶液 | |
| C. | pH=14-pOH 的溶液 | |
| D. | 浓度均为0.1 mol•L-1的一元酸与氢氧化钠溶液等体积混合 |
1.研究有机物一般经过以下几个基本步骤:分离、提纯→确定最简式→确定分子式→确定结构式,以下用于研究有机物的方法错误的是( )
| A. | 蒸馏常用于分离提纯液态有机混合物 | |
| B. | 燃烧法是研究确定有机物成分的有效方法 | |
| C. | 1H核磁共振谱通常用于分析有机物的相对分子质量 | |
| D. | 对有机物分子红外光谱图的研究有助于确定有机物分子中的官能团 |
