题目内容
10.下列反应中,反应后固体质量一定减少的是( )| A. | 铝与V2O5发生铝热反应 | B. | 镁粉投入到FeCl3溶液中 | ||
| C. | 碳粉与CuO混合物在试管中加热 | D. | 水蒸气通入足量Na2O2粉末 |
分析 A.铝与V2O5发生铝热反应,反应前后都是固体,固体质量不变;
B.如果镁粉过量,则反应生成铁,根据关系式3Mg~2Fe判断;
C.碳与氧化铜反应生成一氧化碳气体和铜,反应后固体质量一定减少;
D.水蒸气与过氧化钠反应生成氢氧化钠和氧气,过氧化钠转化成氢氧化钠,固体质量一定增加.
解答 解:A.Al与V2O5反应生成Al2O3和V,反应前固体为V2O5、Al,反应后固体为氧化铝、V,均为固体,固体质量不变,故A错误;
B.镁粉投入到FeCl3溶液中,如果镁足量,根据关系式3Mg~2Fe,固体质量变化为:72→112,反应后固体质量增加,故B错误;
C.碳粉与CuO混合物在试管中加热,反应物都是固体,反应后生成了CO气体,则固体质量一定减少,故C正确;
D.水蒸气通入足量Na2O2粉末,反应前固体为Na2O2,反应后固体为氢氧化钠,反应后的固体中增加了H元素,故D错误;
故选C.
点评 本题考查了混合物反应的计算和判断,题目难度中等,明确常见物质的性质及发生反应原理为解答关键,A为易错点,注意反应物、生成物都是固体,反应前后固体质量不变.

练习册系列答案
 寒假大串联黄山书社系列答案
寒假大串联黄山书社系列答案 寒假创新型自主学习第三学期寒假衔接系列答案
寒假创新型自主学习第三学期寒假衔接系列答案
相关题目
20.已知:2H2(g)+O2(g)=2H2O(l)△H=-571.6kJ/mol
C3H8(g)+5O2(g)=3CO2(g)+4H2O(l)△H=-2220kJ/mol
7molH2与C3H8混合物完全燃烧,共放热5869kJ,则二者的体积比V(H2):V(C3H8)为( )
C3H8(g)+5O2(g)=3CO2(g)+4H2O(l)△H=-2220kJ/mol
7molH2与C3H8混合物完全燃烧,共放热5869kJ,则二者的体积比V(H2):V(C3H8)为( )
| A. | 1:1 | B. | 2:5 | C. | 3:4 | D. | 5:2 |
1.用NA表示阿伏加德罗常数的值,下列说法正确的是( )
| A. | 常温常压下,16gO2中含有的氧分子数为NA | |
| B. | 1molOH-中含有的电子数为10NA | |
| C. | 标准状况下,11.2LH2O中含有的氢原子数为NA | |
| D. | 1mol/LBaCl2溶液中含有的钡离子数为NA |
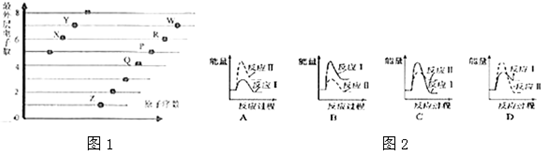
5. X、Y、Z、W、R、T是元素周期表前四周期常见元素,且原子序数依次增大,其相关信息如下表:
X、Y、Z、W、R、T是元素周期表前四周期常见元素,且原子序数依次增大,其相关信息如下表:
请用化学用语填空:
(1)R位于元素周期表第三周期第ⅥA族;T的基态原子核外电子排布式为1s22s22p63s23p63d54s1.
(2)用“>”或“<”填空:
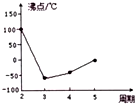
(3)在加热的条件下单质X可与R的浓的最高价氧化物的水化物反应,写出该反应的化学方程式并标出电子转移的方向和数目 (或
(或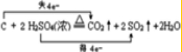 ).
).
(4)Y及其同主族元素的氢化物沸点变化趋势如图所示,其中Y的氢化物沸点最高的原因是水分子间可以形成氢键,大大加强了分子间作用力,从而使水的沸点最高.
(5)在101KPa、25℃下,由最稳定单质生成1mol该化合物是的热效应称为该化合物的标准生成焓(△H).已知Z2O3标准生成焓(△H)为:△H=-399.09kJ/mol,T2O3的标准生成焓(△H)为:△H=-269.70kJ/mol,试写出单质Z和T2O3反应的热化学方程式2Al(s)+Cr2O3(s)=2Cr+Al2O3(s)△H=-129.39kJ/mol.
 X、Y、Z、W、R、T是元素周期表前四周期常见元素,且原子序数依次增大,其相关信息如下表:
X、Y、Z、W、R、T是元素周期表前四周期常见元素,且原子序数依次增大,其相关信息如下表:| 元素 | 相关信息 |
| X | 元素最高正价与最低负价的绝对值相等 |
| Y | 是地壳中含量最多的元素 |
| Z | 元素基态原子3p能级只有一个电子 |
| W | 与Z位于同周期,能量最高的p 能级电子为半充满 |
| R | 单质为黄色固体,常存在于火山喷发口 |
| T | 元素基态原子核未成对电子最多 |
(1)R位于元素周期表第三周期第ⅥA族;T的基态原子核外电子排布式为1s22s22p63s23p63d54s1.
(2)用“>”或“<”填空:
| 第一电离能 | 离子半径 | 离子还原性 | 最高价氧化物的熔点 |
| W>R | Y>Z | Y<R | X<Z |
 (或
(或 ).
).(4)Y及其同主族元素的氢化物沸点变化趋势如图所示,其中Y的氢化物沸点最高的原因是水分子间可以形成氢键,大大加强了分子间作用力,从而使水的沸点最高.
(5)在101KPa、25℃下,由最稳定单质生成1mol该化合物是的热效应称为该化合物的标准生成焓(△H).已知Z2O3标准生成焓(△H)为:△H=-399.09kJ/mol,T2O3的标准生成焓(△H)为:△H=-269.70kJ/mol,试写出单质Z和T2O3反应的热化学方程式2Al(s)+Cr2O3(s)=2Cr+Al2O3(s)△H=-129.39kJ/mol.
2.有机物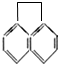 的一氯代物共有(不考虑立体异构)( )
的一氯代物共有(不考虑立体异构)( )
 的一氯代物共有(不考虑立体异构)( )
的一氯代物共有(不考虑立体异构)( )| A. | 3种 | B. | 4种 | C. | 5 种 | D. | 7种 |
14.下列化学用语使用正确的是( )
| A. | 四氯化碳的电子式 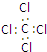 | B. | 乙炔的最简式 CH≡CH | ||
| C. | 聚乙烯的结构简式为 CH2=CH2 | D. | 丙烷的分子结构模型示意图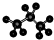 |