题目内容
15.化工生产中常用MnS做沉淀剂除去工业废水中的Cu2+:Cu2+(aq)+MnS(s)═CuS(s)+Mn2+(aq)下列有关叙述中正确的是( )
①MnS的Ksp大于CuS的Ksp
②达到平衡时c(Mn2+)=c(Cu2+)
③溶液中加入少量Na2S固体后,溶液中c(Cu2+)、c(Mn2+)保持不变
④该反应平衡常数K=$\frac{{K}_{sp}(MnS)}{{K}_{SP}(CuS)}$.
| A. | ①④ | B. | ②③ | C. | ①②③ | D. | ②③④ |
分析 ①根据分子式相似的分子,溶度积大的沉淀可以转化为溶度积小的沉淀;
②该反应达到平衡时离子的浓度不变;
③增大硫离子的浓度平衡左移;
④反应的平衡常数K=$\frac{c(M{n}^{2+})}{c(C{u}^{2+})}$=$\frac{c(M{n}^{2+})×c({S}^{2-})}{c(C{u}^{2+})c({S}^{2-})}=\frac{Ksp(MnS)}{Ksp(CuS)}$.
解答 解:①分子式相似的分子,溶度积大的沉淀可以转化为溶度积小的沉淀,所以MnS的Ksp比CuS的Ksp大,故正确;
②该反应达到平衡时各离子的浓度保持不变,但不一定相等,故错误;
③增大硫离子的浓度,平衡左向移动,所以c(Cu2+)、c(Mn2+)均减小,故错误;
④反应的平衡常数K=$\frac{c(M{n}^{2+})}{c(C{u}^{2+})}$=$\frac{c(M{n}^{2+})×c({S}^{2-})}{c(C{u}^{2+})c({S}^{2-})}=\frac{Ksp(MnS)}{Ksp(CuS)}$,故正确; 故选A.
点评 本题主要考查了沉淀的平衡以及转化,难度不大,根据平衡移动原理以及沉淀转化的知识即可完成.

练习册系列答案
相关题目
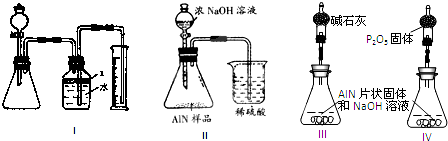
5.某研究性学习小组对过量炭粉与氧化铁反应的气体产物成分进行研究.

设计方案如图1,将一定量的氧化铁在隔绝空气的条件下与过量炭粉完全反应,测定参加反应的碳元素与氧元素的质量比.
(1)查阅资料:
①氮气不与炭粉、氧化铁发生反应.实验室可以用氯化铵饱和溶液和亚硝酸钠(NaNO2)饱和溶液混合加热制得氮气.写出该反应的离子方程式:NH4++NO2-$\frac{\underline{\;\;△\;\;}}{\;}$N2↑+2H2O.
②使上述制得的气体通过B装置方能获得干燥的N2
(2)实验步骤:
①按图2连接装置,并检查装置的气密性,称取3.20g氧化铁、2.00g炭粉混合均匀,放入48.48g的硬质玻璃管中;
②加热前,先通一段时间纯净干燥的氮气;
③停止通入N2后,夹紧弹簧夹,加热一段时间,澄清石灰水(足量)变浑浊;
④待反应结束,再缓缓通入一段时间的氮气.冷却至室温,称得硬质玻璃管和固体总质量为52.24g;
⑤过滤出石灰水中的沉淀,洗涤、烘干后称得质量为2.00g.步骤②、④中都分别通入N2,其作用分别为步骤②通入氮气的目的是排除装置中的O2;步骤④通入氮气的目的是将生成的CO2全部通入澄清的石灰水中.
(3)数据处理:
①试根据实验数据分析,该反应的气体产物是CO2和CO,理由是过量炭粉与二氧化碳气体反应生成CO气体
②写出该实验中氧化铁与炭粉发生反应的化学方程式:2C+Fe2O3 $\frac{\underline{\;高温\;}}{\;}$2Fe+CO↑+CO2↑.
(4)实验优化:学习小组有同学认为应对实验装置进一步完善.
①甲同学认为:应将澄清石灰水换成Ba(OH)2溶液,其理由是将澄清的石灰水换成Ba(OH)2溶解度大,浓度大,使CO2被吸收更完全;碳酸钡的相对原子质量大于碳酸钙的,称量时相对误差小.
②pC类似pH,是指极稀溶液中溶质物质的量浓度的常用对数负值.如某溶液溶质的浓度为:1×10-3mol/L,则该溶液中该溶质的pC=-lg1×10-3=3.现向0.2mol/LBa(OH)2溶液中通入CO2气体,沉淀开始产生时,溶液中CO32-的PC值为7.6(已知:lg2=0.2;Ksp(BaCO3)=5.0x10-9)
③从环境保护的角度,请你再提出一个优化方案将此实验装置进一步完善:在尾气出口处加一点燃的酒精灯.

设计方案如图1,将一定量的氧化铁在隔绝空气的条件下与过量炭粉完全反应,测定参加反应的碳元素与氧元素的质量比.
| TiCl4 | Mg | MgCl2 | Ti | |
| 熔点/℃ | -25.0 | 648.8 | 714 | 1667 |
| 沸点/℃ | 136.4 | 1090 | 1412 | 3287 |
①氮气不与炭粉、氧化铁发生反应.实验室可以用氯化铵饱和溶液和亚硝酸钠(NaNO2)饱和溶液混合加热制得氮气.写出该反应的离子方程式:NH4++NO2-$\frac{\underline{\;\;△\;\;}}{\;}$N2↑+2H2O.
②使上述制得的气体通过B装置方能获得干燥的N2
(2)实验步骤:
①按图2连接装置,并检查装置的气密性,称取3.20g氧化铁、2.00g炭粉混合均匀,放入48.48g的硬质玻璃管中;
②加热前,先通一段时间纯净干燥的氮气;
③停止通入N2后,夹紧弹簧夹,加热一段时间,澄清石灰水(足量)变浑浊;
④待反应结束,再缓缓通入一段时间的氮气.冷却至室温,称得硬质玻璃管和固体总质量为52.24g;
⑤过滤出石灰水中的沉淀,洗涤、烘干后称得质量为2.00g.步骤②、④中都分别通入N2,其作用分别为步骤②通入氮气的目的是排除装置中的O2;步骤④通入氮气的目的是将生成的CO2全部通入澄清的石灰水中.
(3)数据处理:
①试根据实验数据分析,该反应的气体产物是CO2和CO,理由是过量炭粉与二氧化碳气体反应生成CO气体
②写出该实验中氧化铁与炭粉发生反应的化学方程式:2C+Fe2O3 $\frac{\underline{\;高温\;}}{\;}$2Fe+CO↑+CO2↑.
(4)实验优化:学习小组有同学认为应对实验装置进一步完善.
①甲同学认为:应将澄清石灰水换成Ba(OH)2溶液,其理由是将澄清的石灰水换成Ba(OH)2溶解度大,浓度大,使CO2被吸收更完全;碳酸钡的相对原子质量大于碳酸钙的,称量时相对误差小.
②pC类似pH,是指极稀溶液中溶质物质的量浓度的常用对数负值.如某溶液溶质的浓度为:1×10-3mol/L,则该溶液中该溶质的pC=-lg1×10-3=3.现向0.2mol/LBa(OH)2溶液中通入CO2气体,沉淀开始产生时,溶液中CO32-的PC值为7.6(已知:lg2=0.2;Ksp(BaCO3)=5.0x10-9)
③从环境保护的角度,请你再提出一个优化方案将此实验装置进一步完善:在尾气出口处加一点燃的酒精灯.
6.化学在生产和生活中有着重要的作用,下列有关说法不正确的是( )
| A. | 铝需经过特别处理能具有抗腐蚀能力 | |
| B. | “地沟油”经过加工处理可用来制肥皂 | |
| C. | 嫦娥系列卫星中使用的碳纤维,是一种新型无机非金属材料 | |
| D. | 只要符合限量,“食用色素”、“亚硝酸盐”可以作为某些食品的添加剂 |
3. 在密闭容器中,1molH2与1molCO发生反应:CO(g)+2H2(g)?CH3OH(g),△H<0,反应达到平衡时,改变温度(T)和压强(P),反应混合物中甲醇的物质的量分数变化情况如图所示,下列说法正确的是( )
在密闭容器中,1molH2与1molCO发生反应:CO(g)+2H2(g)?CH3OH(g),△H<0,反应达到平衡时,改变温度(T)和压强(P),反应混合物中甲醇的物质的量分数变化情况如图所示,下列说法正确的是( )
 在密闭容器中,1molH2与1molCO发生反应:CO(g)+2H2(g)?CH3OH(g),△H<0,反应达到平衡时,改变温度(T)和压强(P),反应混合物中甲醇的物质的量分数变化情况如图所示,下列说法正确的是( )
在密闭容器中,1molH2与1molCO发生反应:CO(g)+2H2(g)?CH3OH(g),△H<0,反应达到平衡时,改变温度(T)和压强(P),反应混合物中甲醇的物质的量分数变化情况如图所示,下列说法正确的是( )| A. | P1<P2<P3<P4 | |
| B. | T1<T2<T3<T4 | |
| C. | T4和P1状态下,H2的平衡转化率为8/9 | |
| D. | 甲醇的物质的量分数越小,反应的平衡常数越小 |
10.下列反应中,反应后固体质量一定减少的是( )
| A. | 铝与V2O5发生铝热反应 | B. | 镁粉投入到FeCl3溶液中 | ||
| C. | 碳粉与CuO混合物在试管中加热 | D. | 水蒸气通入足量Na2O2粉末 |
20.近年来,乳酸成为研究热点之一,以乳酸为原料制成的高分子材料具有生物兼容性.已知乳酸的结构简式为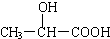 ,下列物质中能与乳酸反应的是( )
,下列物质中能与乳酸反应的是( )
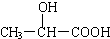 ,下列物质中能与乳酸反应的是( )
,下列物质中能与乳酸反应的是( )| A. | 金属铁 | B. | NH4Cl溶液 | C. | 乙烷 | D. | 苯 |
18.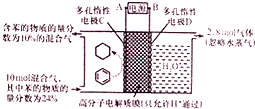 一定条件,如图所示装置可实现有机物的电化学储氢(忽略其他有机物).下列说法中不正确的是( )
一定条件,如图所示装置可实现有机物的电化学储氢(忽略其他有机物).下列说法中不正确的是( )
 一定条件,如图所示装置可实现有机物的电化学储氢(忽略其他有机物).下列说法中不正确的是( )
一定条件,如图所示装置可实现有机物的电化学储氢(忽略其他有机物).下列说法中不正确的是( )| A. | 导线中电子转移方向为C到A | |
| B. | 阳极生成2.8mol气体时,转移电子为11.2mol | |
| C. | 生成目标产物的电极反应式为C6H6+6H++6e-=C6H12 | |
| D. | 该储氢装置的电流效率η=64.3%(η=$\frac{生成目标产物消耗的电子数}{转移的电子总数}$×100%) |
19.用NA表示阿伏加德罗常数的值.下列叙述正确的是( )
| A. | 标准状况下,5.6L四氯化碳含有的分子数为0.25NA | |
| B. | 2.8g[CH2 CH2]n 中含有的碳原子数为0.2NA | |
| C. | 1mol苯分子中含有C=C双键数为3NA | |
| D. | 乙烷和丙烯的物质的量共1mol,完全燃烧生成水分子数为3NA |