题目内容
11.下列物质不能直接化合得到的是( )| A. | FeCl2 | B. | Na2S | C. | Fe(OH)3 | D. | CuS |
分析 A.铁和氯化铁反应生成氯化亚铁;
B.钠和S反应生成Na2S;
C.氢氧化亚铁和氧气、水反应生成氢氧化铁;
D.Cu与S反应生成Cu2S.
解答 解:A.Fe+2FeCl3=3FeCl2,所以能通过化合反应制得,故A不选;
B.钠和S反应生成Na2S,所以能通过化合反应制得,故B不选;
C.Fe(OH)2与氧气、水反应生成Fe(OH)3,反应方程式为:4Fe(OH)2+O2+2H2O═4Fe(OH)3,故C不选;
D.Cu与S发生化合反应直接生成Cu2S,不能生成CuS,故D选.
故选D.
点评 本题考查了物质间的反应,明确物质的性质是解本题关键,根据物质间的性质来分析解答,要熟练掌握元素化合物知识,灵活运用知识解答,题目难度不大.

练习册系列答案
 新活力总动员暑系列答案
新活力总动员暑系列答案 龙人图书快乐假期暑假作业郑州大学出版社系列答案
龙人图书快乐假期暑假作业郑州大学出版社系列答案
相关题目
2. 将镁片、铝片平行插入到一定浓度的NaOH溶液中,用导线连接成闭合回路,该装置在工作时,下列叙述正确的是( )
将镁片、铝片平行插入到一定浓度的NaOH溶液中,用导线连接成闭合回路,该装置在工作时,下列叙述正确的是( )
 将镁片、铝片平行插入到一定浓度的NaOH溶液中,用导线连接成闭合回路,该装置在工作时,下列叙述正确的是( )
将镁片、铝片平行插入到一定浓度的NaOH溶液中,用导线连接成闭合回路,该装置在工作时,下列叙述正确的是( )| A. | 镁比铝活泼,镁失去电子被氧化成Mg2+ | |
| B. | 铝是电池负极,开始工作时溶液中会立即有白色沉淀生成 | |
| C. | 该装置的内、外电路中,均是电子的定向移动形成电流 | |
| D. | 该装置开始工作时,铝片表面的氧化膜可不必处理 |
6.若溶液中由水电离产生的c(OH-)=1×10-14 mol•L-1,满足此条件的溶液中一定可以大量共存的离子组是( )
| A. | Al3+ Na+ NO3- Cl- | B. | K+ Na+ Cl- NO3- | ||
| C. | K+ Na+ Cl- AlO2- | D. | K+ NH4+ SO42- NO3- |
16.下列分离或提纯物质的说法正确的是( )
| A. | 过滤,可以除去NaCl溶液中少量的淀粉胶体 | |
| B. | 溶解、过滤,可以提纯含少量BaSO4的BaCO3 | |
| C. | 加热蒸发,可以除去粗盐中的CaCl2、MgCl2等杂质 | |
| D. | 加入足量铁屑,充分反应后,过滤,可以除去FeCl2溶液中少量FeCl3 |
3.NA代表阿伏加德罗常数,下列说法正确的是( )
| A. | 9gD2O 中含有的电子数为 5NA | |
| B. | 92gNO2和 N2O4混合气体中含有原子数为 6NA | |
| C. | 1molC3H8分子中共价键总数为 8 NA | |
| D. | 65 g Zn 全部溶解在一定浓度的硝酸溶液中,有NO生成,则转移的电子数为 NA |
20.下表中的数据是破坏1mol物质中的化学键所消耗的能量(kJ)
在一定条件下,1mol H2与1mol Cl2反应生成2mol HCl的能量变化为( )
| 物质 | Cl2 | Br2 | I2 | HCl | HBr | HI | H2 |
| 能量(kJ) | 243 | 193 | 151 | 431 | 366 | 298 | 436 |
| A. | 放出248 kJ 热量 | B. | 吸收248 kJ 热量 | C. | 放出183kJ热量 | D. | 吸收183 kJ热量 |
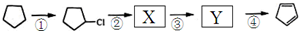

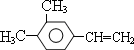 (任写一种).金刚烷与四氢二聚环戊二烯的关系是B.(填字母)
(任写一种).金刚烷与四氢二聚环戊二烯的关系是B.(填字母)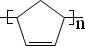 ..
.. .请写出下列反应的有机产物的结构简式:
.请写出下列反应的有机产物的结构简式: OHC-CHO、OHC-CH2-CHO.
OHC-CHO、OHC-CH2-CHO. A、B、C、D、E为周期表中原子序数依次递增的前四周期元素.
A、B、C、D、E为周期表中原子序数依次递增的前四周期元素.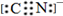 ,
,