题目内容
16.关于3C+SiO2 $\frac{\underline{\;高温\;}}{\;}$ SiC+2CO↑,下列说法正确的是( )| A. | SiC是氧化产物 | |
| B. | 还原剂与氧化剂的物质的量之比为1:2 | |
| C. | C 既是氧化剂又是还原剂 | |
| D. | 若生成4.48L CO,则转移0.4 mol 电子 |
分析 反应3C+SiO2 $\frac{\underline{\;高温\;}}{\;}$ SiC+2CO↑中,Si元素化合价没有发生变化,C元素化合价分别由0价升高为+2价和降低为-4价,则C既是氧化剂又是还原剂;氧化产物为CO,SiC为还原产物,以此解答该题.
解答 解:A.生成SiC,C元素化合价降低,则SiC为还原产物,故A错误;
B.C既是氧化剂又是还原剂,由方程式可知3molC参加反应,有2mol被氧化,1mol被还原,则在反应中还原剂和氧化剂的物质的量之比为2:1,故B错误;
C.C元素化合价分别由0价升高为+2价和降低为-4价,则C既是氧化剂又是还原剂,故C正确;
D.CO存在的条件未知,不能确定物质的量,故D错误.
故选C.
点评 本题考查了氧化还原反应,题目难度不大,明确氧化还原反应的实质、特征为解答关键,注意掌握氧化剂与还原剂、氧化产物与还原产物的概念及判断方法,试题培养了学生的分析、理解能力及化学计算能力.

练习册系列答案
 全能测控一本好卷系列答案
全能测控一本好卷系列答案
相关题目
6.下列有关NO2的说法正确的是( )
| A. | NO2可由N2与O2反应直接制备 | |
| B. | NO2有毒,但因其易溶于水且与水反应,因此不属于大气污染物 | |
| C. | NO2既有氧化性也有还原性 | |
| D. | NO2为红棕色气体,因此将NO2通入水中,溶液显红棕色 |
7.在下列各溶液中,离子一定能大量共存的是( )
| A. | 强碱性溶液中:K+、Cu2+、Cl-、SO42- | |
| B. | 含有0.1 mol•L-1 Fe3+的溶液中:K+、Ba2+、OH-、NO3- | |
| C. | 含有0.1 mol•L-1 Ca2+酸溶液中:Na+、K+、CO32-、Cl- | |
| D. | 室温下,强酸性溶液中:Na+、Fe3+、NO3-、SO42- |
4.工业上常用二氧化硫来漂白纸浆、丝毛、草帽等,此外二氧化硫还能够抑制霉菌和细菌的滋生,可以用作食物和干果的防腐剂.但必须严格按照国家有关范围和标准使用,我国规定葡萄酒中SO2的最大使用量为0.25g/L.某化学兴趣小组制备并对SO2的化学性质和用途进行探究,探究过程实验装置如图,夹持仪器省略.
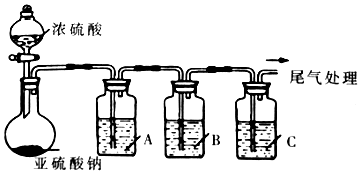
(1)实验可选用的实验试剂有浓硫酸、Na2SO3固体、Na2S溶液、BaCl2溶液、FeCl3溶液、品红溶液等.
①请完成下列表格
②A中发生反应的离子方程式为2Fe3++SO2+2H2O=2Fe2++4H++SO42-.
③在上述装置中通入过量的SO2,为了验证A中发生了氧化还原反应,取A中溶液分成两份,并设计了如下实验:
方案一:往第一份试液中加入少量酸化的KMnO4溶液,紫红色褪去.该方案是否合理否.(填“是”或“否”)
方案二:往第二份试液中加入K3[Fe(CN)6]溶液,实验现象为生成蓝色沉淀.
④该小组将SO2通入酸化的高锰酸钾溶液中,再向溶液中滴加氯化钡溶液,发现有白色沉淀生成,说明SO2具有还原性.该方案的不妥之处可能为高锰酸钾用硫酸酸化.
(2)该兴趣小组利用“直接碘量法”对葡萄酒中的SO2进行测量.取50.00ml葡萄酒样品于250mL碘量瓶中.加入少量碎冰块,再加入1mL淀粉指示液,10mL硫酸溶液,用浓度为cmol/L的碘标准滴定溶液迅速滴定至淡蓝色,保持30s不变即为终点,记下消耗碘标准滴定溶液的体积为VmL.以水代替样品,做空白试验,操作同上,空白试验消耗碘标准滴定溶液的体积为Voml.该葡萄酒中SO2含量计算式为$\frac{c(V-{V}_{0})×64}{50}$g/L.

(1)实验可选用的实验试剂有浓硫酸、Na2SO3固体、Na2S溶液、BaCl2溶液、FeCl3溶液、品红溶液等.
①请完成下列表格
| 试剂 | 作用 | |
| A | 验证SO2的还原性 | |
| B | Na2S溶液 | |
| C | 品红溶液 |
③在上述装置中通入过量的SO2,为了验证A中发生了氧化还原反应,取A中溶液分成两份,并设计了如下实验:
方案一:往第一份试液中加入少量酸化的KMnO4溶液,紫红色褪去.该方案是否合理否.(填“是”或“否”)
方案二:往第二份试液中加入K3[Fe(CN)6]溶液,实验现象为生成蓝色沉淀.
④该小组将SO2通入酸化的高锰酸钾溶液中,再向溶液中滴加氯化钡溶液,发现有白色沉淀生成,说明SO2具有还原性.该方案的不妥之处可能为高锰酸钾用硫酸酸化.
(2)该兴趣小组利用“直接碘量法”对葡萄酒中的SO2进行测量.取50.00ml葡萄酒样品于250mL碘量瓶中.加入少量碎冰块,再加入1mL淀粉指示液,10mL硫酸溶液,用浓度为cmol/L的碘标准滴定溶液迅速滴定至淡蓝色,保持30s不变即为终点,记下消耗碘标准滴定溶液的体积为VmL.以水代替样品,做空白试验,操作同上,空白试验消耗碘标准滴定溶液的体积为Voml.该葡萄酒中SO2含量计算式为$\frac{c(V-{V}_{0})×64}{50}$g/L.
11.下列变化中,属于物理变化的是( )
| A. | 熔融态的KCl导电 | |
| B. | 在Fe(OH)3胶体中加入MgSO4溶液析出红褐色沉淀 | |
| C. | 用加热方法分离沙子和NH4Cl晶体 | |
| D. | 蓝色CuSO4晶体,受热变为白色CuSO4粉末 |
8.氢镍电池是近年来开发出来的可充电电池,它可以取代会产生污染的镍电池.氢镍电池的总反应式是$\frac{1}{2}$H2+NiO(OH)$?_{充电}^{放电}$ Ni(OH)2,根据此反应式判断,下列叙述中正确的是( )
| A. | 电池放电时,电池负极周围溶液的pH不断增大 | |
| B. | 电池放电时,镍元素被氧化 | |
| C. | 电池充电时,氢元素被氧化 | |
| D. | 电池放电时,H2是负极 |
5.点燃的镁条能在氨气中剧烈燃烧,发生如下反应:Mg+2NH3$\frac{\underline{\;点燃\;}}{\;}$Mg(NH2)2+H2,对该反应说法正确的是( )
| A. | NH3既是氧化剂又是还原剂 | B. | 氢元素既被氧化又被还原 | ||
| C. | 0.5mol氢气生成时转移1mol电子 | D. | 镁具有氧化性 |
 某化学兴趣小组为探究铜与浓硫酸的反应以及SO2的性质,用右图所示装置进行有关实验.请回答下列问题:
某化学兴趣小组为探究铜与浓硫酸的反应以及SO2的性质,用右图所示装置进行有关实验.请回答下列问题: