题目内容
(1)据报道以硼氢化合物NaBH4(H的化合价为-1价)和H2O2作原料的燃料电池,可用作通信卫星电源.负极材料采用Pt/C,正极材料采用MnO2,其工作原理如图1所示.写出该电池放电时负极的电极反应式:

(2)火箭发射常以液态肼(N2H4)为燃料,液态过氧化氢为助燃剂.
已知:N2H4(l)+O2(g)=N2(g)+2H2O(l)△H=-534kJ?mol-1
H2O2(l)=H2O(l)+
O2(g)△H=-98.6kJ?mol-1
写出常温下,N2H4(l) 与 H2O2(l)反应生成N2和H2O的热化学方程式 .
(3)O3可由臭氧发生器(原理如右图2所示)电解稀硫酸制得.
①图中阴极为 (填“A”或“B”).
②若C处通入O2,则A极的电极反应式为:
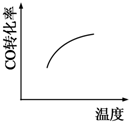
(4)向一密闭容器中充入一定量一氧化碳跟水蒸气发生反应 CO(g)+H2O(g)═CO2(g)+H2(g),下列情况下能判断该反应一定达到平衡状态的是 (选填编号).
A.v正(H2O)=v逆(H2)
B.容器中气体的压强不再发生改变
C.H2O的体积分数不再改变
D.容器中CO2和H2的物质的量之比不再发生改变
E.容器中气体的密度不再发生改变
(5)温度T1时,在一体积为2L的密闭容积中,加入0.4molCO2和0.4mol的H2,反应中c(H2O)的变化情况如图3所示,T1时反应CO(g)+H2O(g)═CO2(g)+H2(g)第4分钟达到平衡.在第5分钟时向体系中同时再充入0.1molCO和0.1molH2(其他条件不变),请在右图中画出第5分钟到9分钟c(H2O)浓度变化趋势的曲线.

(2)火箭发射常以液态肼(N2H4)为燃料,液态过氧化氢为助燃剂.
已知:N2H4(l)+O2(g)=N2(g)+2H2O(l)△H=-534kJ?mol-1
H2O2(l)=H2O(l)+
| 1 |
| 2 |
写出常温下,N2H4(l) 与 H2O2(l)反应生成N2和H2O的热化学方程式
(3)O3可由臭氧发生器(原理如右图2所示)电解稀硫酸制得.
①图中阴极为
②若C处通入O2,则A极的电极反应式为:
(4)向一密闭容器中充入一定量一氧化碳跟水蒸气发生反应 CO(g)+H2O(g)═CO2(g)+H2(g),下列情况下能判断该反应一定达到平衡状态的是
A.v正(H2O)=v逆(H2)
B.容器中气体的压强不再发生改变
C.H2O的体积分数不再改变
D.容器中CO2和H2的物质的量之比不再发生改变
E.容器中气体的密度不再发生改变
(5)温度T1时,在一体积为2L的密闭容积中,加入0.4molCO2和0.4mol的H2,反应中c(H2O)的变化情况如图3所示,T1时反应CO(g)+H2O(g)═CO2(g)+H2(g)第4分钟达到平衡.在第5分钟时向体系中同时再充入0.1molCO和0.1molH2(其他条件不变),请在右图中画出第5分钟到9分钟c(H2O)浓度变化趋势的曲线.
考点:原电池和电解池的工作原理,热化学方程式,化学平衡建立的过程,化学平衡状态的判断,电解原理
专题:
分析:(1)原电池负极发生氧化反应,正极反应还原反应,由原电池工作原理图1可知,电极a为负极,电极b为正极,BH4-在负极放电生成BO2-;
(2)根据盖斯定律,由已知热化学方程式乘以适当的系数进行加减,反应热也处于相应的系数进行相应的加减,构造目标热化学方程式,据此计算△H;
(3)①由图可知,B极生成O2、O3,B极反应氧化反应,电解池阳极发生氧化反应,故A为阴极;
②C处通入O2,O2发生还原反应,在酸性条件下生成水;
(4)化学反应达到化学平衡状态时,正逆反应速率相等,且不等于0,各物质的浓度不再发生变化,由此衍生的一些物理量不发生变化,以此进行判断,得出正确结论;
(5)据图象分析,平衡时各物质浓度都是0.10mol/L,其平衡常数K=1,再加入0.1molCO和0.1molH2时,比较K与Q的相对大小,即可判断5min后反应情况.
(2)根据盖斯定律,由已知热化学方程式乘以适当的系数进行加减,反应热也处于相应的系数进行相应的加减,构造目标热化学方程式,据此计算△H;
(3)①由图可知,B极生成O2、O3,B极反应氧化反应,电解池阳极发生氧化反应,故A为阴极;
②C处通入O2,O2发生还原反应,在酸性条件下生成水;
(4)化学反应达到化学平衡状态时,正逆反应速率相等,且不等于0,各物质的浓度不再发生变化,由此衍生的一些物理量不发生变化,以此进行判断,得出正确结论;
(5)据图象分析,平衡时各物质浓度都是0.10mol/L,其平衡常数K=1,再加入0.1molCO和0.1molH2时,比较K与Q的相对大小,即可判断5min后反应情况.
解答:
解:(1)原电池负极发生氧化反应,正极反应还原反应,由原电池工作原理图1可知,电极a为负极,电极b为正极,BH4-在负极放电生成BO2-,电极反应式为BH4--8e-+8OH-=BO2-+6H2OMnO2.
故答案为:BH4--8e-+8OH-=BO2-+6H2O;
(2)已知:①N2H4(g)+O2(g)=N2(g)+2H2O(l)△H=-534kJ?mol-1
②H2O2(l)=H2O(l)+1/2O2(g)△H=-98.64kJ?mol-1
由盖斯定律,①+②×2得N2H4(g)+2H2O2(l)=N2(g)+4H2O(g)△H=-534kJ?mol-1+2×(-98.64kJ?mol-1)=-731.2kJ?mol-1
故答案为:N2H4(l)+2H2O2(l)=N2(g)+4H2O(l)△H=-731.2 kJ/mol;
(3)①由图可知,B极生成O2、O3,B极反应氧化反应,电解池阳极发生氧化反应,故A为阴极,故答案为:A;
②C处通入O2,O2发生还原反应,在酸性条件下生成水,电极反应式为O2+4H++4e-=2H2O,故答案为:O2+4H++4e-=2H2O;
(4)A.v正(H2O)=v逆(H2),正逆反应速率相等,说明反应达到平衡状态,故A正确;
B.容器中气体的压强不再发生改变,反应前后气体体积不变,压强始终不变,压强不变不能说明反应达到平衡状态,故B错误;
C.H2O的体积分数不再改变,说明各组分浓度不变,反应达到平衡状态,故C正确;
D.容器中CO2和H2的物质的量之比决定于反应前加入物质的多少,与是否平衡无关,故C错误;
E.容器中气体的密度不再发生改变,容器体积不变,气体质量不变,密度始终不变,密度不变不能说明反应达到平衡状态,故E错误;
故答案为:AC;
(5)据图象分析,平衡时各物质浓度都是0.10mol/L,其平衡常数K=1,再加入0.1molCO和0.1molH2时,其浓度熵Q=
=1=K,平衡不移动,所以水蒸气浓度不再变化,图象为 ,故答案为:
,故答案为: .
.
故答案为:BH4--8e-+8OH-=BO2-+6H2O;
(2)已知:①N2H4(g)+O2(g)=N2(g)+2H2O(l)△H=-534kJ?mol-1
②H2O2(l)=H2O(l)+1/2O2(g)△H=-98.64kJ?mol-1
由盖斯定律,①+②×2得N2H4(g)+2H2O2(l)=N2(g)+4H2O(g)△H=-534kJ?mol-1+2×(-98.64kJ?mol-1)=-731.2kJ?mol-1
故答案为:N2H4(l)+2H2O2(l)=N2(g)+4H2O(l)△H=-731.2 kJ/mol;
(3)①由图可知,B极生成O2、O3,B极反应氧化反应,电解池阳极发生氧化反应,故A为阴极,故答案为:A;
②C处通入O2,O2发生还原反应,在酸性条件下生成水,电极反应式为O2+4H++4e-=2H2O,故答案为:O2+4H++4e-=2H2O;
(4)A.v正(H2O)=v逆(H2),正逆反应速率相等,说明反应达到平衡状态,故A正确;
B.容器中气体的压强不再发生改变,反应前后气体体积不变,压强始终不变,压强不变不能说明反应达到平衡状态,故B错误;
C.H2O的体积分数不再改变,说明各组分浓度不变,反应达到平衡状态,故C正确;
D.容器中CO2和H2的物质的量之比决定于反应前加入物质的多少,与是否平衡无关,故C错误;
E.容器中气体的密度不再发生改变,容器体积不变,气体质量不变,密度始终不变,密度不变不能说明反应达到平衡状态,故E错误;
故答案为:AC;
(5)据图象分析,平衡时各物质浓度都是0.10mol/L,其平衡常数K=1,再加入0.1molCO和0.1molH2时,其浓度熵Q=
| 0.1mol/L×(0,1+0,05)mol/L |
| 0.1mol/L×(0.1+0.05mol/L) |
 ,故答案为:
,故答案为: .
.
点评:本题考查原电池与电解池反应原理、反应热的计算、氧化还原反应计算、平衡状态判断、化学平衡图象、阅读题目获取信息的能力等,难度中等,需要学生具备运用信息与基础知识分析问题、解决问题的能力.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
有X、Y、Z、W、M五种短周期元素,其中X、Y、Z、W同周期,Z、M同主族; X+与M2-具有相同的电子层结构;离子半径:Z2->W-;Y的单质晶体熔点高、硬度大,是一种重要的半导体材料.下列说法中,正确的是( )
| A、X、M两种元素只能形成X2M型化合物 |
| B、元素Y、Z、W的单质晶体属于同种类型的晶体 |
| C、元素W和M的某些单质可作为水处理中的消毒剂 |
| D、由于W、Z、M元素的氢气化物相对分子质量依次减小,所以其沸点依次降低 |
如果ag某气体中含有的分子数为b,则cg该气体的物质的量为(设阿伏加德罗常数为NA)( )
A、
| ||
B、
| ||
C、
| ||
D、
|
下列叙述中,正确的是( )
| A、石油、煤、天然气、氢气都属于化石燃料 |
| B、常温下,反应C(s)+CO2(g)=2CO(g)不能自发进行,则该反应的△H<0 |
| C、人们通常用标准燃烧热或热值来衡量燃料燃烧放出热量的大小,某物质的热值越高则其标准燃烧热越大 |
| D、两个体积相同的容器中充入等量的NO2发生反应:2NO2(g)?N2O4(g)△H<0,绝热容器中气体的颜色比恒温容器中颜色深 |
碱性电池具有容量大、放电电流大的特点,因而得到广泛应用.锌-锰碱性电池以氢氧化钾溶液为电解液,电池总反应式为:Zn(s)+2MnO2(s)+H2O(l)
Zn(OH)2(s)+Mn2O3(s) 下列说法错误的是( )
| 放电 |
| 通电 |
| A、电池工作时,锌失去电子 |
| B、电池正极的电极反应式为:2MnO2(s)+H2O(1)+2e-=Mn2O3(s)+2OH-(aq) |
| C、电池工作时,电子由正极通过外电路流向负极 |
| D、外电路中每通过0.2mol电子,锌的质量理论上减小6.5g |
设NA 表示阿伏加德罗常数的值.下列说法正确的是( )
| A、标准状况下,22.4LCH2Cl2中含C-Cl键数目为0.2NA |
| B、常温常压下,10g92%酒精水溶液含氧原子总数为0.2NA |
| C、常温常压下,0.1molNa2O2与水完全反应转移电子数为0.2NA |
| D、常温常压下,3.0g尿素与乙酸的混合物,含氢原子总数为0.2NA |