题目内容
下列叙述中,正确的是( )
| A、石油、煤、天然气、氢气都属于化石燃料 |
| B、常温下,反应C(s)+CO2(g)=2CO(g)不能自发进行,则该反应的△H<0 |
| C、人们通常用标准燃烧热或热值来衡量燃料燃烧放出热量的大小,某物质的热值越高则其标准燃烧热越大 |
| D、两个体积相同的容器中充入等量的NO2发生反应:2NO2(g)?N2O4(g)△H<0,绝热容器中气体的颜色比恒温容器中颜色深 |
考点:焓变和熵变,化学平衡的影响因素
专题:
分析:A、氢气不是化石燃料;
B、反应不能自发,应满足△G=△H-T?△S>0;
C、1kg某种燃料完全燃烧放出的热量叫做这种燃料的热值.热值是燃料的一种特性,它只与燃料的种类有关,与燃料的质量、燃烧程度、放出热量的多少以及燃烧温度的高低等均无关;
D、反应2NO2(g)?N2O4(g)△H<0是放热反应,升温平衡向逆方向进行.
B、反应不能自发,应满足△G=△H-T?△S>0;
C、1kg某种燃料完全燃烧放出的热量叫做这种燃料的热值.热值是燃料的一种特性,它只与燃料的种类有关,与燃料的质量、燃烧程度、放出热量的多少以及燃烧温度的高低等均无关;
D、反应2NO2(g)?N2O4(g)△H<0是放热反应,升温平衡向逆方向进行.
解答:
解:A、煤、石油、天然气属于化石燃料,氢气不是化石燃料,故A错误;
B、常温下,反应C(s)+CO2(g)=2CO(g)不能自发进行,该反应的△S>0,反应不能自发,则△G=△H-T?△S>0,所以△H>0,故B错误;
C、某物质的热值高,其标准燃烧热不一定大,故C错误;
D、反应2NO2(g)?N2O4(g)△H<0是放热反应,升温平衡向逆方向进行,再次平衡时体系颜色加深,故D正确.
故选:D.
B、常温下,反应C(s)+CO2(g)=2CO(g)不能自发进行,该反应的△S>0,反应不能自发,则△G=△H-T?△S>0,所以△H>0,故B错误;
C、某物质的热值高,其标准燃烧热不一定大,故C错误;
D、反应2NO2(g)?N2O4(g)△H<0是放热反应,升温平衡向逆方向进行,再次平衡时体系颜色加深,故D正确.
故选:D.
点评:本题考查了焓变的问题化学平衡移动的原理以及平衡的影响因素等,题目难度中等,注意从等效的角度分析判断.

练习册系列答案
 云南师大附小一线名师提优作业系列答案
云南师大附小一线名师提优作业系列答案 冲刺100分单元优化练考卷系列答案
冲刺100分单元优化练考卷系列答案
相关题目
若某原子的摩尔质量是M g?mol-1,阿伏加德罗常数为NA mol-1,一个12C的质量为m g,则一个该原子的真实质量是( )
A、
| ||
B、
| ||
| C、M?NA g | ||
D、
|
将a%的某物质的水溶液加热蒸发掉m g水(溶质不挥发、且蒸发过程无溶质析出),所得溶液体积为V L,溶质的质量分数为蒸发前的2倍,设溶质的相对分子质量为M,则蒸发后所得溶液的物质的量浓度为( )mol/L.
A、
| ||
B、
| ||
C、
| ||
D、
|
下列有关化学用语的表示正确的是( )
| A、HClO的结构式:H-Cl-O |
| B、硝基和二氧化氮两种粒子所含电子数相等 |
C、甲烷分子的比例模型是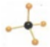 |
D、甲基的电子式: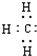 |
下列物质属于纯净物的是( )
| A、稀硫酸 | B、NaOH |
| C、液化石油气 | D、天然气 |
搜狐网曾报道,中国每年要进口5亿吨左右的铁矿石,占世界海上铁矿石贸易量的一半以上,随着全球铁矿石价格的上涨,中国钢铁工业协会与澳大利亚必和必拓公司谈判陷入困境,关于铁矿石说法正确的是( )
| A、赤铁矿的主要成分是Fe3O4 |
| B、铁矿石的主要成分与铁锈的主要成分相同 |
| C、磁铁矿粉末溶于盐酸后,加入KSCN溶液,溶液变红色 |
| D、FeO俗称铁红 |