题目内容
化学实验中,常将溶液或试剂进行酸化,下列酸化处理的措施中正确的是
A. 定性检验SO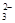 ,可用HNO3酸化的BaCl2溶液
,可用HNO3酸化的BaCl2溶液
B. 为了提高KMnO4溶液的氧化能力,可用盐酸将其酸化
C. 检验某溶液中是否含Cl–,用HNO3酸化的AgNO3溶液
D. 配制FeCl2溶液时通常加少量H2SO4酸化,减小其水解程度
练习册系列答案
相关题目
1.Ⅰ、已知室温下,碳酸的电离常数K1=4.4×10-7,K2=4.7×10-11.NaHCO3水溶液显碱性,在NaHCO3溶液中继续逐渐通入二氧化碳,至溶液中n(HCO3-):n(H2CO3)=4.4时溶液可以达中性.
Ⅱ、工业上可通过CO和H2化合制得CH3OH:CO(g)+2H2(g) CH3OH(g)△H (CO结构式为C≡O).又知某些化学键的键能(断开 1mol化学键时所需要的最低能量)数值如下表:
则△H=-116kJ•mol-1.
Ⅲ、电化学降解NO3-的原理如图1所示.
①电源 A 极为正极(填“正极”或“负极”),阴极反应式为2NO3-+10e-+12H+=6H2O+N2↑.
②若电解过程中转移了 1mol 电子,则膜左侧电解液的质量减少量为9g.
Ⅳ、已知NO2和N2O4可以相互转化:2NO2(g)?N2O4(g)△H<0.现将一定量NO2和N2O4的混合气体通入一体积为 2L的恒温密闭玻璃容器中,10min反应达平衡.反应物浓度随时间变化关系如图2.
①图2中共有两条曲线X和Y,其中曲线X表示NO2浓度随时间的变化.下列不能说明该反应已达到平衡状态的是B.
A.容器内混合气体的压强不随时间变化而改变
B.容器内混合气体的密度不随时间变化而改变
C.容器内混合气体的颜色不随时间变化而改变
D.容器内混合气体的平均分子量不随时间变化而改变
②前 10min内化学反应的平衡常数K(b) 值为$\frac{10}{9}$
③反应 25min 时,若只改变了某一个条件,使曲线发生如图2所示的变化,该条件可能是增大NO2的浓度(用文字表达);其平衡常数 K(d)=K(b)(填“>”、“=”或“<”).
Ⅱ、工业上可通过CO和H2化合制得CH3OH:CO(g)+2H2(g) CH3OH(g)△H (CO结构式为C≡O).又知某些化学键的键能(断开 1mol化学键时所需要的最低能量)数值如下表:
| 化学键 | C-C | C-H | H-H | C-O | C≡O | H-O |
| 键能 (kJ•mol-1) | 348 | 413 | 436 | 358 | 1072 | 463 |
Ⅲ、电化学降解NO3-的原理如图1所示.

①电源 A 极为正极(填“正极”或“负极”),阴极反应式为2NO3-+10e-+12H+=6H2O+N2↑.
②若电解过程中转移了 1mol 电子,则膜左侧电解液的质量减少量为9g.
Ⅳ、已知NO2和N2O4可以相互转化:2NO2(g)?N2O4(g)△H<0.现将一定量NO2和N2O4的混合气体通入一体积为 2L的恒温密闭玻璃容器中,10min反应达平衡.反应物浓度随时间变化关系如图2.
①图2中共有两条曲线X和Y,其中曲线X表示NO2浓度随时间的变化.下列不能说明该反应已达到平衡状态的是B.
A.容器内混合气体的压强不随时间变化而改变
B.容器内混合气体的密度不随时间变化而改变
C.容器内混合气体的颜色不随时间变化而改变
D.容器内混合气体的平均分子量不随时间变化而改变
②前 10min内化学反应的平衡常数K(b) 值为$\frac{10}{9}$
③反应 25min 时,若只改变了某一个条件,使曲线发生如图2所示的变化,该条件可能是增大NO2的浓度(用文字表达);其平衡常数 K(d)=K(b)(填“>”、“=”或“<”).



 液12mL,恰好与0.04mol//L的K2Cr2O7溶液10mL完全反应,通过计算确定Cr元素
液12mL,恰好与0.04mol//L的K2Cr2O7溶液10mL完全反应,通过计算确定Cr元素 在还原产物中的化合价
在还原产物中的化合价


 、B
、B .
. ,③
,③ .
.