题目内容
14.下表中实线是元素周期表的部分边界,其中上边界并未用实线画出.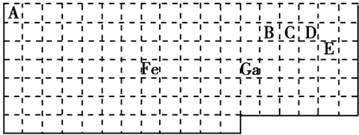
根据信息回答下列问题:
(1)基态Ga原子的最外层电子排布式为4s24p1.
(2)铁元素位于元素周期表的d区;Fe和CO易形成配合物Fe(CO)5,在Fe(CO)5中铁的化合价为0.
(3)已知:原子数目和价电子总数均相同的微粒互为等电子体,等电子体具有相似的结构特征.与CO互为等电子体的分子和离子分别为N2和CN-(填化学式).
(4)在CH4、CO、CH3OH中,碳原子采取sp3杂化的分子有CH4、CH3OH.
(5)根据VSEPR模型预测ED${\;}_{4}^{-}$的空间构型为正四面体.B、C、D、E原子相互化合形成的分子中,所有原子都满足最外层8电子稳定结构的分子为CO2、N2O3、CCl4(写3种).
分析 (1)Ga位于第四周期第IIIA族,最外层有3个电子;
(2)元素周期表五区的划分是根据最后排入的电子名称命名的;根据化合物的化合价代数和为0分析;
(3)价电子数相同和原子数相同的微粒互称等电子体;
(4)先根据价层电子对互斥理论判断价层电子对,然后再确定采取的杂化方式;
(5)价层电子对数=σ键电子对数+中心原子上的孤电子对数,根据价层电子对数判断微粒构型;根据元素周期表知,B、C、D、E分别是C、N、O、Cl是四种元素,若化合价的绝对值+原子最外层电子数=8,分子中每个原子最外层都达到8电子稳定结构,据此分析.
解答 解:(1)Ga位于第四周期第IIIA族,最外层有3个电子,其最外层电子排布式为4s24p1;
故答案为:4s24p1;
(2)元素周期表五区的划分是根据最后排入的电子名称命名的.Fe原子是26号元素,Fe原子的基态核外电子排布式为:1s22s22p63s23p63d64s2,
这些电子排列时遵循能量最低原理(先排能量低的后排能量高的),这些能级的能量大小顺序为:1s<2s<2p<3s<3p<4s<3d,
根据能量最低原理先排4s电子后排3d电子,所以 最后排入的是3d电子,根据命名规则属d区,根据化合物化合价的代数和为0,Fe与CO易形成配合物Fe(CO)5化合价的代数和为0,CO的化合价的代数和为0,
故答案为:d;0;
(3)根据等电子体的定义,CO的等电子体必须是双原子分子或离子,且电子总数相等.对于原子,原子序数=原子核外电子总数,所以,如果是分子,只要原子序数之和相等即可.CO中C是6号元素,O是8号元素,原子序数之和为14,N是7号元素,且可形成双原子分子,所以分子是N2.
故答案为:N2、CN-;
(4)在CH4中价层电子对数=σ键电子对数(4)+中心原子上的孤电子对数(0),所以碳原子采取sp3杂化.在CO分子中价层电子对数=σ键电子对数(1)+中心原子上的孤电子对数(1),所以碳原子采取sp杂化.CH3OH中,价层电子对数=σ键电子对数(4)+中心原子上的孤电子对数(0),所以碳原子采取sp3杂化.
故答案为:CH4、CH3OH;
(5)根据元素周期表知,E是Cl元素,D是O元素,ED4-是ClO4-离子,价层电子对数=σ键电子对数+中心原子上的孤电子对数,价层电子对数=4+$\frac{1}{2}$(7+1-4×2)=4,根据VSEPR理论预测ED4-离子的空间构型为正四面体型.
C、N、O、Cl是四种元素,两两形成的化合物且每个原子最外层都达到8电子稳定结构的化合物有:CO2、N2O3、CCl4;
故答案为:正四面体;CO2、N2O3、CCl4.
点评 本题考查基态原子或离子的核外电子排布或最外层电子排布、分子中原子采取的杂化方式、对于元素周期表,学习时要记住它的周期、族的划分,要熟记前36号元素,五区的划分、边界、划分依据等都要掌握,在学习中要灵活掌握根据VSEPR理论预测分子或离子的空间构型是学习的重点,也是近几年高考的热点.

CH4(g)+2O2(g)=CO2(g)+2H2O(l)△H1
2H2(g)+O2(g)═2H2O(g)△H2
2H2(g)+O2(g)=2H2O(l)△H3
常温下取体积为4:1的甲烷和氢气混合气体11.2L(标况),完全燃烧后恢复常温,放出热量为( )
| A. | 0.4△H1+0.05△H3 | B. | 0.4△H1+0.05△H2 | C. | 0.4△H1+0.1△H3 | D. | 0.4△H1+0.2△H3 |
| A. | CO2的电子式 | B. | Cl-的结构示意图: | ||
| C. | 乙烯的结构简式C2H4 | D. | Z质量数为37的氯原子${\;}_{37}^{17}$Cl |
| A. | NO:0.06mol•L-1 | B. | H2O:0.002mol•L-1 | ||
| C. | NH3:0.002mol•L-1 | D. | O2:0.00125mol•L-1 |
| 元素编号 元素性质 | ① | ② | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ |
| 原子半径 | 0.74 | 1.60 | 1.52 | 1.10 | 0.99 | 1.86 | 0.75 | 0.82 |
| 最高或 最低化合价 | +2 | +1 | +5 | +7 | +1 | +5 | +3 | |
| -2 | -3 | -1 | -3 |
(1)元素③在周期表中的位置是第二周期第ⅠA族;元素①②④⑦的气态氢化物中最稳定的是H2O(填化学式);
(2)上述元素形成的单核离子中半径最大的是P3-,半径最小的是Li+;
(3)元素①与元素⑥按照原子个数比为1:1形成的化合物与水反应的化学反应方程式2Na2O2+2H2O═4NaOH+O2↑;
(4)元素⑤形成的单质加入到元素②的氢化物的水溶液中,反应生成两种强酸的离子方程式4Cl2+H2S+4H2O═10H++8Cl-+SO42-.
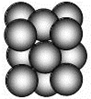 现有六种元素,其中B、C、D、E为短周期主族元素,F、G为第四周期元素,它们的原子序数依次增大.请根据下列相关信息,回答问题
现有六种元素,其中B、C、D、E为短周期主族元素,F、G为第四周期元素,它们的原子序数依次增大.请根据下列相关信息,回答问题| B元素原子的核外p电子数比s电子数少1 |
| C原子的第一至第四电离能分别是: I1=738kJ/mol I2=1451kJ/mol I3=7733kJ/mol I4=10540kJ/mol |
| D原子核外所有p轨道全满或半满 |
| E元素的主族序数与周期数的差为4 |
| F 是前四周期原子电子轨道表示式中单电子数最多的元素 |
| G在周期表的第十一列 |
(2)C和与其左右相邻元素原子的第一电离能由大到小的顺序是Mg>Al>Na.
(3)①DE3中心原子的杂化方式为sp3杂化,该分子中的键角比离子DE4+中的键角小的原因是孤电子对与成键电子对的排斥作用力大于成键电子对之间的排斥作用力
②将E的单质通入到黄血盐{K4[Fe(CN)6]}溶液中,可得到赤血盐{K3[Fe(CN)6]}.该反应的离子方程式为2[Fe(CN)6]4-+Cl2=2[Fe(CN)6]3-+2Cl-
③已知含E的一种化合物与过氧化氢发生如下反应(已配平):H2O2+
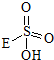 →
→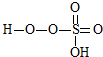 +HE,请写出横线上物质的结构式.
+HE,请写出横线上物质的结构式.(4)F位于d区,价电子排布式为3d54s1.
(5)G单质晶体中原子的堆积方式为面心立方最密堆积(如图),则晶胞中每个原子的配位数为12.假设晶胞边长为a,原子半径为r,列式表示该晶胞的空间利用率为$\frac{\sqrt{2}}{6}π$.
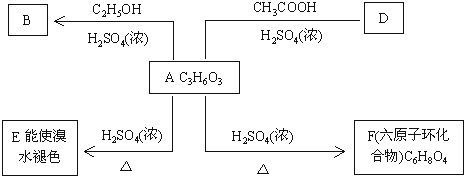

 .
.
 (X为卤素原子)
(X为卤素原子) 的物质,该物质是一种香料.请根据下述路线,回答下列问题:
的物质,该物质是一种香料.请根据下述路线,回答下列问题:
 .
. .
.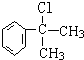 的水解产物
的水解产物 不能经氧化反应⑥而得到产品,导致产率低.
不能经氧化反应⑥而得到产品,导致产率低. 等.
等.