题目内容
4.下列物质一定属于同系物的是( )
| A. | ①和② | B. | ⑤和⑦ | C. | ④和⑥ | D. | ③和④ |
分析 结构相似,在分子组成上相差一个或若干个CH2原子团的物质互称为同系物;互为同系物的物质满足以下特点:结构相似、化学性质相似、分子式通式相同、分子式不同.
解答 解:①该有机物为甲苯,含有1个苯环;②为萘,含有两个苯环;③为苯乙烯,含有苯环和碳碳双键;④为乙烯,含有碳碳双键;⑤为1,3-丁二烯,含有两个碳碳双键;⑥为丙烯或者环丙烷;⑦为1,3-戊二烯;⑧为2-丁烯,
互为同系物的有机物,必须满足含有官能团类型、个数相等,且在分子组成上相差一个或若干个CH2原子团,以上8种物质中,满足该条件的是⑤和⑦或④和⑧,
故选B.
点评 本题考查同系物的判断,难度不大.明确同系物的概念及判断方法是解题的关键.

练习册系列答案
 阳光同学一线名师全优好卷系列答案
阳光同学一线名师全优好卷系列答案
相关题目
14.将pH=8的NaOH与pH=10的NaOH溶液等体积混合后,混合溶液的pH最接近于( )
| A. | 8.3 | B. | 8.7 | C. | 9.3 | D. | 9.7 |
15.有A、B、C、D、E五种元素,其相关信息如下:
(1)写出E元素原子基态时的电子排布式1s22s22p63s23p6sd104s1.
(2)C元素的第一电离能比氧元素的第一电离能大(填“大”或“小”).
(3)CA3分子中C原子的杂化类型是sp3,其在水中溶解度大,理由:NH3与H2O分子间形成氢键
(4)A、C、E三种元素可形成[E(CA3)4]2+,其中存在的化学键类型有①③(填序号);
①配位键 ②金属键 ③极性共价键 ④非极性共价键 ⑤离子键 ⑥氢键
若[E(CA3)4]2+具有对称的空间构型,且当[E(CA3)4]2+中的两个CA3被两个Cl-取代时,能得到两种不同结构的产物,则[E(CA3)4]2+的空间构型为a(填序号).
a.平面正方形 b.正四面体 c.三角锥形 d.V形
1mol[E(CA3)4]2+中含有σ键的数目为16mol.
| 元素 | 相关信息 |
| A | A原子的1s轨道上只有1个电子 |
| B | B是电负性最大的元素 |
| C | C基态原子的2p轨道中有3个未成对电子 |
| D | D是主族元素且与E同周期,其最外能层上有2个运动状态不同的电子 |
| E | E能形成红色(或砖红色)的E2O和黑色的EO两种氧化物 |
(2)C元素的第一电离能比氧元素的第一电离能大(填“大”或“小”).
(3)CA3分子中C原子的杂化类型是sp3,其在水中溶解度大,理由:NH3与H2O分子间形成氢键
(4)A、C、E三种元素可形成[E(CA3)4]2+,其中存在的化学键类型有①③(填序号);
①配位键 ②金属键 ③极性共价键 ④非极性共价键 ⑤离子键 ⑥氢键
若[E(CA3)4]2+具有对称的空间构型,且当[E(CA3)4]2+中的两个CA3被两个Cl-取代时,能得到两种不同结构的产物,则[E(CA3)4]2+的空间构型为a(填序号).
a.平面正方形 b.正四面体 c.三角锥形 d.V形
1mol[E(CA3)4]2+中含有σ键的数目为16mol.
19.试推断,82号元素位于周期表中的( )
| A. | 第6周期、VIA族 | B. | 第7周期、ⅥA族 | C. | 第6周期、IVA族 | D. | 第7周期、IVA族 |
9.某元素原子结构示意图为 ,该原子( )
,该原子( )
 ,该原子( )
,该原子( )| A. | 核电荷数为32 | B. | 核外电子数为16 | C. | 最外层电子数为6 | D. | 核外电子层数为3 |
16.解释下列事实的方程式不正确的是( )
| A. | 次氯酸钙溶液中通人过量二氧化碳:ClO-+H2O+CO2=HCO3-+HClO | |
| B. | 硫酸型酸雨放置一段时间溶液的pH减小:2H2SO3+O2═2H2SO4 | |
| C. | 已知:Fe2O3(s)+3C(s,石墨)═2Fe(s)+3CO(g)△H=+489.0kJ/mol CO(g)+$\frac{1}{2}$ O2(g)═CO2(g)△H=-283.0 kJ/mol C(s,石墨)+O2( g)═CO2(g)△H=-393.5kJ/mol 则4Fe(s))+3O2(g)═2Fe2O3(s)△H=-1641.0kJ/mol | |
| D. | 在复盐NH4Fe(SO4)2溶液中逐滴加入Ba(OH)2溶液,可能发生的反应的离子方程式是:3NH4++Fe3++3SO42-+3Ba2++6OH-═3BaSO4↓+Fe(OH)3↓+3NH3•H2O |
13.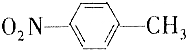 和
和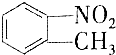 的一些物理性质如下表所示:
的一些物理性质如下表所示:
(1)分离这两种物质的混合物可采用的方法是D(填字母).
A.过滤 B.分液 C.蒸发 D.分馏
(2)实验需要用到的主要玻璃仪器是蒸馏烧瓶、酒精灯、温度计、冷凝管以及锥形瓶.
 和
和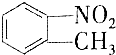 的一些物理性质如下表所示:
的一些物理性质如下表所示:| 物质 | 熔点 | 沸点 | 密度 | 水溶性 |
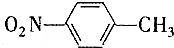 | -10℃ | 212℃ | 1.1622g/cm3 | 不溶于水 |
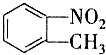 | 54℃ | 238℃ | 1.1581g/cm3 | 不溶于水 |
A.过滤 B.分液 C.蒸发 D.分馏
(2)实验需要用到的主要玻璃仪器是蒸馏烧瓶、酒精灯、温度计、冷凝管以及锥形瓶.
11.下表是周期表中的一部分,根据A~I在周期表中的位置,用相对应的元素符号或化学式 回答下列问题.
表中元素,原子半径最小的是H,原子半径最大的是Na化学性质最不活泼的是Ne,氧化性最强的单质是F2.
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 一 | H | |||||||
| 二 | C | N | F | Ne | ||||
| 三 | Na | Al | P | S |
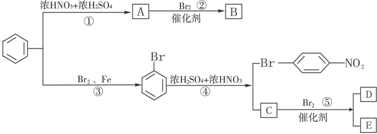
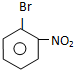 .
. ,E为
,E为 .
. .
.