题目内容
4.如图所示有关浓硫酸性质的实验装置中,实验开始一段时间后,对看到的现象叙述及原因解释都正确的是( )| A. | 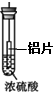 铝片无明显变化,说明浓硫酸与铝片不反应 | |
| B. | 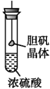 胆矾晶体表面有“白斑”,说明浓硫酸具有脱水性 | |
| C. | 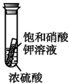 小试管内有晶体析出,说明浓硫酸具有吸水性 | |
| D. | 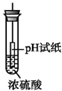 pH试纸变红,说明浓硫酸具有酸性 |
分析 A、铝片与浓硫酸无明显变化,是铝与浓硫酸发生钝化;
B、胆矾晶体表面有“白斑”,是硫酸的吸水性;
C、浓硫酸具有吸水性,导致溶液中溶剂的量减小;
D、pH试纸先变红,后变黑.
解答 解:A、铝片与浓硫酸无明显变化,是铝与浓硫酸发生钝化,而不是不反应,故A错误;
B、胆矾晶体表面有“白斑”,是硫酸的吸水性,而不是脱水性,故B错误;
C、浓硫酸具有吸水性,导致溶液中溶剂的量减小,有晶体析出,故C正确;
D、pH试纸先变红,后变黑,说明浓硫酸具有脱水性和酸性,故D错误;
故选C.
点评 本题考查浓硫酸的三大特性,吸水性、脱水性、强氧化性,学生要知道铝与浓硫酸发生钝化是化学变化,难度不大.

练习册系列答案
 小学生10分钟口算测试100分系列答案
小学生10分钟口算测试100分系列答案
相关题目
14.你认为下列说法正确的是( )
| A. | 氢键存在于分子之间,也存在于分子之内 | |
| B. | 对于分子,其范德华力只随着相对分子质量的增大而增大 | |
| C. | NH3极易溶于水而CH4难溶于水的原因只是NH3是极性分子,CH4是非极性分子 | |
| D. | 冰熔化时只破坏分子间作用力 |
12.分子式为C4H8Cl2,只含二个甲基的不同结构的物质的数目(不考虑立体异构)为( )
| A. | 2种 | B. | 3种 | C. | 5种 | D. | 4种 |
19.下列变化过程需要克服共价键的是( )
| A. | I2升华 | B. | 烧碱熔化 | ||
| C. | HCl溶于水 | D. | 溴蒸气被活性炭吸附 |
9.下列各组顺序的排列不正确的是( )
| A. | 离子半径:F->Na+>Mg2+>Al3+ | B. | 热稳定性:HF>H2O>H2S | ||
| C. | 还原性:F-<Cl-<I- | D. | 碱性强弱:NaOH>KOH>CsOH |
16.某单质(金属或非金属)跟足量的浓硫酸反应,每有1.5mol的单质反应就消耗3mol的H2SO4,则单质中的元素被氧化后的化合价可能是下列中的( )
①+1 ②+2 ③+3 ④+4.
①+1 ②+2 ③+3 ④+4.
| A. | ①② | B. | ③④ | C. | ②④ | D. | ①③ |
13.下列叙述正确的是( )
| A. | 非金属原子间以共价键结合的物质一定是共价化合物 | |
| B. | 凡是含有离子键的化合物一定是离子化合物 | |
| C. | 凡是能电离出离子的化合物一定是离子化合物 | |
| D. | 含有共价键的化合物一定是共价化合物 |
14.化学与人类生活密切相关,下列说法正确的是( )
| A. | 食品添加剂既可以是天然物质,也可以是人工合成物质,两者使用时都要控制用量 | |
| B. | 形成酸雨的元凶主要有NOx、SO2、CO2等 | |
| C. | 人体的血脂高,是因为血液中含有的名为“血脂”的化学物质超标 | |
| D. | 我国古代化学即对人类做出了重大贡献,其中冶铁和炼钢就是其中之一,前者得到的是混合物,后者是将前者提纯得到纯净物 |