题目内容
14.你认为下列说法正确的是( )| A. | 氢键存在于分子之间,也存在于分子之内 | |
| B. | 对于分子,其范德华力只随着相对分子质量的增大而增大 | |
| C. | NH3极易溶于水而CH4难溶于水的原因只是NH3是极性分子,CH4是非极性分子 | |
| D. | 冰熔化时只破坏分子间作用力 |
分析 A.邻羟基苯甲醛分子(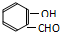 ) 内的羟基与醛基之间即存在氢键,对羟基苯甲醛分子(
) 内的羟基与醛基之间即存在氢键,对羟基苯甲醛分子( 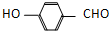 )之间存在氢键;
)之间存在氢键;
B.范德华力与相对分子质量和分子结构有关;
C.NH3与水分子之间存在氢键;
D.冰熔化时破坏分子间作用力和氢键.
解答 解:A.邻羟基苯甲醛分子(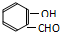 ) 内的羟基与醛基之间即存在氢键,对羟基苯甲醛分子(
) 内的羟基与醛基之间即存在氢键,对羟基苯甲醛分子(  )之间存在氢键,所以氢键存在于分子之间,也存在于分子之内,故A正确;
)之间存在氢键,所以氢键存在于分子之间,也存在于分子之内,故A正确;
B.范德华力与相对分子质量和分子结构有关,有机物同分异构体的分子式相同,相对分子质量相同,其支链越多,沸点越低,故B错误;
C.NH3与水分子之间存在氢键,使氨气易溶于水,所以NH3极易溶于水的原因为NH3是极性分子和氨气与水分子间存在氢键,故C错误;
D.水分子间存在氢键,冰熔化时破坏分子间作用力和氢键,故D错误.
故选A.
点评 本题考查了氢键、分子间作用力,题目难度不大,注意把握氢键对物质物理性质的影响.

练习册系列答案
相关题目
4.下列除去杂质(括号内为杂质)的方法中,正确的是( )
| A. | 乙烷(乙炔):将混合气体通过酸性高锰酸钾溶液,洗气除去乙烷中的乙炔气体 | |
| B. | 苯(苯酚):向混合液中加入适量的浓溴水,过滤,除去苯中的少量苯酚 | |
| C. | 酒精(水):向含水酒精中加入生石灰,蒸馏,得到无水酒精 | |
| D. | 硝基苯(NO2):向溶有杂质的硝基苯加入一定量的浓氢氧化钠溶液,振荡,分液可除去中溶解的NO2 |
5.向以下四种溶液中分别持续通入CO2,最终得到沉淀的一组是( )
①BaCl2
②Ca(OH)2
③Na2SiO3
④Na[Al(OH)4].
①BaCl2
②Ca(OH)2
③Na2SiO3
④Na[Al(OH)4].
| A. | ①③④ | B. | ②③④ | C. | ③④ | D. | ①②③ |
2.下列叙述正确的是( )
| A. | C2H2分子内含有极性键,但C2H2分子是非极性分子 | |
| B. | 分子晶体、原子晶体一定含有共价键,离子晶体一定含有离子键 | |
| C. | 气态氢化物的稳定性随着其相对分子量的增大而增强 | |
| D. | 某非金属元素从游离态变成化合态时,该元素一定被还原 |
9.与CO32-不是等电子体的是( )
| A. | SO3 | B. | BF3 | C. | NO3- | D. | PCl3 |
6.X、Y、Z是原子序数依次增大的短周期主族元素,X2-、Z+都与Mg2+具有相同的核外电子层结构,下列说法中正确的是( )
| A. | Y元素位于第二周期第ⅦA族或0族 | |
| B. | X、Y、Z三种元素中非金属性最强的是X元素 | |
| C. | Y的最高氧化物对应的水化物是已知酸中最强的酸 | |
| D. | Z分别与X、Y形成的化合物都是离子化合物 |
3.下列各组元素中,按最高正价递增顺序排列的是( )
| A. | C、N、O、F | B. | Li、Na、K、Rb | C. | F、Cl、Br、I | D. | K、Mg、C、S |
4.如图所示有关浓硫酸性质的实验装置中,实验开始一段时间后,对看到的现象叙述及原因解释都正确的是( )
| A. | 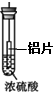 铝片无明显变化,说明浓硫酸与铝片不反应 | |
| B. | 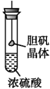 胆矾晶体表面有“白斑”,说明浓硫酸具有脱水性 | |
| C. | 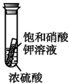 小试管内有晶体析出,说明浓硫酸具有吸水性 | |
| D. | 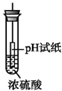 pH试纸变红,说明浓硫酸具有酸性 |