题目内容
下列实验能达到预期目的是 (填写序号).
①95%的酒精加入生石灰再蒸馏制得无水乙醇
②配制银氨溶液时,将稀氨水慢慢滴入硝酸银溶液中,至产生沉淀为止
③制乙烯时,温度计应插入反应混合液中并控制温度在140℃
④测定硫酸铜晶体结晶水的质量分数时用潮湿的坩埚
⑤检验C2H5C1中氯元素时,将C2H5C1与NaOH水溶液混合加热,再加入AgNO3溶液
⑥蔗糖水解用稀硫酸作催化剂.
①95%的酒精加入生石灰再蒸馏制得无水乙醇
②配制银氨溶液时,将稀氨水慢慢滴入硝酸银溶液中,至产生沉淀为止
③制乙烯时,温度计应插入反应混合液中并控制温度在140℃
④测定硫酸铜晶体结晶水的质量分数时用潮湿的坩埚
⑤检验C2H5C1中氯元素时,将C2H5C1与NaOH水溶液混合加热,再加入AgNO3溶液
⑥蔗糖水解用稀硫酸作催化剂.
考点:化学实验方案的评价
专题:实验评价题
分析:①乙醇易挥发,可用蒸馏的方法分离;
②配制银氨溶液,先生成沉淀,继续滴加氨水,沉淀溶解;
③制乙烯时,应控制温度在170℃;
④测定硫酸铜晶体结晶水的质量分数时应减小误差;
⑤应先酸化,防止干扰实验现象;
⑥蔗糖在酸性条件下水解.
②配制银氨溶液,先生成沉淀,继续滴加氨水,沉淀溶解;
③制乙烯时,应控制温度在170℃;
④测定硫酸铜晶体结晶水的质量分数时应减小误差;
⑤应先酸化,防止干扰实验现象;
⑥蔗糖在酸性条件下水解.
解答:
解:①加入生石灰,可起到吸收水的作用,可用蒸馏的方法分离,故①正确;
②配制银氨溶液,先生成沉淀,继续滴加氨水,沉淀溶解,生成银氨溶液,故②错误;
③制乙烯时,应控制温度在170℃,控制温度在140℃时生成乙醚,故③错误;
④测定硫酸铜晶体结晶水的质量分数时应减小误差,应用干燥的坩埚,故④错误;
⑤氯代烃在碱性条件下水解,如直接加入硝酸银生成氢氧化银沉淀而干扰实验现象,应先酸化,故⑤错误;
⑥蔗糖在酸性条件下水解,故⑥正确.
故答案为:①⑥.
②配制银氨溶液,先生成沉淀,继续滴加氨水,沉淀溶解,生成银氨溶液,故②错误;
③制乙烯时,应控制温度在170℃,控制温度在140℃时生成乙醚,故③错误;
④测定硫酸铜晶体结晶水的质量分数时应减小误差,应用干燥的坩埚,故④错误;
⑤氯代烃在碱性条件下水解,如直接加入硝酸银生成氢氧化银沉淀而干扰实验现象,应先酸化,故⑤错误;
⑥蔗糖在酸性条件下水解,故⑥正确.
故答案为:①⑥.
点评:本题考查较为综合,涉及物质的制备、检验和分离等知识,是高考中的常见题型,属于中等难度的试题.试题综合性强,在注重对学生基础知识巩固和训练的同时,侧重对学生能力的培养,有助于调动学生的学习兴趣和学习积极性,提高学生规范答题能力和学习效率.

练习册系列答案
 黎明文化寒假作业系列答案
黎明文化寒假作业系列答案 寒假天地重庆出版社系列答案
寒假天地重庆出版社系列答案
相关题目
对实验Ⅰ~Ⅳ的实验现象判断正确的是( )
A、 实验Ⅰ:产生红褐色沉淀 |
B、 实验Ⅱ:试管中溶液变红色 |
C、 实验Ⅲ:试管中溶液变红色 实验Ⅲ:试管中溶液变红色 |
D、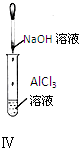 实验Ⅳ:试管中先出现白色沉淀,后溶解 |
阿伏加德罗常数约为6.02×1023mol-1,下列叙述正确的是( )
| A、常温常压下,18.0g重水(D2O)所含的电子数约为10×6.02×1023 |
| B、2.24LCl2中含有的原子数为0.2×6.02×1023 |
| C、室温下,42.0g乙烯和丙烯的混合气体中含有的碳原子数约为3×6.02×1023 |
| D、7.8g过氧化钠粉末与水反应转移的电子数为0.1×6.02×1023 |
在无色透明溶液中,一定能大量共存的离子组是( )
| A、Na+、Mg2+、SO42- |
| B、K+、H+、CO32- |
| C、Fe3+、SO42-、NO3- |
| D、Ba2+、Al3+、SO42- |
将足量CO2通入下列各溶液中,所含离子还能大量共存的是( )
| A、K+、SiO32-、NO3- |
| B、NH4+、Al3+、SO42- |
| C、Na+、OH-、SO42- |
| D、Na+、CH3COO-、ClO- |
 .请推断乳酸的结构简式:
.请推断乳酸的结构简式: