题目内容
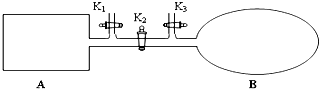 如图所示,A是由导热材料制成的密闭容器,B是一耐化学腐蚀且易于传热的透明气囊.关闭K2,将各1mol NO2通过K1、K3分别充入A、B中,反应起始时A、B的体积相同均为a L.
如图所示,A是由导热材料制成的密闭容器,B是一耐化学腐蚀且易于传热的透明气囊.关闭K2,将各1mol NO2通过K1、K3分别充入A、B中,反应起始时A、B的体积相同均为a L.①B中可通过
②若平衡后在A容器中再充入0.5mol N2O4,则重新到达平衡后,平衡混合气中NO2的体积分数
③若打开K2,平衡后B容器的体积缩至0.4a L,则打开K2之前,气球B体积为
考点:化学平衡的计算
专题:
分析:①反应达到平衡状态时,正逆反应速率相等,平衡时各种物质的物质的量、浓度等不再发生变化;
②根据压强对化学平衡的移动的影响因素来回答.
③根据等效平衡分析.
②根据压强对化学平衡的移动的影响因素来回答.
③根据等效平衡分析.
解答:
解:①B是一个气体压强不变的容器,所以当反应达到平衡状态时,混合气体的颜色和气囊体积不再改变,
故答案为:气囊不再变小或颜色不再变化;
②再加入气体,相当于增大压强,化学平衡正向移动,二氧化氮的百分含量会减小,故答案为:变小;
③打开K2,则相当于是在等温等压时的平衡,因此平衡时等效的.由于此时反应物的物质的量是B中的二倍,所以打开K2之前,气球B体积为(aL+0.4aL)÷2=0.7aL,
故答案为:0.7a;
故答案为:气囊不再变小或颜色不再变化;
②再加入气体,相当于增大压强,化学平衡正向移动,二氧化氮的百分含量会减小,故答案为:变小;
③打开K2,则相当于是在等温等压时的平衡,因此平衡时等效的.由于此时反应物的物质的量是B中的二倍,所以打开K2之前,气球B体积为(aL+0.4aL)÷2=0.7aL,
故答案为:0.7a;
点评:本题考查了化学平衡的计算等知识点,难点是根据等效平衡进行计算,难度较大.

练习册系列答案
相关题目
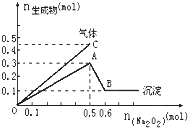 向一定量的Mg2+、NH4+、Al3+混合溶液中加入Na2O2的量与生成沉淀和气体的量(纵坐标)的关系如图所示,则溶液中Mg2+、NH4+、Al3+三种离子的物质的量之比为( )
向一定量的Mg2+、NH4+、Al3+混合溶液中加入Na2O2的量与生成沉淀和气体的量(纵坐标)的关系如图所示,则溶液中Mg2+、NH4+、Al3+三种离子的物质的量之比为( )| A、1:1:2 |
| B、2:2:1 |
| C、1:2:2 |
| D、9:2:4 |
已知某气态烃1mol最多可与2molHCl发生加成反应,所得产物与Cl2发生取代反应时,若将氢原子全部取代,需要8mol Cl2,则该烃可能是( )
| A、丙炔 | B、乙炔 |
| C、2-丁炔 | D、2-丁烯 |
下列物质的分离方法不正确的是( )
| A、用过滤的方法除去食盐水中的泥沙 |
| B、用蒸馏的方法将自来水制成蒸馏水 |
| C、用酒精萃取碘水中的碘 |
| D、用淘洗的方法从沙里淘金 |
某小组为研究原电池原理,设计如图Ⅰ、Ⅱ装置,下列叙述正确的是( )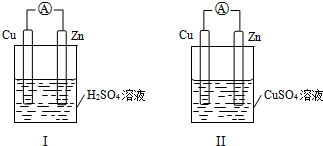

| A、装置Ⅰ,铜片上有O2逸出 |
| B、装置Ⅰ,锌片溶解,发生还原反应 |
| C、装置Ⅱ,电池反应为:Zn+Cu2+=Zn2++Cu |
| D、装置Ⅱ,外电路中,电子从铜电极流向锌电极 |