题目内容
下列关于氯水的叙述,正确的是( )
| A、新制的氯水中只含有Cl2和H2O分子 |
| B、新制的氯水可使蓝色石蕊试纸先变蓝后褪色 |
| C、光照氯水有气泡逸出,该气体是Cl2 |
| D、氯水放置数天后,pH值变小,漂白能力变弱 |
考点:氯、溴、碘及其化合物的综合应用
专题:
分析:A、新制氯水中存在氯气和水反应的化学平衡;
B、氯水溶液中氯气和水反应生成盐酸和次氯酸,溶液呈酸性;
C、氯水中次氯酸光照分解生成氧气;
D、氯水中次氯酸分解生成盐酸和氧气,溶液酸性增强,pH减小,漂白能力减弱.
B、氯水溶液中氯气和水反应生成盐酸和次氯酸,溶液呈酸性;
C、氯水中次氯酸光照分解生成氧气;
D、氯水中次氯酸分解生成盐酸和氧气,溶液酸性增强,pH减小,漂白能力减弱.
解答:
解:A、新制氯水中存在氯气和水反应的化学平衡,生成盐酸和次氯酸,故A错误;
B、氯水溶液中氯气和水反应生成盐酸和次氯酸,溶液呈酸性,可使蓝色石蕊试纸先变红后褪色,故B错误;
C、氯水中次氯酸光照分解生成氧气,故C错误;
D、氯水放置数天后,氯水中次氯酸分解生成盐酸和氧气,溶液酸性增强,pH减小,漂白能力减弱,故D正确;
故选D.
B、氯水溶液中氯气和水反应生成盐酸和次氯酸,溶液呈酸性,可使蓝色石蕊试纸先变红后褪色,故B错误;
C、氯水中次氯酸光照分解生成氧气,故C错误;
D、氯水放置数天后,氯水中次氯酸分解生成盐酸和氧气,溶液酸性增强,pH减小,漂白能力减弱,故D正确;
故选D.
点评:本题考查了氯气性质的分析判断,物质性质的理解应用是解题关键,题目较简单.

练习册系列答案
 云南师大附小一线名师提优作业系列答案
云南师大附小一线名师提优作业系列答案 冲刺100分单元优化练考卷系列答案
冲刺100分单元优化练考卷系列答案
相关题目
下列分子的VSEPR模型与分子立体结构模型一致的是( )
| A、NH3 |
| B、CCl4 |
| C、H2O |
| D、PCl3 |
下列说法不正确的是( )
| A、水晶项链和餐桌上的瓷盘都是硅酸盐制品 |
| B、形成酸雨的氧化物主要是SO2和氮的氧化物,CO2是造成温室效应的主要气体 |
| C、欲提高氯水中HClO的浓度可往氯水加适量的碳酸钙粉末 |
| D、大气中的N2可转化为NO,NO可转化为NO2、硝酸等;含硫物质在自然界中可转化为SO2等含硫化合物 |
下列实验仪器不能用于混合物分离提纯的是( )
| A、漏斗 | B、蒸馏烧瓶 |
| C、容量瓶 | D、分液漏斗 |
把质量为m g的铜丝灼烧变黑,立即放入下列物质中,能使铜丝变红,而且质量仍为m g的是( )
| A、稀H2SO4 |
| B、C2H5OH |
| C、稀HNO3 |
| D、CH3COOH溶液 |
在0.1mol?L-1 CH3COOH溶液中存在如下电离平衡:CH3COOH?CH3COO-+H+.对于该平衡,下列叙述正确的是( )
| A、加入水时,CH3COOH的电离程度增大 |
| B、加入少量NaOH固体,平衡向正反应方向移动 |
| C、通入少量 HCl气体,溶液中c(H+)减小 |
| D、加入少量CH3COONa固体,平衡向正反应方向移动 |
若将某种富含维生素C的水果切碎捣烂,加水溶解,提取其滤液就能达到充分提取水果中的维生素c的目的,这说明服用维生素c可使食物中的Fe3+转化成Fe2+,有利于人体吸收,在该化学反应中维生素c体现( )
| A、能溶于水,氧化性 |
| B、不能溶于水,氧化性 |
| C、能溶于水,还原性 |
| D、不能溶于水,还原性 |
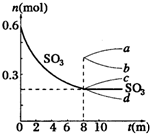 在一个2L的密闭容器中,发生反应:2SO3(g)?2SO2+O2△H>0,其中SO3的变化如图示:
在一个2L的密闭容器中,发生反应:2SO3(g)?2SO2+O2△H>0,其中SO3的变化如图示: