题目内容
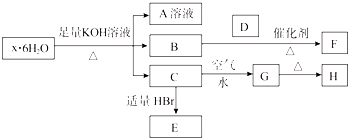
17. 在图所示物质的转化关系中,D在常温下为无色无味的液体(反应条件均已省略).请回答下列问题:
在图所示物质的转化关系中,D在常温下为无色无味的液体(反应条件均已省略).请回答下列问题:(1)高温下发生的反应②中,若F为常见的金属单质,H是非金属单质,用化学方程式表示G的一个重要用途:Fe3O4+4CO$\frac{\underline{\;高温\;}}{\;}$3Fe+4CO2.
(2)若F为淡黄色粉末,
①写出反应②的化学方程式并用双线桥标出电子转移的方向和数目
 .
.②F的电子式
 .
.(3)若A是一种强酸,B是一含有两种金属元素的盐,且其水溶液显碱性,写出①反应的离子方程式AlO2-+4H+=Al3+2H2O.
(4)若A、F、H是短周期且相邻的两个族的元素单质,且反应均在溶液中进行,请写出:
①的离子方程式Cl2+2OH-=Cl-+ClO-+H2O;
②的化学方程式2F2+2H2O=4HF+O2.
分析 (1)D常温常压下为无色无味液体,可判断D为水.高温下与水反应的常见金属单质可以是铁,同时放出无色气体H为H2,G为Fe3O4,Fe3O4的重要用途有炼铁、铝热反应等;
(2)F为淡黄色粉末,且能与水反应生成非金属单质,则F是Na2O2;
(3)B是含有两种金属形成的盐,且溶液呈碱性,说明是弱酸盐,常见的B为偏铝酸盐;
(4)单质A能与B反应生成三种物质,其中之一为水,其相邻元素与水反应生成非金属单质可判断,符合条件的反应只有Cl2和碱反应生成氯化物、次氯酸盐和水,H2O与F2反应可生成HF和O2.
解答 解:(1)D常温常压下为无色无味液体,可判断D为水.高温下与水反应的常见金属单质可以是铁,同时放出无色气体H为H2,G为Fe3O4,Fe3O4的重要用途有炼铁、铝热反应等,反应方程式为:Fe3O4+4CO$\frac{\underline{\;高温\;}}{\;}$3Fe+4CO2等,
故答案为:Fe3O4+4CO$\frac{\underline{\;高温\;}}{\;}$3Fe+4CO2;
(2)F为淡黄色粉末,且能与水反应生成非金属单质,则F是Na2O2.
①用双线桥标出反应②的电子转移的方向和数目为: ,
,
故答案为: ;
;
②Na2O2的电子式为 ,故答案为:
,故答案为: ;
;
(3)B是含有两种金属形成的盐,且溶液呈碱性,说明是弱酸盐,常见的B为偏铝酸盐,①反应的离子方程式为AlO2-+4H+=Al3+2H2O,故答案为:AlO2-+4H+=Al3+2H2O;
(4)单质A能与B反应生成三种物质,其中之一为水,其相邻元素与水反应生成非金属单质可判断,符合条件的反应只有Cl2和碱反应生成氯化物、次氯酸盐和水,H2O与F2反应可生成HF和O2.反应①的离子方程式为:Cl2+2OH-=Cl-+ClO-+H2O,反应②的化学方程式:2F2+2H2O=4HF+O2,
故答案为:Cl2+2OH-=Cl-+ClO-+H2O;2F2+2H2O=4HF+O2.
点评 本题考查无机物推断,基本属于猜测验证型题目,需要学生熟练掌握元素化合物性质,难度较大.

| A. | 生活中常用的塑料制品及橡胶制品都为高分子材料 | |
| B. | 向牛奶中加入果汁会产生沉淀,这是因为酸碱发生了中和反应 | |
| C. | 节日焰火是某些金属元素焰色反应所呈现出来的色彩 | |
| D. | 可用蘸浓盐酸的棉棒检验输送氨气的管道是否漏气 |
| A. | 将AlCl3溶液加热蒸干可得无水AlCl3 | |
| B. | 用25ml碱式滴定管量出14.80ml的碳酸钠溶液 | |
| C. | 在中和滴定的实验过程中,目光只应注视滴定管的液面 | |
| D. | 用蒸馏水湿润过的pH试纸测0.1mol/L的醋酸溶液的pH值 |
| A. | 将分别蘸有浓硝酸和浓氨水的玻璃棒相互靠近时,有白烟生成 | |
| B. | 硝酸具有酸的通性,如果与活泼金属反应,会有H2生成 | |
| C. | 浓硝酸能使活泼金属如铝、镁、锌、铁等发生“钝化” | |
| D. | 常温下,铜与稀HNO3反应很慢,是因为发生了“钝化” |
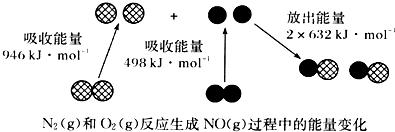
| A. | 1molN2(g)和NA个O2(g)反应放出的能量为180 kJ | |
| B. | 1molN2(g)和1molO2(g)具有总能量小于2molNO(g)具有的总能量 | |
| C. | 通常情况下,N2(g)和O2(g)混合能直接生成NO | |
| D. | 吸热反应一定需要加热才能发生 |
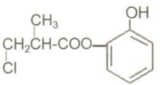
| A. | 有机物A与浓硫酸混合加热,可以发生消去反应 | |
| B. | 1molA和足量的H2发生加成反应,最多可以消耗4molH2 | |
| C. | 1molA和足量NaOH溶液发生反应,最多可以消耗 4molNaOH | |
| D. | 有机物A不能在稀硫酸下水解 |
| A. | 金刚石>碳化硅>晶体硅 | B. | 邻羟基苯甲酸>对羟基苯甲酸 | ||
| C. | 纯铁>生铁 | D. | MgO>MgCl2 |
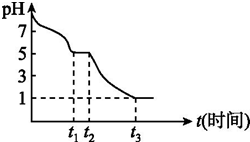 连二亚硫酸钠(Na2S2O4)又称保险粉,是印刷工业中重要的还原剂.某课题小组进行如下实验.
连二亚硫酸钠(Na2S2O4)又称保险粉,是印刷工业中重要的还原剂.某课题小组进行如下实验.