题目内容
11.实验室配制500mL 0.1mol/LNa2CO3溶液回答下列问题(1)应用托盘天平称取十水碳酸钠晶体(Na2CO3•10H2O)14.3g
(2)用托盘天平和小烧杯称出碳酸钠晶体的质量,其正确操作顺序的标号为ACBDE
A.调整零点
B.将碳酸钠晶体放入小烧杯中称量
C.称量空的小烧杯
D.将砝码放回砝码盒内
E.记录称量结果
(3)配制Na2CO3溶液时需用的主要仪器有托盘天平、滤纸、烧杯、药匙、玻璃棒、烧杯、500mL容量瓶、胶头滴管.
(4)若实验遇下列情况,溶液的浓度是偏高,偏低还是不变?
A.加水时超过刻度线偏低;
B.忘记将洗涤液转入容量瓶偏低;
C.容量瓶内壁附有水珠而未干燥处理不变;
D.定容后摇匀液面低于刻度线不变.
E.转移时有少量液体溅出偏低.
分析 (1)依据n=CV、m=nM计算需要溶质的质量;
(2)根据用天平称量物体时的正确操作顺序进行分析解答;
(3)根据实验操作的步骤以确定溶液配制所需仪器;
(4)分析操作对溶液物质的量、溶液体积的影响,根据c=$\frac{n}{V}$分析操作对所配溶液浓度的影响.
解答 解:(1)500L 0.1mol/LNa2CO3溶液含有溶质的物质的物质的量为:0.1mol/L×0.5L=0.05mol,所以需要Na2CO3•10H2O的质量是0.05mol×286g/mol=14.3g;
故答案为:14.3;
(2)用天平称量物体时的正确操作步骤是:先将游码移至刻度尺的零刻度处并调零点,然后先称量空的小烧杯的质量,记录称量的结果,将碳酸钠晶体放入小烧杯中称量,记录称量的结果,将砝码放回砝码盒内,最后将游码移至刻度尺的零刻度处,
故答案为:ACBDE;
(3)溶液配制操作步骤有:称量、溶解、移液、洗涤、定容、摇匀等操作,一般用托盘天平称量,用药匙取药品,在烧杯中溶解,并用玻璃棒搅拌,冷却后转移到500ml容量瓶中,并用玻璃棒引流,洗涤并将该洗涤液移入容量瓶中,当加水至液面距离刻度线1~2cm时,改用胶头滴管滴加,所需要的仪器为:烧杯、天平、玻璃棒、500mL容量瓶、胶头滴管、药匙,还缺少的仪器:烧杯、玻璃棒、500mL容量瓶、胶头滴管;
故答案为:烧杯、玻璃棒、500mL容量瓶、胶头滴管;
(4)A.定容时加水时超过刻度线,溶液体积偏大,配制浓度偏低;
B.洗涤液未移入容量瓶,会造成溶质损失,使配制溶液浓度偏低;
C.容量瓶内壁附有水珠而未干燥,对溶质和溶剂都无影响,所以配制浓度不变;
D.定容后摇匀,液面低于刻度线,容量瓶内壁附有水珠,属于正常操作,对所配溶液浓度不变;
E.转移时有少量液体溅出,导致部分溶质损耗,溶质的物质的量偏小,溶液浓度偏低;
故答案为:偏低;偏低;不变;不变;偏低.
点评 本题考查一定物质的量浓度溶液的配制操作及误差分析等,难度中等,注意根据c=$\frac{n}{V}$理解溶液的原理与误差分析.

 高中必刷题系列答案
高中必刷题系列答案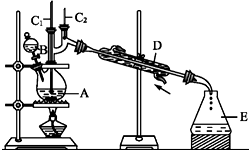
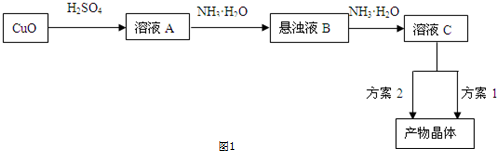
发生的反应如下:
CH3CH2CH2CH2OH$→_{H_{2}SO_{4},△}^{Na_{2}Cr_{2}O_{7}}$CH3CH2CH2CHO
反应物和产物的相关数据列表如下:
| 沸点/℃ | 密度/(g•cm-3) | 水中溶解性 | |
| 正丁醇 | 117.2 | 0.810 9 | 微溶 |
| 正丁醛 | 75.7 | 0.801 7 | 微溶 |
将6.0g Na2Cr2O7放入100mL烧杯中,加30mL水溶解,再缓慢加入5mL浓硫酸,将所得溶液小心转移至B中.在A中加入4.0g正丁醇和几粒沸石,加热.当有蒸气出现时,开始滴加B中溶液.滴加过程中保持反应温度为90-95℃,在E中收集90℃以下的馏分.将馏出物倒入分液漏斗中,分去水层,有机层干燥后蒸馏,收集75-77℃馏分,产量2.0g.
回答下列问题:
(1)实验中,能否将Na2Cr2O7溶液加到浓硫酸中,说明理由不能,容易发生迸溅.
(2)加入沸石的作用是防止暴沸.若加热后发现未加沸石,应采取的正确方法是冷却后补加.
(3)上述装置图中,B仪器的名称是分液漏斗,D仪器的名称是直形冷凝管.
(4)分液漏斗使用前必须进行的操作是C(填正确答案标号).
A.润湿 B.干燥 C.检漏 D.标定
(5)将正丁醛粗产品置于分液漏斗中分水时,水在下层(填“上”或“下”).
(6)反应温度应保持在90~95℃,其原因是保证正丁醛及时蒸出,又可尽量避免其被进一步氧化
(7)本实验中,正丁醛的产率为51%.
| 溶质 | NaF | CH3COONa | Na2S |
| pH | 7.5 | 9.5 | 11.8 |
| A. | 根据如,NaF的水解程度比CH3COONa的大 | |
| B. | 同体积、同pH的两种酸溶液消耗同浓度NaOH的体积:HF>CH3COOH | |
| C. | 向100mL 0.1 mol•L-1 CH3COONa溶液中通入224mL HF气体(标准状况):c(CH3COOH)+c(H+)═c(OH-)+c(F-) | |
| D. | 若将0.05 mol HC1缓慢地通入1 L 0.1 moL•L-Na2S溶液中,则溶液中离子浓度大小为:c(Cl-)>c(HS-)>c(OH-)c(S2-)>c(H+) |
①用天平(使用游码)称量时,被称量物与砝码的位置放颠倒了
②用量筒量取液体时,仰视读数
③溶液转移到容量瓶后,烧杯及玻璃棒未用蒸馏水洗涤
④转移溶液前容量瓶内有少量蒸馏水
⑤定容时,仰视容量瓶的刻度线
⑥定容后摇匀,发现液面降低,又补加少量水,重新达到刻度线.
| A. | ①③⑤⑥ | B. | ①②⑤⑥ | C. | ②③④⑥ | D. | ③④⑤⑥ |
 水煤气是重要燃料和化工原料,可用水蒸气通过炽热的炭层制得:
水煤气是重要燃料和化工原料,可用水蒸气通过炽热的炭层制得:C (s)+H2O(g)?CO (g)+H2 (g)△H=+131.3kJ•mol-1
(1)该反应的平衡常数K随温度的升高而增大(增大、减小、不变).
(2)上述反应达到平衡后,增加H2O(g)的量,则C (s) 的物质的量减小(增大、减小、不变).
(3)下列说法一定能判断如上反应达平衡的是BC
A.消耗1mol H2O(g)同时生成1mol H2
B.容器内混合气体的总质量不变
C.恒温恒容时容器内气体的压强不变
D.H2O(g)、CO (g)、H2 (g)三种气体的浓度比为1:1:1
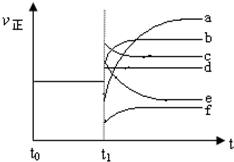
(4)上述反应在t0时刻达到平衡,在t1时刻改变某一条件后正反应速率(ν正)随时间的变化如下图所示,填出对应的编号.
①缩小容器体积b;
②降低温度f.
(5)一定温度下,三个容器中均进行着上述反应,各容器中炭足量,其它物质的物质的量浓度及正逆反应速率关系如下表所示.请填写表中①②相应的空格.
| 容器编号 | c(H2O)/mol•L-1 | c(CO)/mol•L-1 | c(H2)/mol•L-1 | ν正、ν逆比较 |
| I | 0.06 | 0.60 | 0.10 | ν正=ν逆 |
| Ⅱ | 0.12 | 0.20 | 0.60① | ν正=ν逆 |
| Ⅲ | 0.10 | 0.20 | 0.40 | ν正_②>ν逆 |
| A. | B2H6(g)+3O2(g)═B2O3(s)+3H2O(g)△H=-2165kJ•mol-1 | |
| B. | B2H6(g)+3O2(g)═B2O3(s)+3H2O(g)△H=-2033kJ•mol-1 | |
| C. | B2H6(g)+3O2(g)═B2O3+3H2O△H=-2165kJ•mol-1 | |
| D. | B2H6(g)+O2(g)═B2O3(s)+H2O(l)△H=-2165kJ•mol-1 |
| A. | 麻黄碱 | B. | 青霉素 | C. | 板蓝根冲剂 | D. | 牛黄解毒丸 |