��Ŀ����
3��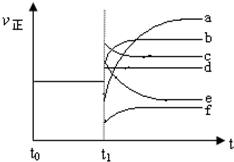 ˮú������Ҫȼ�Ϻͻ���ԭ�ϣ�����ˮ����ͨ�����ȵ�̿���Ƶã�
ˮú������Ҫȼ�Ϻͻ���ԭ�ϣ�����ˮ����ͨ�����ȵ�̿���Ƶã�C ��s��+H2O��g��?CO ��g��+H2 ��g����H=+131.3kJ•mol-1
��1���÷�Ӧ��ƽ�ⳣ��K���¶ȵ����߶���������С�����䣩��
��2��������Ӧ�ﵽƽ�������H2O��g����������C ��s�� �����ʵ�����С������С�����䣩��
��3������˵��һ�����ж����Ϸ�Ӧ��ƽ�����BC
A������1mol H2O��g��ͬʱ����1mol H2
B�������ڻ�����������������
C�����º���ʱ�����������ѹǿ����
D��H2O��g����CO ��g����H2 ��g�����������Ũ�ȱ�Ϊ1��1��1
��4��������Ӧ��t0ʱ�̴ﵽƽ�⣬��t1ʱ�̸ı�ijһ����������Ӧ���ʣ���������ʱ��ı仯����ͼ��ʾ�������Ӧ�ı�ţ�
�����������b��
�ڽ����¶�f��
��5��һ���¶��£����������о�������������Ӧ����������̿�������������ʵ����ʵ���Ũ�ȼ����淴Ӧ���ʹ�ϵ���±���ʾ������д���Т٢���Ӧ�Ŀո�
| ������� | c��H2O��/mol•L-1 | c��CO��/mol•L-1 | c��H2��/mol•L-1 | �����������Ƚ� |
| I | 0.06 | 0.60 | 0.10 | ����=���� |
| �� | 0.12 | 0.20 | 0.60�� | ����=���� |
| �� | 0.10 | 0.20 | 0.40 | ����_�ڣ����� |
���� ��1������ӦΪ���ȷ�Ӧ�������¶ȣ�ƽ��������Ӧ�����ƶ���ƽ�ⳣ������
��2������H2O��g����������ѧƽ��������Ӧ�����ƶ���
��3�����淴Ӧ����ƽ��ʱ��ͬһ���ʱ�ʾ�����淴Ӧ������ȣ�����ֵ�Ũ�ȡ��������䣬�ɴ�����������һЩ�����䣬�ж�ƽ���������Ӧ�淴Ӧ���з����仯�����������ɱ仯�����ٱ仯��˵������ƽ�⣻
��4������С���������ѹǿ����˲�����淴Ӧ���ʶ�����ƽ�����淴Ӧ�����ƶ����淴Ӧ����������࣬�������Ӧ����������ƽ�⣻
�ڽ����¶ȣ�˲�����淴Ӧ���ʶ���С��ƽ�����淴Ӧ�����ƶ�������Ӧ���ʼ�С���࣬�������Ӧ����������ƽ�⣬������ƽ��ʱ������С��ԭƽ������ʣ�
��5�����ݢ����ƽ�ⳣ�������д���ƽ��״̬������ƽ�ⳣ���������c��H2����
������д�ʱ��Ũ����Qc����ƽ�ⳣ���Ƚϣ��жϷ�Ӧ���еķ��ݴ��жϣ�
��� �⣺��1���÷�Ӧ����Ӧ�����ȷ�Ӧ�������¶�ƽ��������Ӧ�����ƶ���ƽ�ⳣ������
�ʴ�Ϊ������
��2������H2O��g����������ѧƽ��������Ӧ�����ƶ���̼�����ʵ�����С��
�ʴ�Ϊ����С��
��3��A������1mol H2O��g��ͬʱ����1mol H2������ʾ����Ӧ���ʣ���Ӧʼ�հ��˹�ϵ���У���A����
B��̼Ϊ���壬��������Ϊ���壬�淴Ӧ���л���������������������ڻ�����������������˵������ƽ�⣬��B��ȷ��
C�����º���ʱ���淴Ӧ���л���������ʵ�������������ѹǿ���������������ѹǿ����ʱ����Ӧ����ƽ�⣬��C��ȷ��
D��ƽ��ʱ�����Ũ��֮����ˮ��ת�����йأ���ˮ��ת���ʲ�һ��Ϊ50%����D����
�ʴ�Ϊ��BC��
��4������С���������ѹǿ����˲�����淴Ӧ���ʶ�����ƽ�����淴Ӧ�����ƶ����淴Ӧ����������࣬�������Ӧ����������ƽ�⣬������b���ϣ�
�ʴ�Ϊ��b��
�ڽ����¶ȣ�˲�����淴Ӧ���ʶ���С��ƽ�����淴Ӧ�����ƶ�������Ӧ���ʼ�С���࣬�������Ӧ����������ƽ�⣬������ƽ��ʱ������С��ԭƽ������ʣ�����f���ϣ��ʴ�Ϊ��f��
��5���ɢ��֪��ƽ�ⳣ��K=$\frac{0.1��0.6}{0.06}$=1�����д���ƽ��״̬������ƽ�ⳣ����֪����c��H2��=$\frac{K��c��{H}_{2}O��}{c��CO��}$=$\frac{1��0.12}{0.2}$mol/L=0.60mol/L��
���д�ʱ��Ũ����Qc=$\frac{0.4��0.2}{0.1}$=0.8��1���ʷ�Ӧ������Ӧ������У��ʦ�����������
�ʴ�Ϊ��0.60������
���� ���⿼�黯ѧƽ�ⳣ��Ӱ�����ء�Ӧ�ü��йؼ��㡢��ѧƽ�⼰��Ӧ���ʵ�Ӱ�����ء���ѧƽ��״̬���жϣ��Ƕ�ѧ���ۺ������Ŀ��飬�Ѷ��еȣ�

 ���Ͱ�ͨ��ĩ���ϵ�д�
���Ͱ�ͨ��ĩ���ϵ�д�| ѡ�� | ����ƿ�ݻ� | �������� | ʵ����� |
| A | 180mL | SrCl2��28.6g | ����180mLˮ |
| B | 200mL | SrCl2��31.8g | ���200mL��Һ |
| C | 250mL | SrCl2��39.8g | ���250mL��Һ |
| D | 250mL | SrCl2•2H2O��39.8g | ���250mL��Һ |
| A�� | A | B�� | B | C�� | C | D�� | D |
| A�� | �������ʯ��ʯ�ϣ�CaCO3+2H+�TCa2++H2O+CO2�� | |
| B�� | �����ʯ��ˮ�м���������Һ��H++OH-�TH2O | |
| C�� | ��Ba��OH��2��Һ�е��������Na2SO ��Һ��2H++SO42-+Ba2++2OH-�TBaSO4��+2H2O | |
| D�� | ϡ�������ͭƬ�ϣ�Cu+2H+�TCu2++H2�� |

