题目内容
1.已知酸性: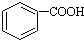 >H2CO3>
>H2CO3>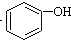 ,将
,将 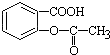 转变为
转变为 的方法是( )
的方法是( )| A. | 与足量的NaOH溶液共热,再通入CO2 | |
| B. | 与稀H2SO4共热后,加入足量的NaOH溶液 | |
| C. | 加热溶液,通入足量的CO2 | |
| D. | 与稀H2SO4共热后,加入足量的NaHCO3溶液 |
分析 将 转变为
转变为 ,可先发生碱性条件的水解,再由酸性的强弱可知,水解产物中通入足量的CO2即可,以此解答.
,可先发生碱性条件的水解,再由酸性的强弱可知,水解产物中通入足量的CO2即可,以此解答.
解答 解:A.与足量的NaOH溶液共热,生成羧酸钠和酚钠结构,因 >H2CO3>
>H2CO3> ,则再通入足量的CO2生成邻羟基苯甲酸钠,故A正确;
,则再通入足量的CO2生成邻羟基苯甲酸钠,故A正确;
B.与稀H2SO4共热后,生成邻羟基苯甲酸,再加入足量的NaOH溶液,生成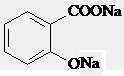 ,故B错误;
,故B错误;
C.加热溶液,通入足量的CO2,不发生反应,故C错误;
D.与稀H2SO4共热后,生成邻羟基苯甲酸,加入足量的NaHCO3溶液,只有-COOH反应生成羧酸钠和酚结构,生成 ,故D正确;
,故D正确;
故选AD.
点评 本题考查有机物的结构和性质,为高频考点,把握官能团与性质的关系为解答的关键,侧重酚、羧酸、酯性质的考查,注意酸性的比较及强酸制取弱酸的反应原理,题目难度不大.

练习册系列答案
 课时训练江苏人民出版社系列答案
课时训练江苏人民出版社系列答案
相关题目
11.沼气的主要成份是CH4,0.5molCH4完全燃烧生成二氧化碳和液态水时放出445kJ热量.下列热化学方程式正确的是( )
| A. | CH4(g)+2O2(g)=CO2(g)+2H2O(l)△H=+890 kJ/mol | |
| B. | CH4(g)+2O2(g)=CO2(g)+2H2O(g)△H=-890kJ/mol | |
| C. | CH4(g)+2O2(g)=CO2(g)+2H2O(l)△H=-445kJ/mol | |
| D. | CH4(g)+2O2(g)=CO2(g)+2H2O(l)△H=-890kJ/mol |
12.TiO2和TiCl4都是钛的重要化合物,某化学兴趣小组在实验室对两者的制备及性质进行探究.
Ⅰ.制备TiCl4
实验室利用反应TiO2 (s)+CCl4(g)$\frac{\underline{\;\;△\;\;}}{\;}$TiCl4(g)+CO2(g),在无水无氧条件下制备TiCl4,装置图和有关信息如下:

请回答下列问题:
(1)仪器A的名称是球形干燥管.
(2)实验开始前的操作包括:①组装仪器,②检验装置气密性,③加装药品,④通N2一段时间,⑤最后点燃酒精灯.实验结束后欲分离D中的液态混合物,所采用操作的名称是蒸馏 (或分馏).
(3)装置E能否不能(填“能”或“不能”)换成装置A,理由是装置A不能吸收空气中的氧气,不能保证反应在无氧环境下进行
(4)TiCl4是制取航天航空工业材料--钛合金的重要原料.某钛合金的元素还有Al和Si等,已知在常温下,钛是一种耐强酸强碱的金属,请设计实验检验其中的Si元素取少量合金样品于试管中,滴加过量NaOH溶液,振荡,静置后取上层清液,再逐滴滴入稀盐酸至过量,若有沉淀产生且最终沉淀不完全溶解,则证明样品中有Si
Ⅱ.制备TiO2及测定TiO2的质量分数:
在TiCl4中加水、加热,水解得到沉淀TiO2•xH2O,经过滤、水洗除去其中的Cl-,再烘干、焙烧除去水分得到粉体TiO2.
(5)写出生成TiO2•xH2O的化学方程式TiCl4+(x+2)H2O$\frac{\underline{\;\;△\;\;}}{\;}$TiO2•xH2O↓+4HCl.
(6)一定条件下,将TiO2溶解并还原为Ti3+,用NH4Fe(SO4)2标准溶液滴定Ti3+至全部生成Ti4+.滴定分析时,称取上述TiO2试样0.2g,消耗0.1mol•L-1 NH4Fe(SO4)2标准溶液20mL.
①配制NH4Fe(SO4)2标准溶液时,加入一定量H2SO4的目的是:抑制NH4Fe(SO4)2水解.
②该滴定操作所用到的指示剂是KSCN溶液.
③则TiO2质量分数为80%.
Ⅰ.制备TiCl4
实验室利用反应TiO2 (s)+CCl4(g)$\frac{\underline{\;\;△\;\;}}{\;}$TiCl4(g)+CO2(g),在无水无氧条件下制备TiCl4,装置图和有关信息如下:

| 物质 | 熔点/℃ | 沸点/℃ | 其他 |
| CCl4 | -23 | 76 | 与TiCl4互溶 |
| TiCl4 | -25 | 136 | 遇潮湿空气产生白雾 |
(1)仪器A的名称是球形干燥管.
(2)实验开始前的操作包括:①组装仪器,②检验装置气密性,③加装药品,④通N2一段时间,⑤最后点燃酒精灯.实验结束后欲分离D中的液态混合物,所采用操作的名称是蒸馏 (或分馏).
(3)装置E能否不能(填“能”或“不能”)换成装置A,理由是装置A不能吸收空气中的氧气,不能保证反应在无氧环境下进行
(4)TiCl4是制取航天航空工业材料--钛合金的重要原料.某钛合金的元素还有Al和Si等,已知在常温下,钛是一种耐强酸强碱的金属,请设计实验检验其中的Si元素取少量合金样品于试管中,滴加过量NaOH溶液,振荡,静置后取上层清液,再逐滴滴入稀盐酸至过量,若有沉淀产生且最终沉淀不完全溶解,则证明样品中有Si
Ⅱ.制备TiO2及测定TiO2的质量分数:
在TiCl4中加水、加热,水解得到沉淀TiO2•xH2O,经过滤、水洗除去其中的Cl-,再烘干、焙烧除去水分得到粉体TiO2.
(5)写出生成TiO2•xH2O的化学方程式TiCl4+(x+2)H2O$\frac{\underline{\;\;△\;\;}}{\;}$TiO2•xH2O↓+4HCl.
(6)一定条件下,将TiO2溶解并还原为Ti3+,用NH4Fe(SO4)2标准溶液滴定Ti3+至全部生成Ti4+.滴定分析时,称取上述TiO2试样0.2g,消耗0.1mol•L-1 NH4Fe(SO4)2标准溶液20mL.
| TiCl4 | Mg | MgCl2 | Ti | |
| 熔点/℃ | -25.0 | 648.8 | 714 | 1667 |
| 沸点/℃ | 136.4 | 1090 | 1412 | 3287 |
②该滴定操作所用到的指示剂是KSCN溶液.
③则TiO2质量分数为80%.
9.下列有机物溶液在适量的浓度时,不能用于杀菌消毒的是( )
| A. | 苯酚溶液 | B. | 乙醇溶液 | C. | 福尔马林 | D. | 乙酸乙酯溶液 |
1.下面为钠及其化合物相关的实验报告,请根据题意完成各空白处:
实 验 报 告
(一)实验目的:探究钠及其化合物的有关性质
(二)实验药品及仪器:金属钠,蒸馏水,酒精灯,试管,木条,石棉网,铁架台
(三)实验过程:
(四)实验反思:
(1)钠的化学性质活泼,在自然界中全部以化合态形态(填“游离态”或“化合态”)存在,因此少量钠应保存在煤油中.
(2)写出Na2O2的一种用途:作供氧剂或利用强氧化性杀菌消毒.
实 验 报 告
(一)实验目的:探究钠及其化合物的有关性质
(二)实验药品及仪器:金属钠,蒸馏水,酒精灯,试管,木条,石棉网,铁架台
(三)实验过程:
| 实验步骤 | 实验现象 | 化学方程式或结论 |
| 金属Na长时间放置在空气中 | 银白色的金属光泽消失,迅速变暗,有水珠生成,最终生成白色的粉末 | ①4Na+O2═2Na2O Na2O+H2O═2NaOH 2Na+2H2O═2NaOH+H2↑ 2NaOH+CO2═Na2CO3+H2O |
| 将一块Na置于石棉网上,点燃酒精灯加热 | 钠先熔成小球,剧烈燃烧并发出黄色的火焰,生成②淡黄色色的粉末 | 2Na+O2 ═Na2O2 |
| 往上述生成的 Na2O2上滴加蒸馏水 | 生成的气体能使带火星的木条复燃 | 该气体为③O2 |
(1)钠的化学性质活泼,在自然界中全部以化合态形态(填“游离态”或“化合态”)存在,因此少量钠应保存在煤油中.
(2)写出Na2O2的一种用途:作供氧剂或利用强氧化性杀菌消毒.
2.下列物质的性质递变规律正确的是( )
| A. | O、S、Na的原子半径依次增大 | B. | LiOH、KOH、CsOH的碱性依次减弱 | ||
| C. | H2CO3的酸性比H3BO3的酸性弱 | D. | Cl-、Br-、I-的还原性依次减弱 |
