题目内容
12.取未知天然氨基酸A 66.50g进行元素分析,与强碱溶液共热,在标准状况下收集到N 25.60L(假设氮全部转化).已知氨基酸1个分子中含有一个氮原子,又取2.66gA溶于水配成溶液,用0.80mol/LNaOH溶液滴定耗去50.00mL恰好中和.试求:(1)氨基酸A的摩尔质量
(2)氨基酸A分子中含羧基的个数
(3)求氨基酸A的化学式;请写出A具有对称结构M氨基酸的简式.
分析 (1)根据n=$\frac{V}{{V}_{m}}$计算氮气的物质的量,根据N元素守恒计算n(-NH2),进而确定氨基酸的物质的量,再根据M=$\frac{m}{n}$计算该氨基酸的摩尔质量;
(2)计算2.66g氨基酸的物质的量、消耗NaOH的物质的量,设氨基酸有x个-COOH,则:R(COOH)x~~xNaOH,据此计算羧基数目;
(3)设氨基酸分子中含有n个CH2,根据含有的氨基、羧基数目确定氨基酸的分子式表达式,结合相对分子质量确定分子式,书写具有对称结构M氨基酸结构简式.
解答 解:(1)m(A)=66.5g,n(-NH2)=2n(N2)=2×$\frac{5.6L}{22.4L/mol}$=0.5 mol
氨基酸A的摩尔质量为:M(A)=66.5g÷0.5mol=133g/mol
答:氨基酸A的摩尔质量为133g/mol;
(2)2.26gA的物质的量为:2.66g÷133g/mol=0.02mmol
消耗氢氧化钠的物质的量=0.8mol/L×0.05L=0.04mol
设氨基酸有x个-COOH,则:
R(COOH)x~~x NaOH
1 x
0.02mol 0.04mol
x=$\frac{0.04mol×1}{0.02mol}$=2,即A含2个-COOH,
答:氨基酸A分子中含有2个羧基;
(3)设氨基酸A的结构简式为:HOOC-CH(NH2)-(CH2)n-COOH,则:
氨氨基酸A化学式为:C3+nH5+2nO4N,
有:12×(3+n)+5+2n+16×4+14=133
解得n=1,
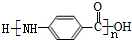
所以氨基酸A化学式为:C4H7O4N,A具有对称结构M氨基酸的结构简式: ,
,
答:氨基酸A化学式为:C4H7O4N,A具有对称结构M氨基酸的结构简式: .
.
点评 本题考查了有机物结构简式、结构式的确定,为高频考点,侧重于学生的分析、计算能力的考查,题目难度中等,明确常见有机物结构与性质为解答关键,

| A. | 能使溴水褪色 | B. | 能与新制Cu(OH)2悬浊液反应 | ||
| C. | 与足量的氢气反应生成1-丙醇 | D. | 不能发生银镜反应 |
| A. | 由乙酸和乙醇制乙酸乙酯 | B. | 由乙醇制乙烯 | ||
| C. | 由丙烯与溴制1,2-二溴丙烷 | D. | 由甲苯氧化制苯甲酸 |
| A. | 干燥的蓝色石蕊试纸 | B. | 硝酸银溶液 | ||
| C. | 干燥的有色布条 | D. | 湿润的碘化钾淀粉试纸 |
| A. | Na+、Ba2+、SO42-、Cl- | B. | Mg2+、K+、Cl-、NO3- | ||
| C. | H+、K+、CO32-、NO3- | D. | Ag+、Ca2+、Cl-、HCO3- |

| A. | 该装置中CCl4的作用是除去产物HBr中混有的Br2蒸气 | |
| B. | 若将液溴改为浓溴水,该反应也能进行 | |
| C. | 通过AgNO3溶液中有淡黄色沉淀产生,说明由苯制溴苯的反应是取代反应 | |
| D. | 该装置中左侧长导管的作用是导气兼冷凝回流 |
| A. | Al2(SO4)3═2Al3++3SO42- | B. | NaHCO3═Na++H++CO32- | ||
| C. | Ba(OH)2═Ba2++(OH-)2 | D. | Na2SO3═Na++SO32- |
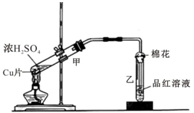 如图为浓硫酸与铜片反应的装置.请回答:
如图为浓硫酸与铜片反应的装置.请回答: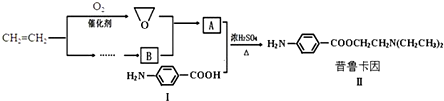

 .
.