题目内容
19. 水合肼(N2H4•H2O)又名水合联氨,无色透明,具有腐蚀性和强还原性的碱性液体,它是一种重要的化工试剂,利用尿素法生产水合肼的原理为:
水合肼(N2H4•H2O)又名水合联氨,无色透明,具有腐蚀性和强还原性的碱性液体,它是一种重要的化工试剂,利用尿素法生产水合肼的原理为:CO(NH2)2+2NaOH+NaClO=Na2CO3+N2H4•H2O+NaCl
实验一:制备NaClO溶液.(实验装置如图1所示)
(1)配制30%NaOH溶液时,所需玻璃仪器除量筒外还有BD(填标号).
A.容量瓶 B.烧杯 C.烧瓶 D.玻璃棒
(2)锥形瓶中发生反应的离子方程式是Cl2+2OH-=ClO-+Cl-+H2O.
(3)设计实验方案:用中和滴定原理测定反应后锥形瓶中剩余NaOH的浓度(实验提供的试剂:H2O2溶液、FeCl2溶液、0.10mol•L-1盐酸、酚酞试液):取一定量锥形瓶内混合溶液,加入适量的H2O2溶液后,滴加2~3滴酚酞试液,用 0.10mol•L-1盐酸滴定,重复上述操作2~3次.
实验二:制取水合肼.(实验装置如右图2所示)
(4)控制反应温度,将分液漏斗中溶液缓慢滴入三颈烧瓶中,充分反应.加热蒸馏三颈烧瓶内的溶液,收集108~114℃馏分.分液漏斗中的溶液是B(填标号).A.CO (NH2) 2溶液 B.NaOH和NaClO混合溶液,原因是:N2H4•H2O+2NaClO=N2↑+3H2O+2NaCl(用化学方程式表示).
实验三:测定馏分中肼含量.
(5)①称取馏分5.0g,加入适量NaHCO3固体,加水配成250mL溶液,移出25.00mL置于锥形瓶中,并滴加2~3滴淀粉溶液,用0.10mol•L-1的I2溶液滴定.滴定过程中,溶液的pH保持在6.5左右.(已知:N2H4•H2O+2I2=N2↑+4HI+H2O)
滴定时,碘的标准溶液盛放在酸式(填“酸式”或“碱式”)滴定管中;本实验滴定终点的现象为溶液出现蓝色且半分钟内不消失.
②实验测得消耗I2溶液的平均值为18.00mL,馏分中水合肼(N2H4•H2O)的质量分数为9%.
分析 (1)用天平称量质量,在烧杯中加水溶解,并用玻璃棒搅拌;
(2)锥形瓶中氯气与氢氧化钠反应生成氯化钠、次氯酸钠与水;
(3)用过氧化氢除去溶液中NaClO,用酚酞作指示剂,用盐酸滴定,重复测定,减少误差;
(4)N2H4•H2O具有强还原性,容易被过量的NaClO氧化;
(5)①碘的标准溶液具有氧化性,可以腐蚀橡皮管,应盛放在酸式滴定管中;肼反应完全,再滴入碘的标准溶液后,遇淀粉变蓝色;
②根据方程式N2H4•H2O+2I2=N2↑+4HI+H2O计算.
解答 解:(1)用天平称量质量,在烧杯中加水溶解,并用玻璃棒搅拌,需要玻璃仪器有:烧杯、玻璃棒,
故选:BD,
(2)锥形瓶中氯气与氢氧化钠反应生成氯化钠、次氯酸钠与水,反应离子方程式为:Cl2+2OH-=ClO-+Cl-+H2O,
故答案为:Cl2+2OH-=ClO-+Cl-+H2O;
(3)用过氧化氢除去溶液中NaClO,用酚酞作指示剂,用中和滴定原理测定反应后锥形瓶中剩余NaOH的浓度:取一定量锥形瓶内混合溶液,加入适量的H2O2溶液后,滴加2~3滴酚酞试液,用 0.10mol•L-1盐酸滴定,重复上述操作2~3次,
故答案为:取一定量锥形瓶内混合溶液,加入适量的H2O2溶液后,滴加2~3滴酚酞试液,用 0.10mol•L-1盐酸滴定,重复上述操作2~3次;
(4)N2H4•H2O具有强还原性,容易被过量的NaClO氧化,会发生反应:N2H4•H2O+2NaClO=N2↑+3H2O+2NaCl,应将NaOH和NaClO混合溶液滴入CO (NH2) 2溶液中,故分液漏斗中盛放的为,NaOH和NaClO混合溶液,
故答案为:B;N2H4•H2O+2NaClO=N2↑+3H2O+2NaCl;
(5)①碘的标准溶液具有氧化性,可以腐蚀橡皮管,应盛放在酸式滴定管中;肼反应完全,再滴入碘的标准溶液后,遇淀粉变蓝色,实验滴定终点的现象为:溶液出现蓝色且半分钟内不消失,
故答案为:酸式;溶液出现蓝色且半分钟内不消失;
②设馏分中水合肼(N2H4•H2O)的质量分数为a,则:
N2H4•H2O+2I2=N2↑+4HI+H2O
50g 2mol
5g×a 0.018L×0.1mol/L×$\frac{250mL}{25mL}$
所以50g:5g×a=2mol:0.018L×0.1mol/L×$\frac{250mL}{25mL}$
解得a=9%,
故答案为:9%.
点评 本题考查物质制备实验、物质含量测定,注意利用题目信息判断溶液添加顺序,较好的考查学生对实验原理的理解、知识迁移应用,难度中等.

 新课标阶梯阅读训练系列答案
新课标阶梯阅读训练系列答案 口算心算速算应用题系列答案
口算心算速算应用题系列答案 同步拓展阅读系列答案
同步拓展阅读系列答案| A. | Cu(OH)2与H2SO4 | B. | Ba(OH)2与H2SO4 | C. | Fe(OH)3与HCl | D. | HNO3与KOH |
| A. | 常温常压32g O2 含2NA个原子 | |
| B. | 标准状况下11.2L H2O 含有的原子数目为1.5NA | |
| C. | 1mol的Cl- 含有NA个电子 | |
| D. | 0.5mol/L的NaCl 溶液中Cl-的个数为0.5 NA |
| A. | 元素原子最外层电子数越多,元素金属性越强 | |
| B. | 非金属元素的非金属性越强,其氧化物对应水化物的酸性也一定越强 | |
| C. | Si、P、S、Cl元素的单质与氢气化合越来越容易 | |
| D. | F-、O2-、Mg2+、Na+离子半径逐渐减小 |
| A. | Fe2+ | B. | Mg2+ | C. | Cl- | D. | Ba2+ |
| X | 动植物生长不可缺少的元素,是蛋白质的重要成分 |
| Y | 地壳中含量居第一位 |
| Z | 短周期中其原子半径最大 |
| Q | 生活中大量使用其合金制品,工业上可用电解其氧化物的方法制备其单质 |
| M | 海水中大量富集的元素之一,其最高正化合价与负价的代数和为6 |
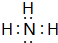 .
.(2)已知37Rb和53I都位于第五周期,分别与Z和M同一主族.下列有关说法正确的是ACD(填序号).
A.原子半径:Rb>I
B.RbM中含有共价键
C.气态氢化物热稳定性:M>I
D.Rb、Q、M的最高价氧化物对应的水化物可以两两发生反应
(3)化合物QX导热性好,热膨胀系数小,是良好的耐热冲击材料.有关化合物QX的制备及化学性质如下(所有热量数据均已折合为25℃、101.3 kPa条件下的数值).
①可用Q和X的单质在800~1 000℃制得,每生成1 mol QX,吸收a kJ的热量.
②可用Q的氧化物、焦炭和X的单质在1 600~1 750℃生成QX,每消耗18 g碳生成1 mol QX,吸收b kJ的热量.
请根据上述信息写出在理论上Q的氧化物跟焦炭反应生成Q单质和CO的热化学方程式Al2O3(s)+3C(s)=2Al(s)+3CO(g)△H=(2b-2a) kJ/mol.
(4)X、Y组成的一种无色气体遇空气变为红棕色.标准状况下将40 L该无色气体与15 L氧气通入一定浓度的NaOH溶液中,恰好被完全吸收,同时生成两种盐.请写出该反应的离子方程式8NO+3O2+8OH-=2NO2-+6NO3-+4H2O.
| A. | 铁跟稀硫酸反应:Fe+2H+═Fe2++H2↑ | |
| B. | 碳酸氢钙溶液跟盐酸反应:Ca(HCO3)2+2H+═Ca2++2H2O+2CO2↑ | |
| C. | 醋酸跟氢氧化钾溶液反应:CH3COOH+OH-═CH3COO-+H2O | |
| D. | 碳酸镁跟硫酸反应:MgCO3+2H+═Mg2++H2O+CO2↑ |
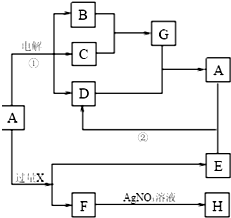 已知A是由两种中学常见元素组成的化合物,H、D为白色沉淀,E的焰色反应为黄色.A~H各物质之间的关系如图(反应中部分产物已略去,除气体间的反应物外,其余反应均在溶液中进行):
已知A是由两种中学常见元素组成的化合物,H、D为白色沉淀,E的焰色反应为黄色.A~H各物质之间的关系如图(反应中部分产物已略去,除气体间的反应物外,其余反应均在溶液中进行):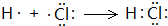 .
.